Clear Sky Science · es
La succinación de INSIG1/2 mediada por la función secundaria de ADSL promueve la lipogénesis y la tumorogénesis hepática
Cómo el azúcar alimenta los tumores hepáticos
¿Por qué las células cancerosas ansían el azúcar y cómo lo convierten en los materiales básicos necesarios para crecer? Este estudio descubre un cableado oculto dentro de las células del cáncer de hígado que vincula la hiperglucemia directamente con la producción de grasa y el crecimiento tumoral. Al rastrear una cadena de eventos desde la glucosa fuera de la célula hasta los interruptores lipogénicos en su interior, los investigadores también revelan cómo un fármaco ya usado contra el VIH podría reutilizarse para frenar el cáncer hepático.
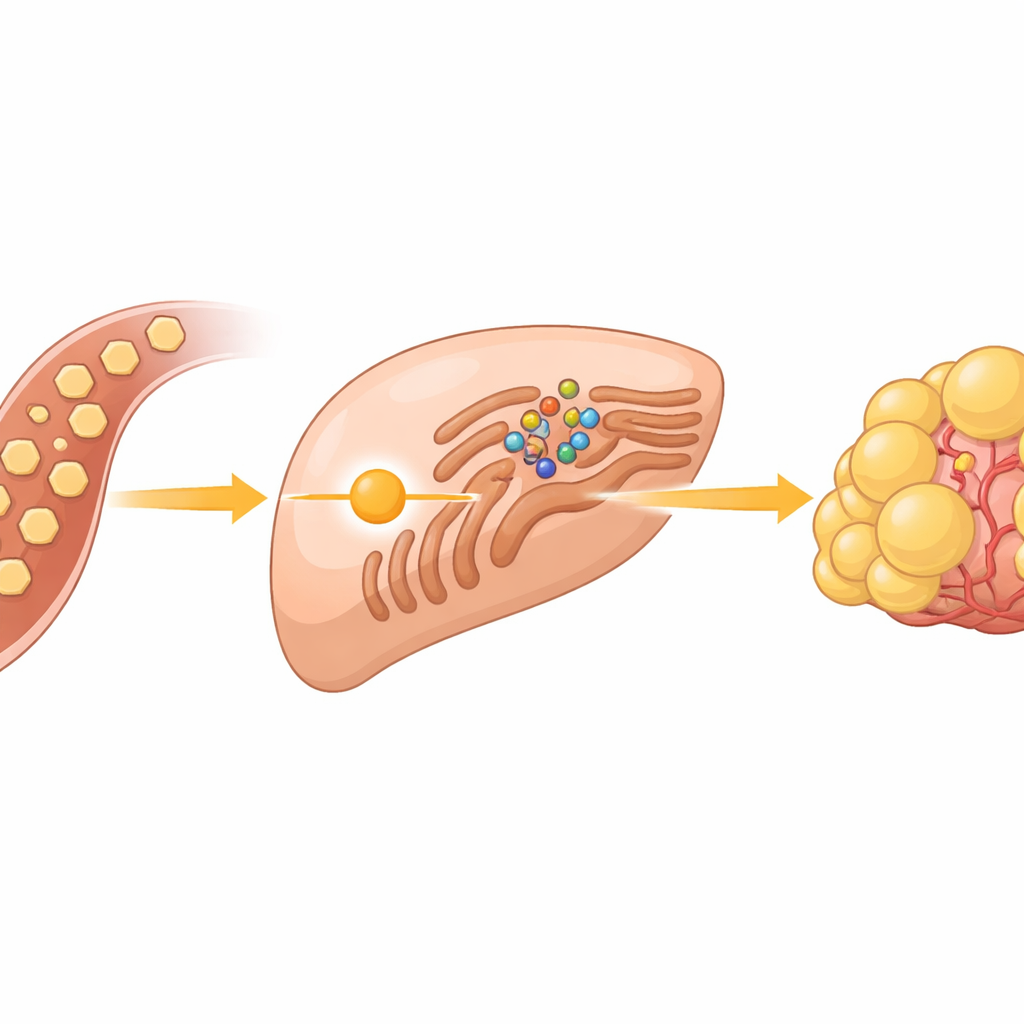
Un sensor de azúcar oculto dentro de las células cancerosas
Las células cancerosas son famosas por quemar azúcar rápidamente, incluso cuando hay oxígeno disponible, un comportamiento conocido como efecto Warburg. En los tumores hepáticos, este afán por la glucosa hace más que proporcionar energía; también alimenta la creación de grasas que construyen nuevas membranas celulares. El equipo se centró en un grupo de proteínas llamadas SREBPs, interruptores maestros que activan genes para producir lípidos y colesterol. En condiciones normales, estos interruptores están controlados en una estructura celular llamada retículo endoplásmico, donde quedan anclados por una proteína sensor llamada INSIG y su socia SCAP. El gran misterio ha sido cómo el exceso de glucosa indica a este sistema que libere a las SREBPs y active la producción de grasas.
Una enzima con un segundo trabajo
Los investigadores descubrieron que una enzima llamada ADSL, conocida sobre todo por ayudar a las células a sintetizar bloques de construcción del ADN, tiene un sorprendente segundo cometido en el cáncer de hígado. Cuando los niveles de glucosa son altos, se activa una quinasa señalizadora llamada PKCε. PKCε añade entonces un grupo fosfato a ADSL en una posición específica, lo que provoca que ADSL se desplace del citosol hacia la superficie del retículo endoplásmico. Allí, ADSL se une físicamente a las proteínas INSIG. Esta reubicación convierte a ADSL de una mera maquinaria metabólica en una fábrica química local que puede influir directamente en los interruptores lipogénicos.
Cicatrices químicas que desbloquean la producción de grasa
Una vez que ADSL se sitúa junto a INSIG, genera una pequeña molécula llamada fumarato como parte de su química habitual. En este nuevo entorno, el fumarato reacciona con un aminoácido concreto en INSIG, formando una “cicatriz” química permanente conocida como succinación. Esta cicatriz se forma en un sitio de cisteína clave (C167 en INSIG1 y C111 en INSIG2) que normalmente ayuda a INSIG a unirse a oxisteroles, mensajeros similares al colesterol que mantienen al complejo SCAP–SREBP anclado en su sitio. La succinación debilita la afinidad de INSIG por estos mensajeros y por SCAP, permitiendo que el complejo SCAP–SREBP abandone el retículo endoplásmico y viaje al aparato de Golgi. Allí, SREBP se escinde y su fragmento activo se traslada al núcleo, activando un conjunto de genes que impulsan la producción de lípidos y colesterol, alimentando el rápido crecimiento de las células tumorales.
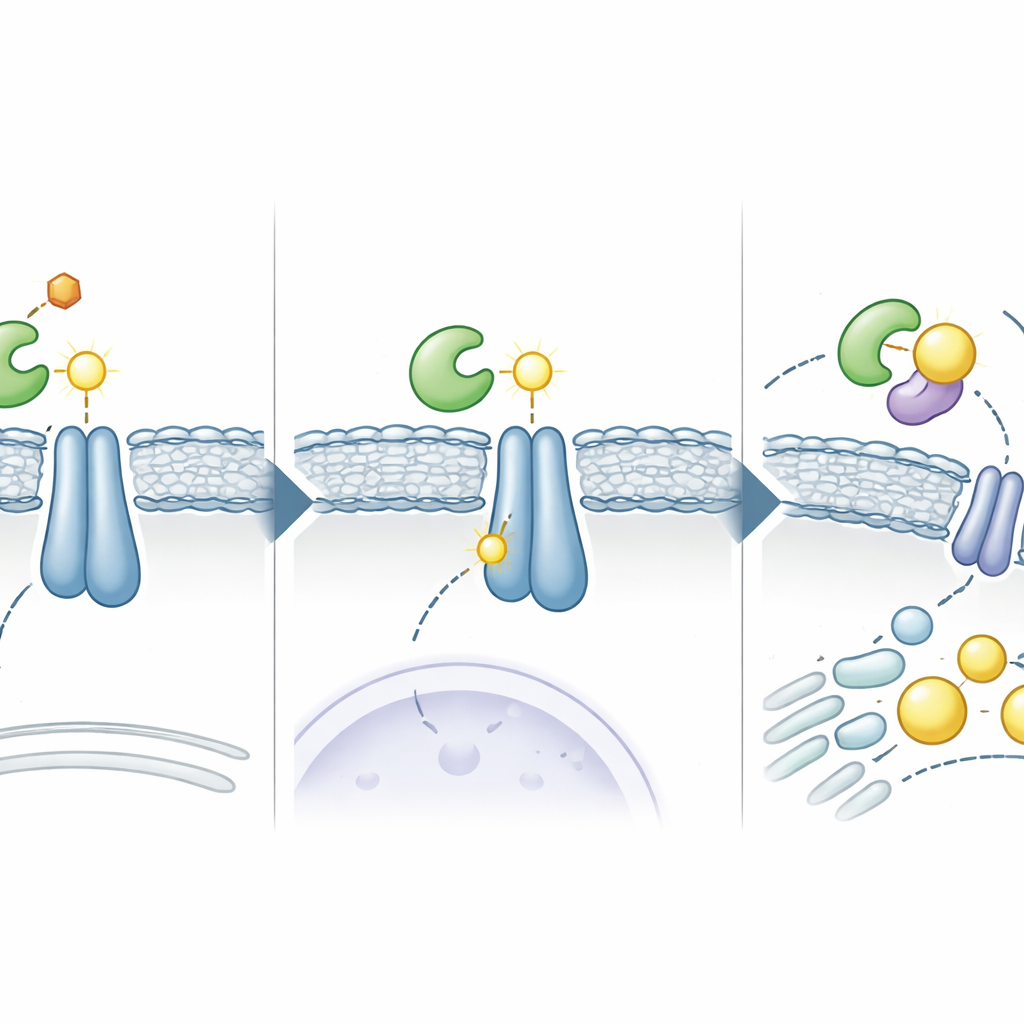
De los circuitos celulares al reposicionamiento de fármacos
Para comprobar si esta vía podía volverse contra el cáncer, los científicos emplearon cribado computacional de fármacos aprobados para encontrar moléculas que pudieran insertarse en la interfaz entre ADSL e INSIG. Identificaron Elsulfavirina, un medicamento contra el VIH, como candidato fuerte. En experimentos de laboratorio y simulaciones por ordenador, Elsulfavirina interrumpió la unión entre ADSL e INSIG, redujo la succinación de INSIG y bloqueó la activación de SREBP en células de cáncer hepático. Como resultado, las células sintetizaron menos grasas, almacenaron menos gotas lipídicas y crecieron más despacio. En modelos de ratón de cáncer de hígado, Elsulfavirina redujo el tamaño de los tumores, y funcionó aún mejor cuando se combinó con el fármaco estándar para cáncer hepático Lenvatinib, lo que sugiere un potente golpe combinado que ataca tanto las señales de crecimiento como las demandas metabólicas.
Qué significa esto para los pacientes
Para vincular estos hallazgos con la enfermedad humana, el equipo examinó muestras de tumores hepáticos humanos. Los tumores con altos niveles de ADSL fosforilada, INSIG fuertemente succinada y abundante SREBP en el núcleo se asociaron con una peor supervivencia de los pacientes. En otras palabras, el mismo circuito sensor de glucosa mapeado en células y ratones parece estar activo en cánceres hepáticos humanos agresivos. El trabajo muestra que los tumores hepáticos pueden detectar directamente el exceso de glucosa y convertirlo en un programa lipogénico pro‑crecimiento mediante la función secundaria (moonlighting) de ADSL. También pone de relieve a Elsulfavirina como candidato prometedor para reposicionamiento, abriendo una posible nueva estrategia para cortar el suministro de lípidos que los tumores hepáticos necesitan para prosperar.
Cita: Duan, Y., Wang, S., Liu, J. et al. INSIG1/2 succination mediated by the moonlighting function of ADSL promotes lipogenesis and liver tumorigenesis. Nat Commun 17, 4002 (2026). https://doi.org/10.1038/s41467-026-70583-0
Palabras clave: cáncer de hígado, metabolismo del cáncer, lipogénesis, vía SREBP, reposicionamiento de fármacos