Clear Sky Science · de
INSIG1/2-Succination vermittelt durch die Moonlighting-Funktion von ADSL fördert Lipogenese und Lebertumorentstehung
Wie Zucker Lebertumoren nährt
Warum verlangen Krebszellen nach Zucker, und wie verwandeln sie ihn in die Rohstoffe, die zum Wachsen nötig sind? Diese Studie deckt eine verborgene Schaltung in Leberkrebszellen auf, die hohen Blutzucker direkt mit Fettbildung und Tumorwachstum verknüpft. Indem die Forschenden eine Kette von Ereignissen vom Glukoseangebot außerhalb der Zelle bis zu den Fettproduktionsschaltern im Inneren nachzeichnen, zeigen sie außerdem, wie ein vorhandenes HIV-Medikament umfunktioniert werden könnte, um Leberkrebs zu bremsen.
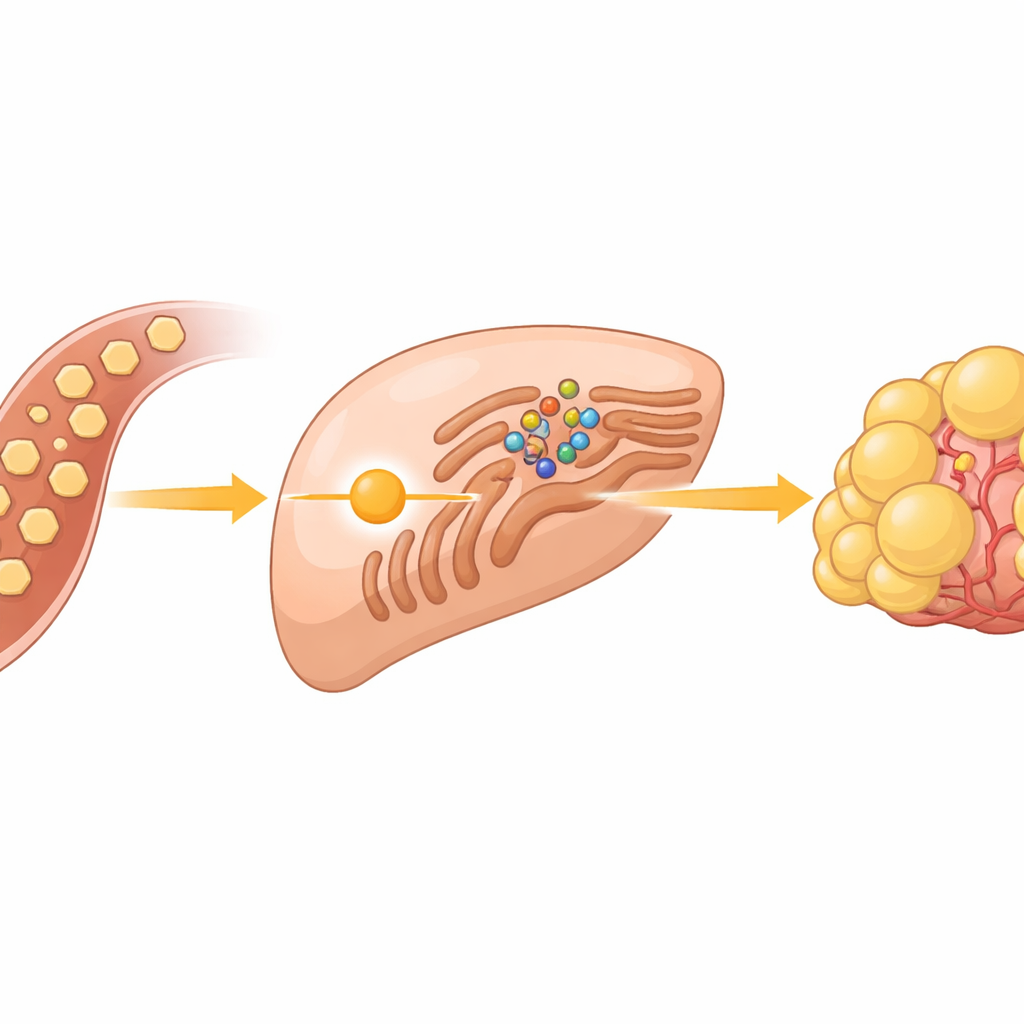
Ein versteckter Zuckersensor in Krebszellen
Krebszellen sind dafür bekannt, Zucker schnell zu verbrennen, selbst wenn ausreichend Sauerstoff vorhanden ist — ein Verhalten, das als Warburg-Effekt bekannt ist. In Lebertumoren liefert dieser Zuckerrausch nicht nur Energie; er speist auch die Herstellung von Fetten, die neue Zellmembranen aufbauen. Das Team konzentrierte sich auf eine Gruppe von Proteinen namens SREBPs, Schaltmeister, die Gene für die Synthese von Fetten und Cholesterin einschalten. Unter normalen Bedingungen werden diese Schalter im endoplasmatischen Retikulum zurückgehalten, wo sie durch ein Sensorsystem aus dem Protein INSIG und seinem Partner SCAP verankert sind. Das große Rätsel war, wie zusätzliche Glukose dieses System veranlasst, SREBPs freizugeben und die Fettproduktion zu starten.
Ein Enzym mit zweiter Aufgabe
Die Forschenden entdeckten, dass ein Enzym namens ADSL, das vor allem dafür bekannt ist, Bausteine der DNA herzustellen, in Leberkrebs eine überraschende zweite Aufgabe hat. Bei hohen Glukosespiegeln aktiviert sich ein Signalkinase-Enzym namens PKCε. PKCε fügt daraufhin an einer bestimmten Stelle eine Phosphatmarke an ADSL an, wodurch ADSL vom wässrigen Zellinneren zur Oberfläche des endoplasmatischen Retikulums umzieht. Dort bindet ADSL physisch an INSIG-Proteine. Diese Umsiedlung verwandelt ADSL von einem einfachen Stoffwechselarbeiter in eine lokale chemische Fabrik, die die Fett-Schalter direkt beeinflussen kann.
Chemische Vernarbung, die Fettproduktion freisetzt
Sobald ADSL neben INSIG geparkt ist, erzeugt es im Rahmen seiner üblichen Chemie ein kleines Molekül namens Fumarat. In diesem neuen Kontext reagiert Fumarat mit einer bestimmten Aminosäure von INSIG und bildet eine permanente chemische "Narbe", bekannt als Succination. Diese Narbe entsteht an einer Schlüssel-Cystein-Stelle (C167 in INSIG1 und C111 in INSIG2), die normalerweise INSIG dabei hilft, Oxysterole zu binden — cholesterinähnliche Botenstoffe, die den SCAP–SREBP-Komplex an Ort und Stelle halten. Succination schwächt INSIGs Bindung an diese Botenstoffe und an SCAP, sodass der SCAP–SREBP-Komplex das endoplasmatische Retikulum verlassen und zum Golgi gelangen kann. Dort wird SREBP geschnitten und sein aktiver Fragment wandert in den Zellkern, wo es ein Programm von Genen einschaltet, das Fett- und Cholesterinproduktion antreibt und schnelles Tumorzellwachstum fördert.
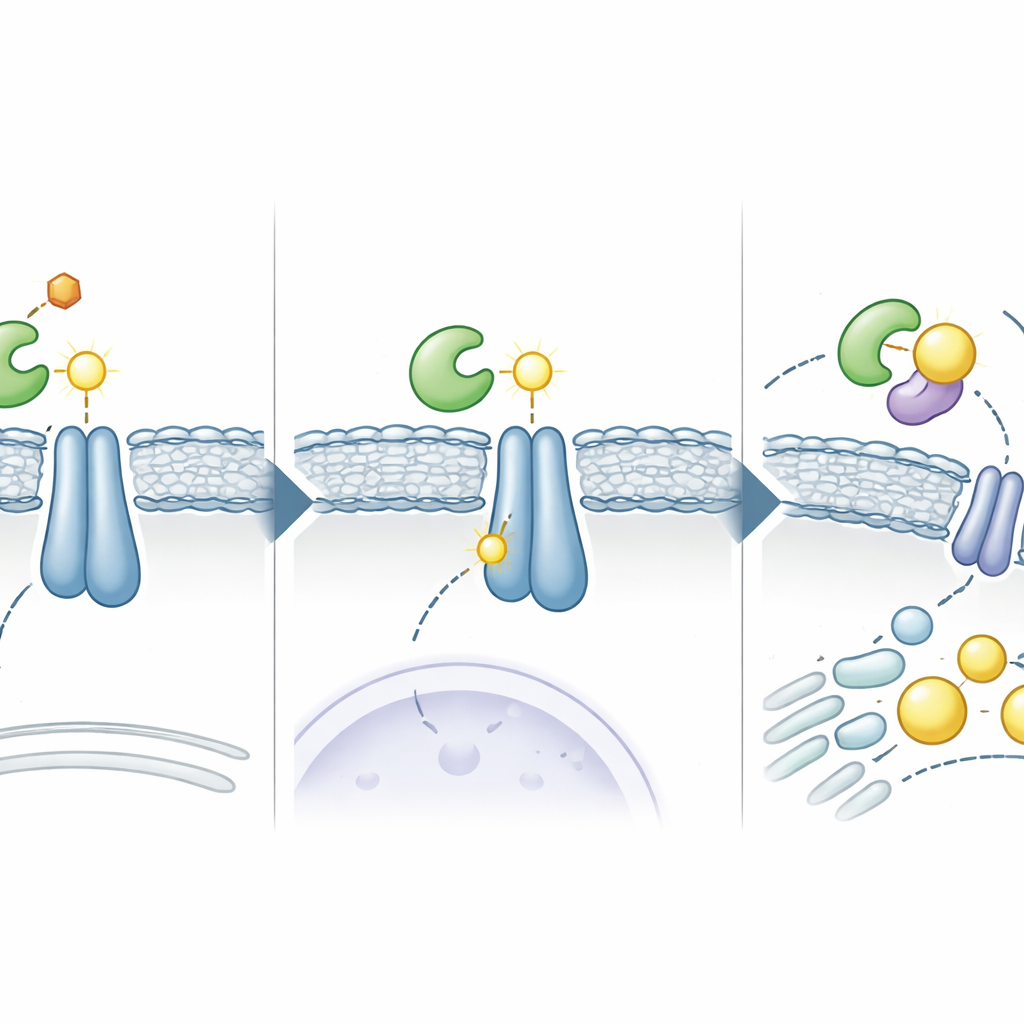
Von Zellschaltkreisen zur Arzneimittel-Repositionierung
Um zu prüfen, ob dieser Weg gegen den Krebs genutzt werden kann, setzten die Wissenschaftler*innen computergestützte Bildschirmverfahren ein, um zugelassene Arzneistoffe zu finden, die sich in die Schnittstelle zwischen ADSL und INSIG einklemmen könnten. Sie identifizierten Elsulfavirine, ein HIV-Medikament, als vielversprechenden Kandidaten. In Laborversuchen und Computersimulationen störte Elsulfavirine die Bindung zwischen ADSL und INSIG, verringerte die INSIG-Succination und blockierte die Aktivierung von SREBP in Leberkrebszellen. Infolgedessen produzierten die Zellen weniger Fette, lagerten weniger Lipidtröpfchen und wuchsen langsamer. In Mausmodellen von Leberkrebs verkleinerte Elsulfavirine Tumoren, und in Kombination mit dem Standardmedikament Lenvatinib wirkte es noch stärker — ein Hinweis auf einen wirksamen Doppelangriff auf Wachstumssignale und metabolische Bedürfnisse.
Was das für Patientinnen und Patienten bedeutet
Um diese Befunde mit realer Krankheit in Verbindung zu bringen, untersuchte das Team menschliche Lebertumorproben. Tumoren mit hohen Pegeln an phosphoryliertem ADSL, stark succiniertem INSIG und reichlich SREBP im Zellkern waren mit schlechterem Überleben der Patient*innen assoziiert. Mit anderen Worten: Dieselbe Zucker-sensierende Schaltung, die in Zellen und Mäusen kartiert wurde, scheint in aggressiven menschlichen Leberkrebserkrankungen aktiv zu sein. Die Arbeit zeigt, dass Lebertumoren zusätzlichen Glukosegehalt direkt erkennen und durch die "Moonlighting"-Funktion von ADSL in ein wachstumsförderndes Fettprogramm umwandeln können. Sie hebt zudem Elsulfavirine als vielversprechenden Kandidaten zur Repositionierung hervor und eröffnet eine potenzielle neue Strategie, die Fettzufuhr anzuzapfen, die Lebertumoren zum Gedeihen benötigen.
Zitation: Duan, Y., Wang, S., Liu, J. et al. INSIG1/2 succination mediated by the moonlighting function of ADSL promotes lipogenesis and liver tumorigenesis. Nat Commun 17, 4002 (2026). https://doi.org/10.1038/s41467-026-70583-0
Schlüsselwörter: Leberkrebs, Krebsstoffwechsel, Lipogenese, SREBP-Weg, Arzneimittel-Repositionierung