Clear Sky Science · fr
La succination d’INSIG1/2 médiée par la fonction secondaire d’ADSL favorise la lipogenèse et la tumorigenèse hépatique
Comment le sucre alimente les tumeurs hépatiques
Pourquoi les cellules cancéreuses ont-elles tant d’appétit pour le sucre, et comment le transforment-elles en matériaux bruts nécessaires à leur croissance ? Cette étude révèle un circuit caché au sein des cellules du cancer du foie qui relie directement l’hyperglycémie à la production de lipides et à la croissance tumorale. En retraçant une chaîne d’événements depuis le glucose extracellulaire jusqu’aux commutateurs lipogéniques intracellulaires, les chercheurs montrent aussi comment un médicament existant contre le VIH pourrait être réorienté pour ralentir le cancer du foie.
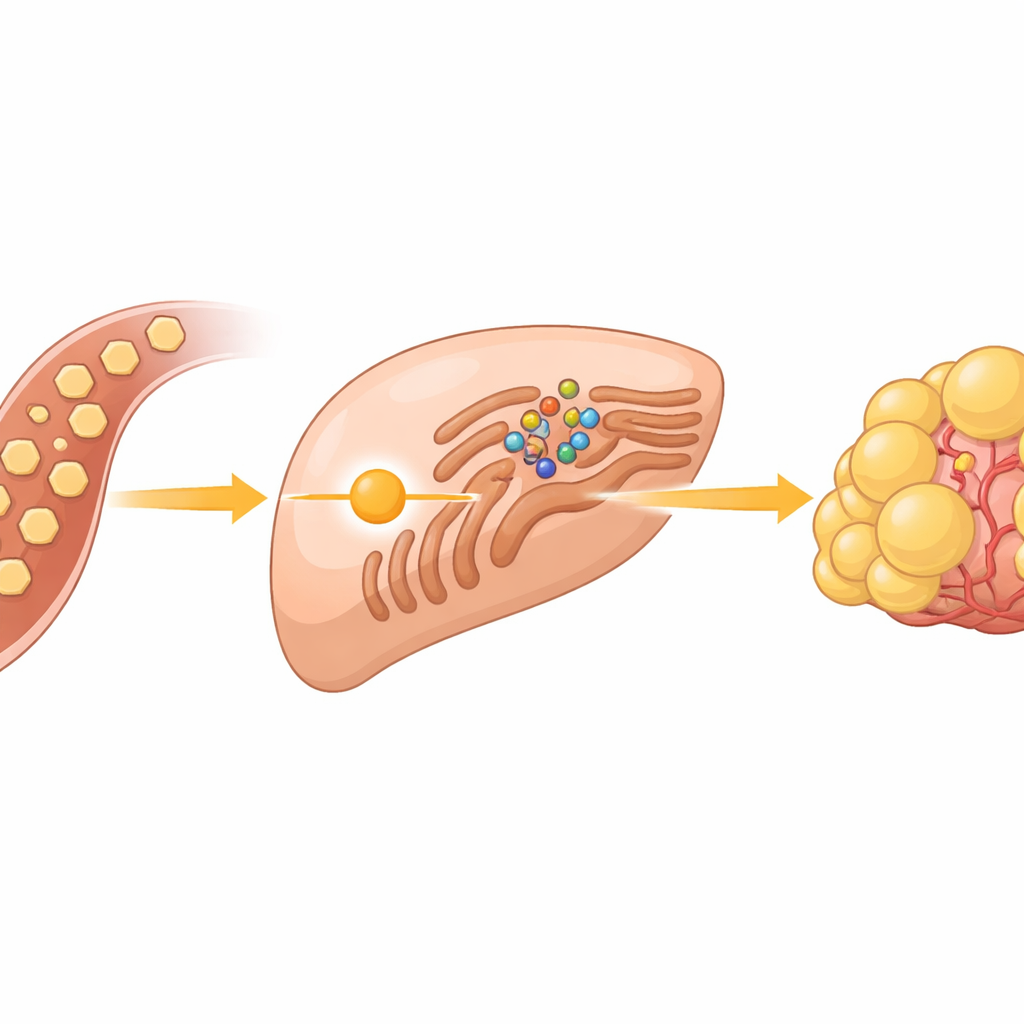
Un capteur de sucre caché à l’intérieur des cellules cancéreuses
Les cellules cancéreuses sont célèbres pour brûler le sucre rapidement, même en présence d’oxygène, comportement connu sous le nom d’effet Warburg. Dans les tumeurs hépatiques, cette consommation élevée de glucose fait plus que fournir de l’énergie : elle alimente aussi la création de lipides nécessaires à la formation de nouvelles membranes cellulaires. L’équipe s’est concentrée sur un groupe de protéines appelées SREBP, des commutateurs maîtres qui activent les gènes responsables de la synthèse des lipides et du cholestérol. Dans des conditions normales, ces commutateurs sont retenus au niveau d’une structure cellulaire appelée réticulum endoplasmique, où ils sont maintenus en place par une protéine capteur nommée INSIG et son partenaire SCAP. Le grand mystère était de savoir comment un surplus de glucose signale à ce système de libérer les SREBP et de lancer la production de lipides.
Une enzyme aux fonctions secondaires
Les chercheurs ont découvert qu’une enzyme appelée ADSL, surtout connue pour aider à la synthèse des briques de l’ADN, a une seconde fonction surprenante dans le cancer du foie. Lorsque les niveaux de glucose sont élevés, cela active une kinase de signalisation appelée PKCε. PKCε ajoute alors une marque phosphate sur ADSL à une position spécifique, provoquant le déplacement d’ADSL de l’intérieur aqueux de la cellule vers la surface du réticulum endoplasmique. Là, ADSL s’attache physiquement aux protéines INSIG. Ce repositionnement transforme ADSL d’un simple acteur métabolique en une usine chimique locale capable d’influencer directement les commutateurs de la synthèse lipidique.
Une cicatrice chimique qui déverrouille la production de lipides
Une fois qu’ADSL est positionné à côté d’INSIG, il génère une petite molécule appelée fumarate dans le cadre de sa chimie habituelle. Dans ce nouveau contexte, le fumarate réagit avec un acide aminé particulier d’INSIG, formant une « cicatrice » chimique permanente connue sous le nom de succination. Cette modification se produit sur un résidu de cystéine clé (C167 pour INSIG1 et C111 pour INSIG2) qui participe normalement à la liaison d’INSIG aux oxystérols, des messagers de type cholestérol qui maintiennent le complexe SCAP–SREBP ancré. La succination affaiblit l’affinité d’INSIG pour ces messagers et pour SCAP, permettant au complexe SCAP–SREBP de quitter le réticulum endoplasmique et de voyager vers le compartiment de Golgi. Là, SREBP est clivé et son fragment actif migre dans le noyau, activant une série de gènes qui stimulent la production de lipides et de cholestérol, alimentant ainsi la croissance rapide des cellules tumorales.
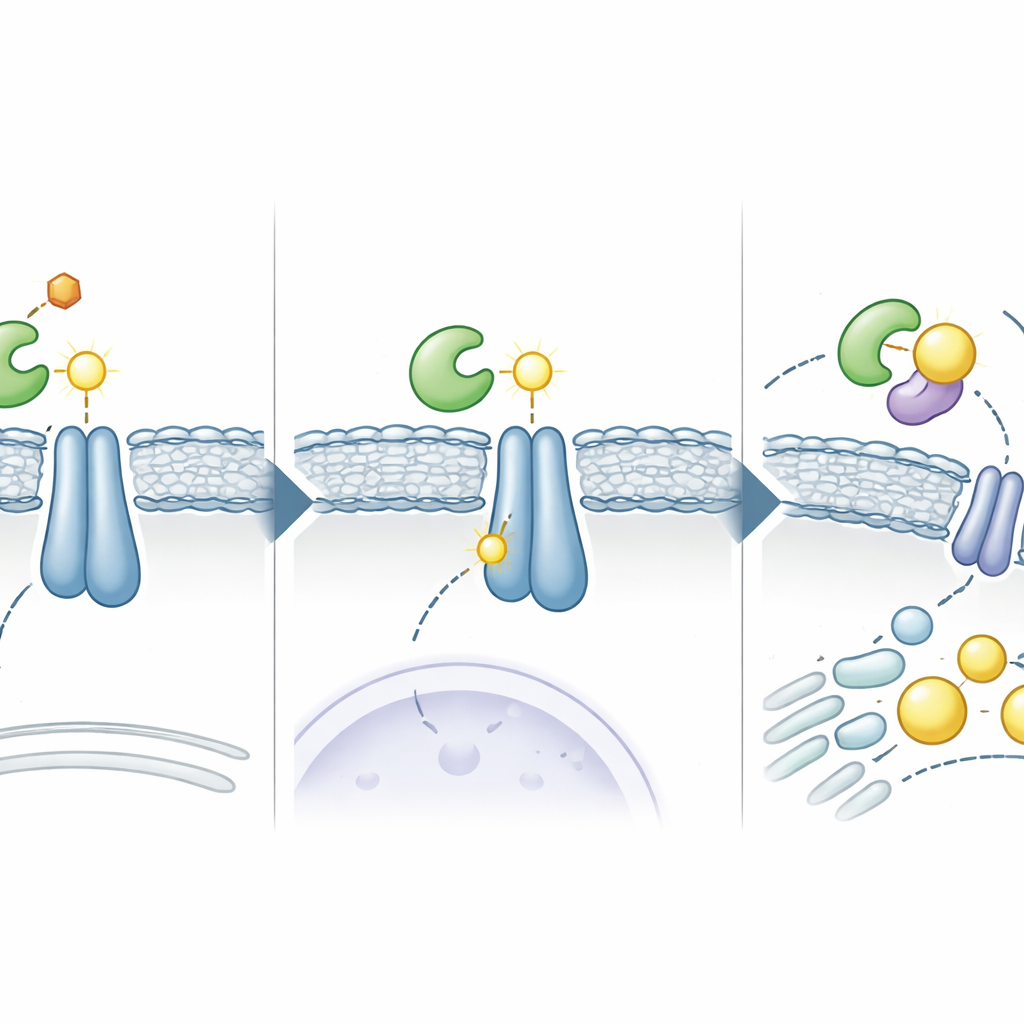
Des circuits cellulaires à la réaffectation de médicaments
Pour déterminer si cette voie pouvait être utilisée contre le cancer, les scientifiques ont réalisé un criblage informatisé de médicaments approuvés pour trouver des molécules susceptibles de s’insérer à l’interface entre ADSL et INSIG. Ils ont identifié l’elsulfavirine, un médicament anti‑VIH, comme un candidat prometteur. Dans des expériences en laboratoire et des simulations informatiques, l’elsulfavirine a perturbé la liaison entre ADSL et INSIG, réduit la succination d’INSIG et bloqué l’activation des SREBP dans des cellules de cancer hépatique. En conséquence, les cellules produisaient moins de lipides, stockaient moins de gouttelettes lipidiques et proliféraient plus lentement. Dans des modèles murins de cancer du foie, l’elsulfavirine a réduit la taille des tumeurs, et son effet était encore meilleur en association avec le traitement standard du cancer hépatique, le Lenvatinib, suggérant une combinaison puissante ciblant à la fois les signaux de croissance et les besoins métaboliques.
Ce que cela signifie pour les patients
Pour relier ces découvertes à la maladie humaine, l’équipe a examiné des échantillons de tumeurs hépatiques humaines. Les tumeurs présentant des niveaux élevés d’ADSL phosphorylé, d’INSIG fortement succinée et une abondance de SREBP nucléaire étaient associées à une survie patient plus faible. En d’autres termes, le même circuit de détection du glucose cartographié dans les cellules et les souris semble actif dans des cancers hépatiques humains agressifs. Ces travaux montrent que les tumeurs du foie peuvent percevoir directement un excès de glucose et le convertir en un programme lipogénique pro‑croissance via la fonction « moonlighting » d’ADSL. Ils mettent également en évidence l’elsulfavirine comme candidat prometteur pour la réaffectation, ouvrant une stratégie potentielle pour couper l’approvisionnement en lipides dont les tumeurs hépatiques ont besoin pour prospérer.
Citation: Duan, Y., Wang, S., Liu, J. et al. INSIG1/2 succination mediated by the moonlighting function of ADSL promotes lipogenesis and liver tumorigenesis. Nat Commun 17, 4002 (2026). https://doi.org/10.1038/s41467-026-70583-0
Mots-clés: cancer du foie, métabolisme du cancer, lipogenèse, voie SREBP, réaffectation de médicaments