Clear Sky Science · pt
INSIG1/2 succinação mediada pela função moonlighting da ADSL promove lipogênese e tumorigenese hepática
Como o açúcar alimenta tumores do fígado
Por que células cancerosas desejam tanto açúcar e como o transformam em matéria‑prima para crescer? Este estudo revela uma conexão escondida dentro de células de câncer hepático que liga diretamente a glicemia alta à produção de gordura e ao crescimento tumoral. Ao rastrear uma cadeia de eventos do glicose fora da célula até interruptores de síntese lipídica no seu interior, os pesquisadores também mostram como um medicamento já usado contra o HIV poderia ser reaproveitado para desacelerar o câncer de fígado.
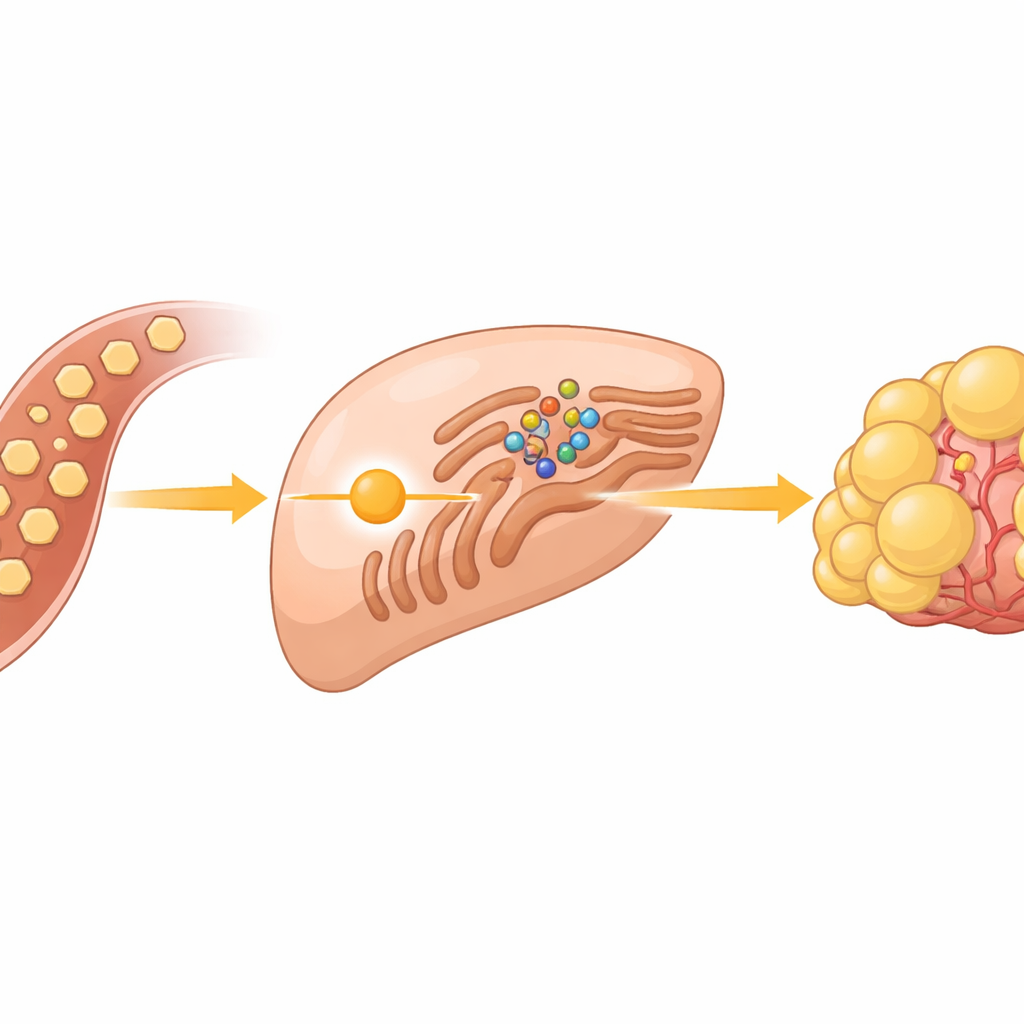
Um sensor de açúcar oculto dentro das células cancerosas
As células cancerosas são famosas por consumir açúcar rapidamente, mesmo quando há oxigênio disponível, um comportamento conhecido como efeito Warburg. Em tumores hepáticos, essa corrida pelo açúcar faz mais do que fornecer energia; também alimenta a criação de gorduras que constroem novas membranas celulares. A equipe concentrou‑se em um grupo de proteínas chamadas SREBPs, interruptores mestres que ligam genes para a síntese de lipídios e colesterol. Em condições normais, esses interruptores são mantidos sob controle em uma estrutura celular chamada retículo endoplasmático, onde ficam presos por uma proteína sensora chamada INSIG e sua parceira SCAP. O grande mistério tem sido como o excesso de glicose faz esse sistema liberar as SREBPs e iniciar a produção de gordura.
Uma enzima com um segundo trabalho
Os pesquisadores descobriram que uma enzima chamada ADSL, mais conhecida por ajudar células a construir blocos de DNA, tem uma surpreendente segunda função no câncer de fígado. Quando os níveis de glicose estão altos, ela ativa uma quinase de sinalização chamada PKCε. A PKCε então adiciona uma marca fosfato à ADSL em uma posição específica, fazendo com que a ADSL migre do citosol para a superfície do retículo endoplasmático. Lá, a ADSL se liga fisicamente às proteínas INSIG. Essa relocação transforma a ADSL de um agente metabólico em uma fábrica química local que pode influenciar diretamente os interruptores de síntese de gordura.
Cicatrização química que destrava a produção de gordura
Uma vez que a ADSL se posiciona ao lado da INSIG, ela gera uma pequena molécula chamada fumarato como parte de sua química habitual. Nesse novo contexto, o fumarato reage com um aminoácido específico na INSIG, formando uma “cicatriz” química permanente conhecida como succinação. Essa cicatriz ocorre em um sítio de cisteína chave (C167 na INSIG1 e C111 na INSIG2) que normalmente ajuda a INSIG a ligar oxisteróis, mensageiros semelhantes ao colesterol que mantêm o complexo SCAP–SREBP ancorado. A succinação enfraquece a afinidade da INSIG por esses mensageiros e por SCAP, permitindo que o complexo SCAP–SREBP saia do retículo endoplasmático e viaje até o Golgi. Lá, a SREBP é clivada e seu fragmento ativo entra no núcleo, ativando um conjunto de genes que impulsionam a produção de lipídios e colesterol, alimentando o rápido crescimento das células tumorais.
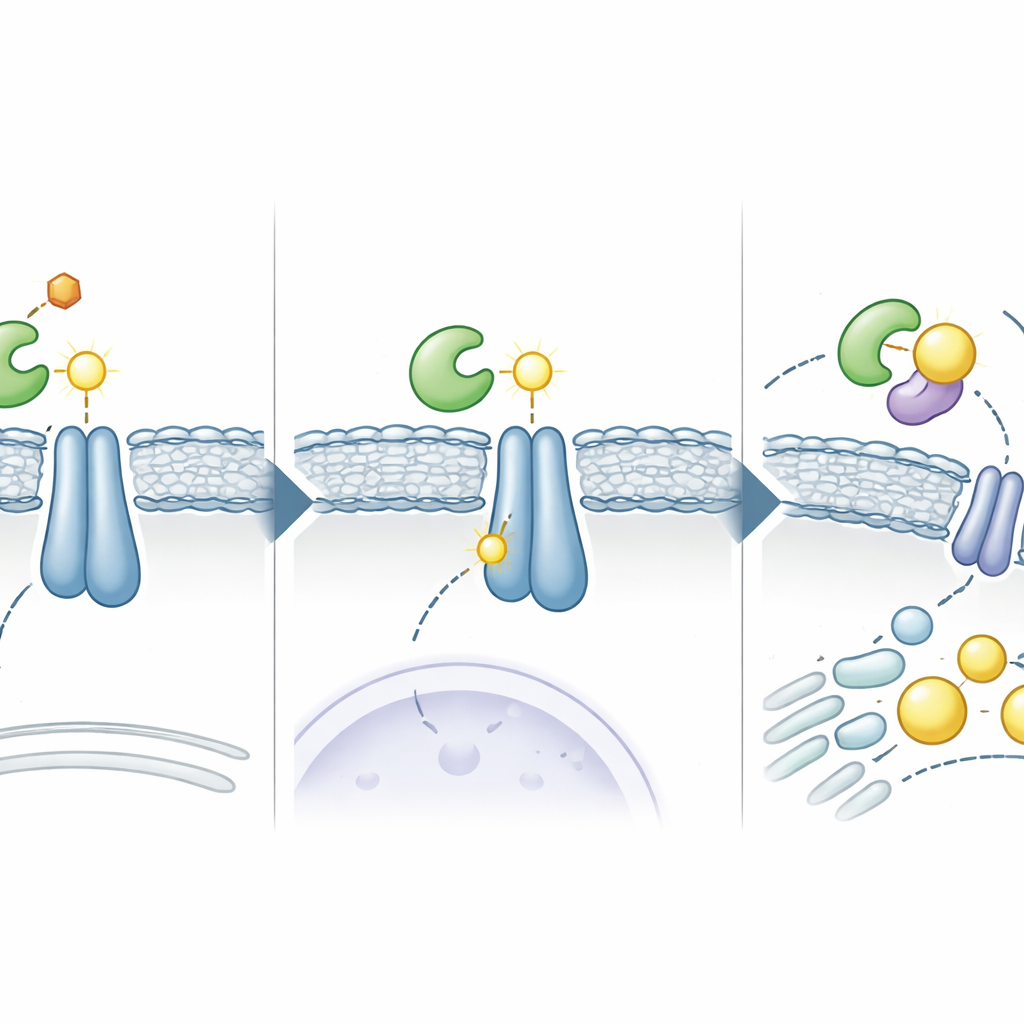
Dos circuitos celulares ao reuso de medicamentos
Para verificar se essa via poderia ser explorada contra o câncer, os cientistas realizaram triagens por computador de fármacos aprovados para encontrar moléculas que pudessem se inserir na interface entre ADSL e INSIG. Eles identificaram Elsulfavirina, um medicamento contra o HIV, como um forte candidato. Em experimentos de laboratório e simulações computacionais, a Elsulfavirina perturbou a interação entre ADSL e INSIG, reduziu a succinação da INSIG e bloqueou a ativação das SREBPs em células de câncer hepático. Como resultado, as células produziram menos gorduras, acumularam menos gotículas lipídicas e proliferaram mais lentamente. Em modelos murinos de câncer de fígado, a Elsulfavirina reduziu tumores, e mostrou efeito ainda maior quando combinada com o medicamento padrão para câncer hepático Lenvatinibe, sugerindo uma estratégia de duplo ataque que mira sinais de crescimento e demandas metabólicas.
O que isso significa para pacientes
Para conectar essas descobertas à doença humana, a equipe examinou amostras de tumores hepáticos humanos. Tumores com altos níveis de ADSL fosforilada, INSIG fortemente succinada e abundância de SREBP no núcleo associaram‑se a pior sobrevida dos pacientes. Em outras palavras, o mesmo circuito sensor de glicose mapeado em células e camundongos parece estar ativo em cânceres hepáticos humanos agressivos. O trabalho mostra que tumores do fígado podem detectar diretamente o excesso de glicose e convertê‑lo em um programa pró‑crescimento de lipogênese através da função “moonlighting” da ADSL. Também destaca a Elsulfavirina como um candidato promissor para repropósito, abrindo uma estratégia potencial para cortar o fornecimento de lipídios de que os tumores hepáticos precisam para prosperar.
Citação: Duan, Y., Wang, S., Liu, J. et al. INSIG1/2 succination mediated by the moonlighting function of ADSL promotes lipogenesis and liver tumorigenesis. Nat Commun 17, 4002 (2026). https://doi.org/10.1038/s41467-026-70583-0
Palavras-chave: câncer de fígado, metabolismo do câncer, lipogênese, via SREBP, repropósito de fármacos