Clear Sky Science · he
הסיכנון של INSIG1/2 באמצעות תפקוד הליקוי של ADSL מקדם ליפוגנזה ושגשוג גידולי בכבד
איך סוכר מזין גידולים בכבד
מדוע תאי סרטן משתוקקים לסוכר, וכיצד הם ממירים אותו לחומרי הגלם הדרושים לצמיחה? המחקר מגלה חיווט סמוי בתוך תאי סרטן של הכבד שמקשר בין רמות סוכר גבוהות בדם לבין יצירת שומנים וצמיחת גידול. בעקיבה אחר שרשרת אירועים מהגלוקוז שמחוץ לתא אל מתגי יצירת שומן עמוקים בתוכו, החוקרים מגלים גם כיצד תרופה קיימת נגד HIV יכולה להיות מותאמת מחדש כדי להאט את סרטן הכבד.
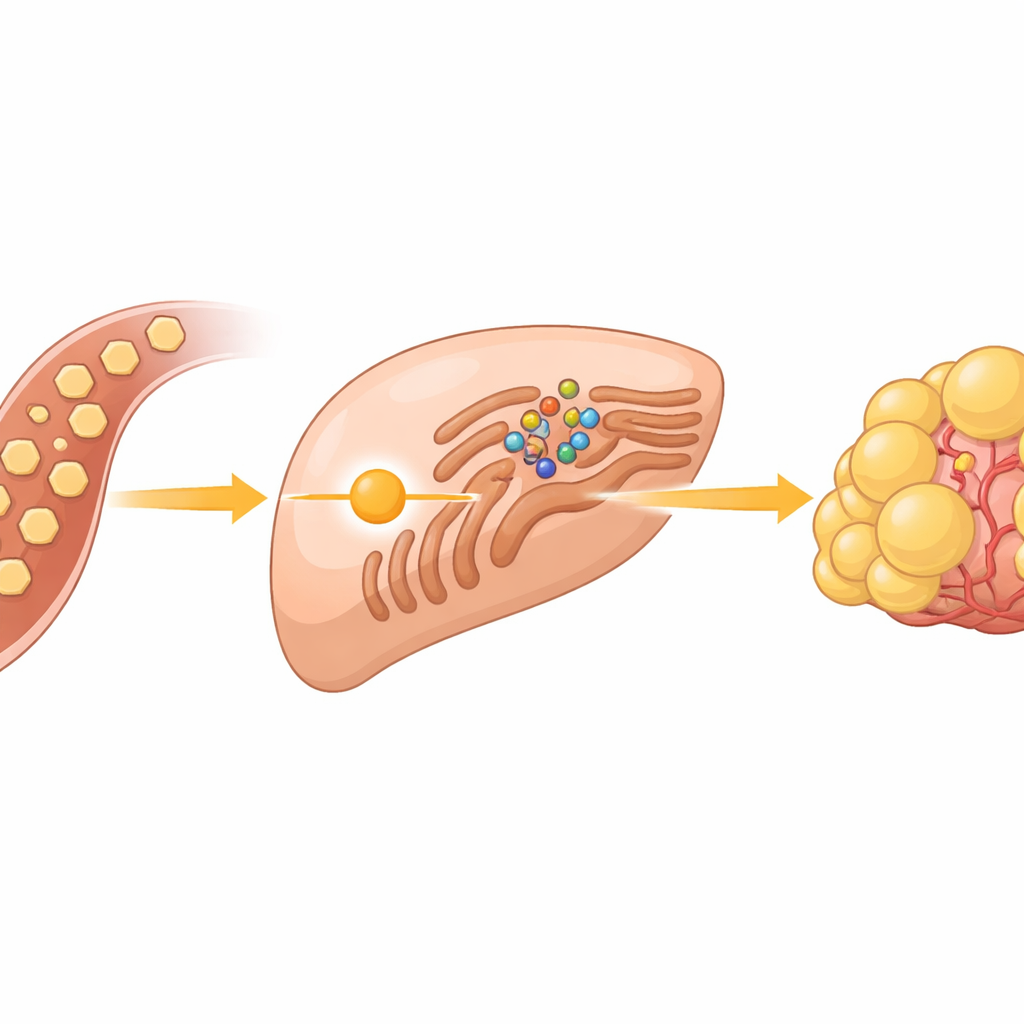
חיישן סוכר נסתר בתוך תאי הסרטן
תאי סרטן ידועים בשריפת סוכר במהירות, גם כשהחמצן בשפע — תופעה הידועה כאפקט ורבורג. בגידולי הכבד, המהירות הזו של צריכת סוכר מספקת לא רק אנרגיה; היא גם מזינה יצירת שומנים שמשמשים לבניית ממברנות חדשות. הצוות התמקד בקבוצת חלבונים הנקראת SREBPs, מתגים מרכזיים שמפעילים גנים לייצור שומנים וכולסטרול. בתנאים נורמליים, מתגים אלה מוחזקים במצב מעוכב במבנה תאי בשם רשתית תוך־תאית (endoplasmic reticulum), שם הם נעולים במקום על ידי חלבון חיישן בשם INSIG ובן־זוגו SCAP. התעלומה הגדולה הייתה כיצד גלוקוז עודף מאותת למערכת הזו לשחרר את ה־SREBPs ולהתחיל ביצירת שומן.
אנזים עם תפקיד שני
החוקרים גילו כי אנזים בשם ADSL, הידוע בעיקר בסיוע בבניית אבני־יסוד של DNA, ממלא תפקיד שני מפתיע בסרטן הכבד. כאשר רמות הגלוקוז גבוהות, הוא מפעיל את האנזים המסגתי PKCε. PKCε מוסיף תיוג זרחני ל־ADSL במיקום ספציפי, מה שדוחף את ADSL לנוע מתוך הציטוזול אל פני השטח של הרשתית התוך־תאית. שם, ADSL מתחבר באופן פיזי לחלבוני INSIG. המעבר הזה הופך את ADSL מעובד מטבולי פשוט למפעל כימי מקומי שיכול להשפיע ישירות על מתגי יצירת השומן.
צלקת כימית שמשחררת את יצירת השומן
ברגע ש‑ADSL עומד לצד INSIG, הוא מייצר מולקולה קטנה בשם פומראט כחלק מכימיה השגרתית שלו. בהקשר החדש הזה, הפומראט מגיב עם חומצת אמינו מסוימת על INSIG ויוצר "צלקת" כימית קבועה הידועה כסוקינציה. הצלקת נוצרת באתר ציסטאין מפתח (C167 ב‑INSIG1 ו‑C111 ב‑INSIG2) שלרוב מסייעת ל‑INSIG לקשור אוקסיסטרולים, מולקולות דמויות כולסטרול שמשמרות את קומפלקס SCAP–SREBP בעוגן. הסוקינציה מחלישה את אחיזת INSIG במסרים אלה וב‑SCAP, ומאפשרת לקומפלקס SCAP–SREBP לעזוב את הרשתית התוך־תאית ולהיסע אל הגולג'י. שם, SREBP נחתך והחתיכה הפעילה שלו נכנסת לגרעין, ומפעילה קבוצת גנים שמניעה ייצור שומן וכולסטרול ומזינה צמיחה מהירה של תאי סרטן.
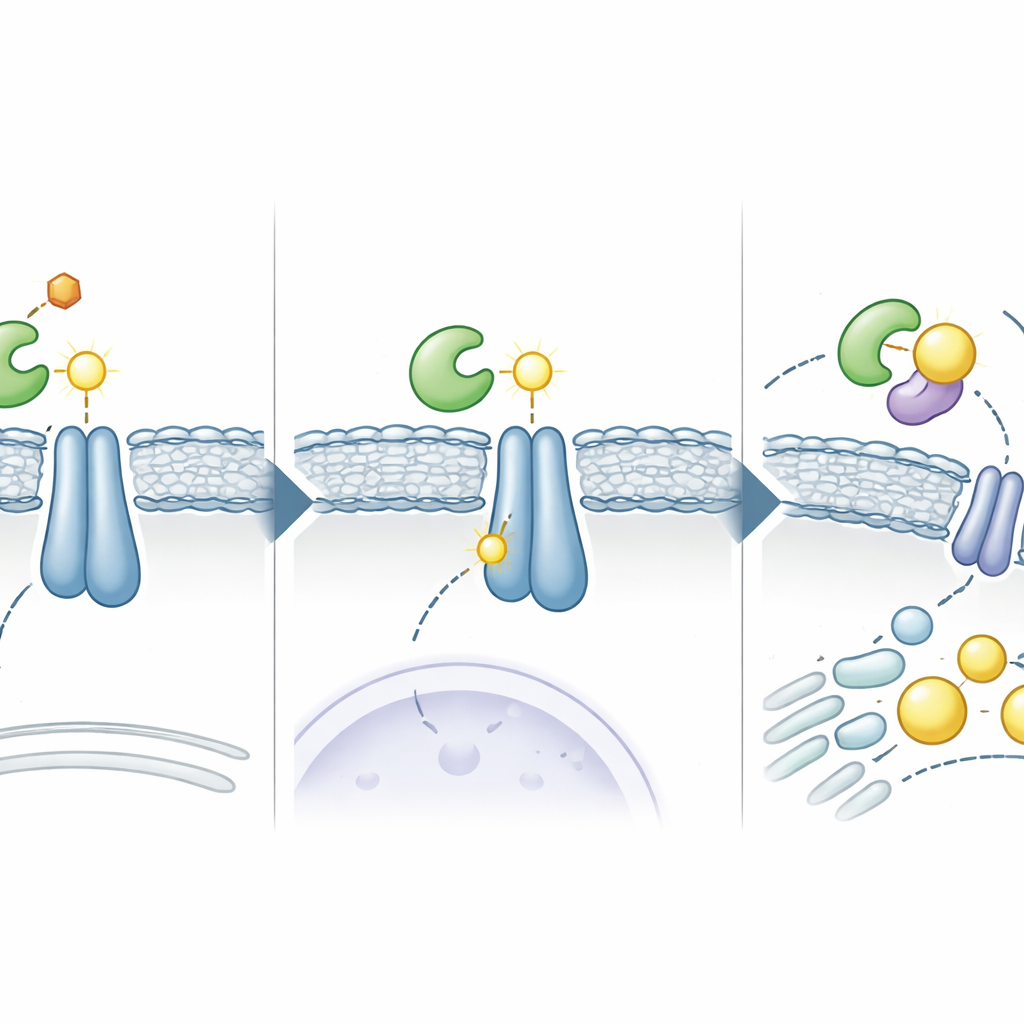
מלולאזים תאיים לשימוש חוזר בתרופות
כדי לבדוק אם אפשר להפוך את המסלול הזה נגד הסרטן, המדענים השתמשו בסריקה ממוחשבת של תרופות מאושרות כדי למצוא מולקולות שעשויות להיכנס לממשק בין ADSL ל‑INSIG. הם זיהו את Elsulfavirine, תרופה נגד HIV, כמועמד חזק. בניסויים במעבדה ובסימולציות מחשב, Elsulfavirine הפריע לקישור בין ADSL ל‑INSIG, צמצם את סוקינציית ה‑INSIG, וחסם את הפעלת SREBP בתאי סרטן של הכבד. כתוצאה מכך, התאים ייצרו פחות שומנים, הצטברו בהם פחות טיפות שומן, וצמחו לאט יותר. במודלים של עכברים עם סרטן הכבד, Elsulfavirine הקטינה גידולים, והיא עבדה אפילו טוב יותר בשילוב עם התרופה הסטנדרטית לסרטן הכבד, לנבטיניב, מה שמרמז על מהלך התקפי רב‑עוצמה הפוגע גם בסיגנלים של צמיחה וגם בדרישות המטבוליות.
מה המשמעות עבור החולים
כדי לקשר את הממצאים למחלה אמיתית, הצוות בחן דגימות גידולי כבד אנושיות. גידולים עם רמות גבוהות של ADSL מזורחן, INSIG בסוקינציה כבדה, ו‑SREBP שפעיל בגרעין היו מקושרים להישרדות ירודה יותר של המטופלים. במילים אחרות, אותו מעגל חישה של סוכר שמופיע בתאים ובעכברים נראה פעיל גם בסרטנים אגרסיביים של הכבד בבני אדם. העבודה מראה כי גידולי הכבד יכולים לחוש גלוקוז עודף ולהמיר אותו לתוכנית שומנית מקדמת‑גידול באמצעות התפקוד "המשני" של ADSL. היא גם מציינת את Elsulfavirine כמועמד מבטיח לשימוש מחדש, ופותחת אסטרטגיה פוטנציאלית לחתוך את אספקת השומנים שעליה מסתמכים גידולי הכבד כדי לשגשג.
ציטוט: Duan, Y., Wang, S., Liu, J. et al. INSIG1/2 succination mediated by the moonlighting function of ADSL promotes lipogenesis and liver tumorigenesis. Nat Commun 17, 4002 (2026). https://doi.org/10.1038/s41467-026-70583-0
מילות מפתח: סרטן הכבד, מטבוליזם של סרטן, ליפוגנזה, מסלול SREBP, שימוש מחדש בתרופות