Clear Sky Science · sv
ASO-baserad PKM-splitswitchterapi ökar effekten av anti-CTLA-4-antikropp vid pankreass ductalt adenokarcinom
Återaktivera kroppens försvar
Bukspottkörtelcancer är notorisk svårbehandlad, delvis eftersom tumörer omger sig med en fientlig omgivning som slår ner immunsvaret. Denna studie undersöker en tvådelad strategi: att omprogrammera hur tumör- och immunceller förbrukar socker, och att kombinera denna metabola omställning med ett befintligt immunterapiläkemedel. Arbetet antyder att en riktad justering av cancermetabolismen kan göra en i övrigt ”kall” tumör mer mottaglig för immunangrepp.
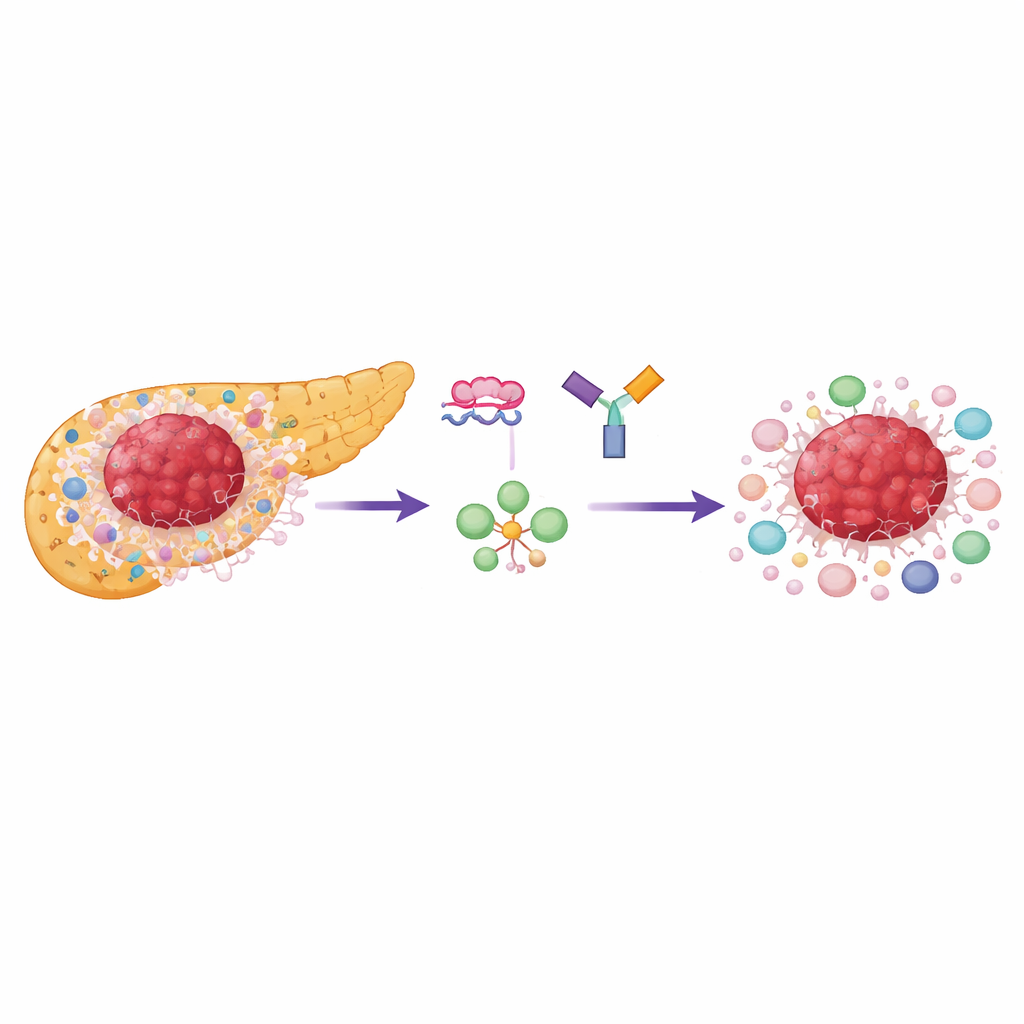
Varför pankreastumörer är så svåra
Pankreass ductalt adenokarcinom växer i en tät, ärrliknande vävnad fylld med stödjeceller och specialiserade immunceller som undertrycker angrepp, särskilt regulatoriska T‑celler (Tregs). Både cancercellerna och många av grannarna är starkt beroende av en snabbförbrännande form av sockeranvändning kallad aerob glykolys. En viktig kontrollpunkt i denna process är enzymet pyruvatkinas, som förekommer i två former: PKM1 och PKM2. De flesta normala, mogna vävnader använder PKM1, men snabbt delande celler och immunceller föredrar PKM2, vilket stöder snabb energi- och byggstensproduktion för tillväxt. Forskarna fann att PKM2 är brett uppreglerat i mänskliga pankreastumörer och kopplat till sämre överlevnad, medan PKM1 förblir låg i större delen av tumörområdena.
Omdirigera tumörens sockeranvändning med skräddarsydd DNA
Teamet använde korta, syntetiska strängar av DNA‑likt material kallade antisensoligonukleotider (ASO) för att tvinga celler att producera mer PKM1 och mindre PKM2 från samma gen. Denna ”spliceswitching” tar inte bort genen; i stället ändrar den vilken version av enzymet som produceras. I cellkultur skiftade dessa ASO effektivt pankreascancerceller mot PKM1, ökade total enzymaktivitet och minskade kraftigt mängden laktat, slutprodukten av glykolys. Basal‑liknande tumörceller — en mer aggressiv undergrupp — var särskilt känsliga och dämpade sin tillväxt mer än den så kallade klassiska undergruppen. Viktigt är att tillväxtnedgången främst berodde på minskad PKM2 snarare än enbart ökad PKM1, vilket belyser hur starkt tumörer förlitar sig på PKM2‑driven metabolism.
Kartläggning av en metabol hotspot runt tumören
För att förstå vilka celler i tumörmiljön som också kunde påverkas kombinerade forskarna vävnadsfärgning med singelcells- och rumsliga genuttryckskartor från mänskliga pankreastumörer. De observerade att många icke‑nervceller som uttryckte PKM‑genen i praktiken använde PKM2‑formen. Särskilt visade basal‑liknande cancerceller och närliggande aktiverade Tregs både högt PKM‑uttryck och starka glykolytiska signaturer. Rumslig analys avslöjade att de mest metaboliskt aktiva, hypoxiska regionerna — där cancerceller är mer basal‑liknande — var omgivna av aktiverade Tregs som är beroende av glykolys för att upprätthålla sitt suppressiva beteende. Detta nära fysiska och metaboliska partnerskap mellan tumörceller och Tregs utmärkte en särskilt immunundertryckande nisch.
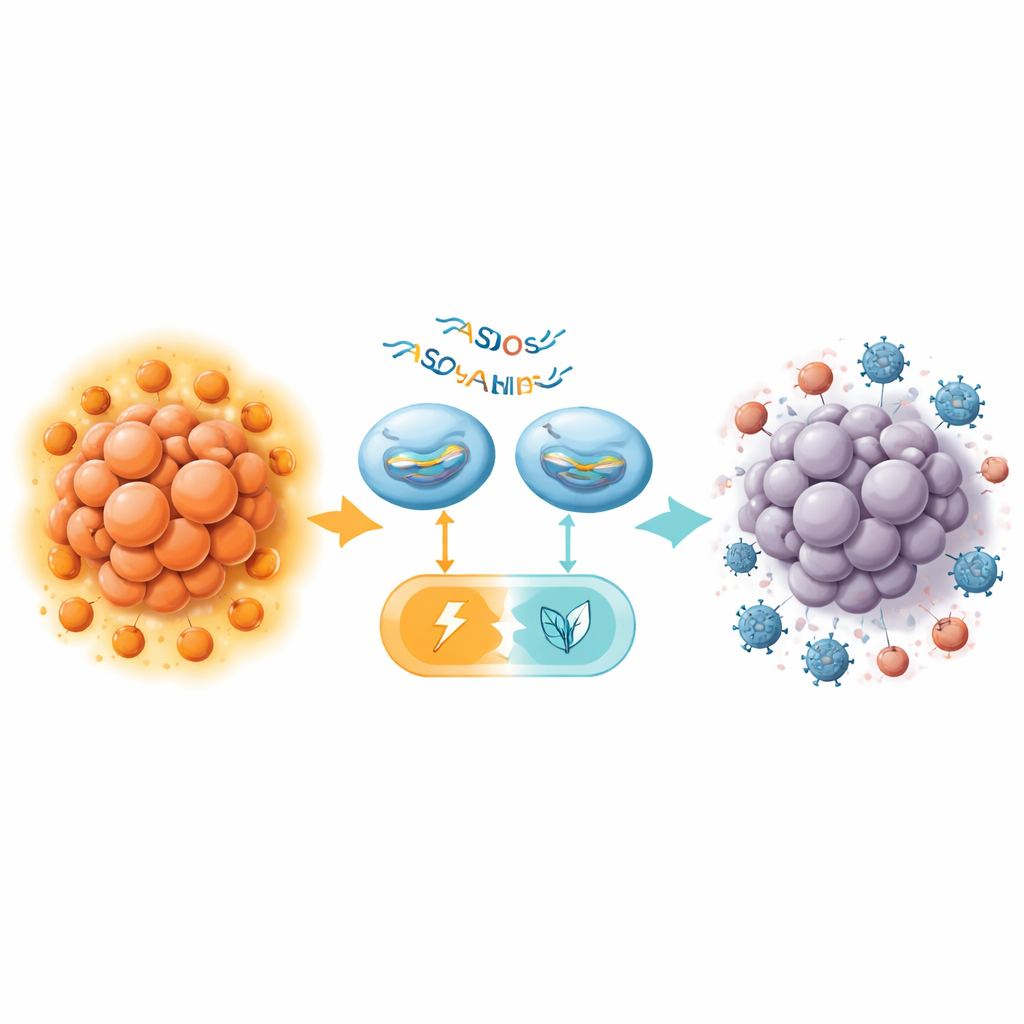
Från metabol omkoppling till starkare immunterapi
I möss utan ett fungerande immunsystem gjorde administrering av PKM splice‑switching ASO direkt i organismen att pankreastumörtillväxten saktade ner, ökade tumörcelldöd och minskade glykolys, allt utan uppenbar toxicitet i känsliga organ som lever och njurar. Effekten var dock måttlig jämfört med tidigare resultat i levercancer. Det avgörande framsteget kom i immunokompetenta möss, där teamet kombinerade en potent mus‑ASO (MOE16) med en anti‑CTLA‑4‑antikropp, ett checkpointsblockerande läkemedel riktat mot Tregs. På egen hand hade anti‑CTLA‑4 liten effekt på pankreastumörer, i linje med besvikna kliniska prövningar. ASO‑behandling ensam gav endast en marginell nytta. Tillsammans krympte dock de två behandlingarna tumörer mycket effektivare, ibland så att bara små rester återstod vid inspektion.
Göra en ”kall” tumör mer mottaglig
Närmare granskning av behandlade musstumörer visade att PKM splice‑switching förändrade enzymnivåerna både i cancerceller och CD4‑positiva T‑celler, minskade antalet infiltrerande Tregs och omformade den lokala metabolismen. Genom att lätta tumörens beroende av PKM2‑driven glykolys och försvaga de omgivande Tregs verkade ASO‑behandlingen göra tumörmikromiljön mindre undertryckande och mer gynnsam för immunangrepp. Medan ytterligare arbete behövs i långsammare, mer realistiska modeller och i vävnader härledda från människa, tyder dessa fynd på att en precis inriktning mot en enda metabolisk omkopplare kan förvandla en resistent pankreastumör till en som slutligen svarar på immunterapi.
Citering: Han, L., Gan, L., Schäfer, B. et al. ASO-based PKM splice-switching therapy increases anti-CTLA-4 antibody efficacy in pancreatic ductal adenocarcinoma. Cell Discov 12, 28 (2026). https://doi.org/10.1038/s41421-026-00882-9
Nyckelord: bukspottkörtelcancer, tumörmetabolism, immunterapi, regulatoriska T‑celler, antisensoligonukleotider