Clear Sky Science · ja
ASOを用いたPKMスプライス切替療法は膵管腺癌における抗CTLA-4抗体の有効性を高める
体の防御を再稼働させる
膵臓がんは治療が極めて難しいことで知られており、その一因は腫瘍が免疫系を遮断する抑圧的な微小環境に身を包むことです。本研究は二方向の戦略を探ります:腫瘍および免疫細胞の糖代謝を書き換えることと、既存の免疫療法薬とその代謝のリセットを組み合わせることです。この研究は、がんの代謝を注意深く標的化することで、本来「寒冷」な腫瘍を免疫攻撃に対してより応答性の高いものにできる可能性を示唆しています。
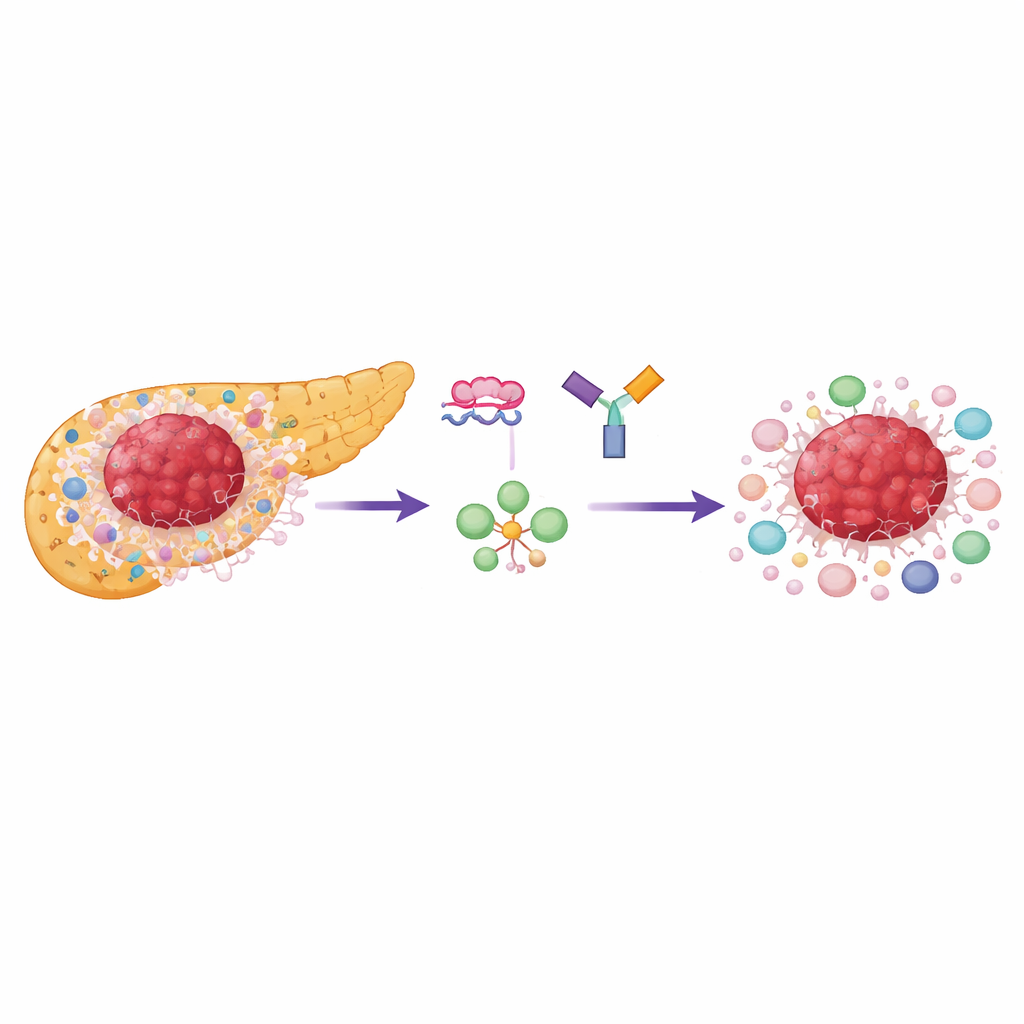
なぜ膵臓腫瘍は手強いのか
膵管腺癌は、支持細胞や攻撃を抑える特殊な免疫細胞、特に制御性T細胞(Treg)に満ちた濃密で瘢痕のような組織内で増殖します。がん細胞と多くの周辺細胞は、好気性解糖と呼ばれる速やかに糖を燃やす様式に強く依存しています。この過程の重要な制御点はピルビン酸キナーゼという酵素で、PKM1とPKM2という二つのアイソフォームが存在します。正常で成熟した多くの組織はPKM1を用いる一方で、急速に分裂する細胞や免疫細胞はPKM2を好み、迅速なエネルギー供給と成長のためのビルディングブロックを支えます。研究者らは、ヒトの膵臓腫瘍でPKM2が広く上昇し生存率低下と関連している一方、PKM1はほとんどの腫瘍領域で低いままであることを見出しました。
設計されたDNAで腫瘍の糖利用を書き換える
研究チームはアンチセンスオリゴヌクレオチド(ASO)と呼ばれる短い合成のDNA様分子を用い、同じ遺伝子からより多くのPKM1を、より少ないPKM2を産生するように細胞を強制しました。この「スプライス切替」は遺伝子を消失させるのではなく、どのアイソフォームの酵素が産生されるかを変えます。細胞培養では、これらのASOは膵臓がん細胞を効果的にPKM1側へシフトさせ、全体の酵素活性を高め、解糖系の最終産物である乳酸を大幅に減少させました。より攻撃的なサブタイプであるベーサル様(basal-like)腫瘍細胞は特に感受性が高く、いわゆるクラシカル型よりも増殖がより強く抑制されました。重要な点は、増殖の鈍化が主にPKM2の減少に依存しており、単にPKM1を増やすだけでは説明できないことから、腫瘍がPKM2駆動の代謝プログラムに強く依存していることが示された点です。
腫瘍周辺における代謝ホットスポットの地図化
腫瘍の近傍でどの細胞が影響を受けうるかを理解するため、研究者らは組織染色を単一細胞および空間遺伝子発現マップと組み合わせてヒト膵臓がんを解析しました。多くの非神経細胞がPKM遺伝子を発現しているものの、実際にはPKM2形を使用していることが観察されました。特にベーサル様がん細胞と近傍の活性化されたTregは高いPKM発現と強い解糖署名を示しました。空間解析により、最も代謝的に活性で低酸素な領域—ここではがん細胞がよりベーサル様である—が、解糖に依存して抑制機能を維持する活性化Tregによって取り囲まれていることが明らかになりました。この腫瘍細胞とTregの密接な物理的かつ代謝的な共生関係は、特に免疫抑制的なニッチを特徴づけていました。
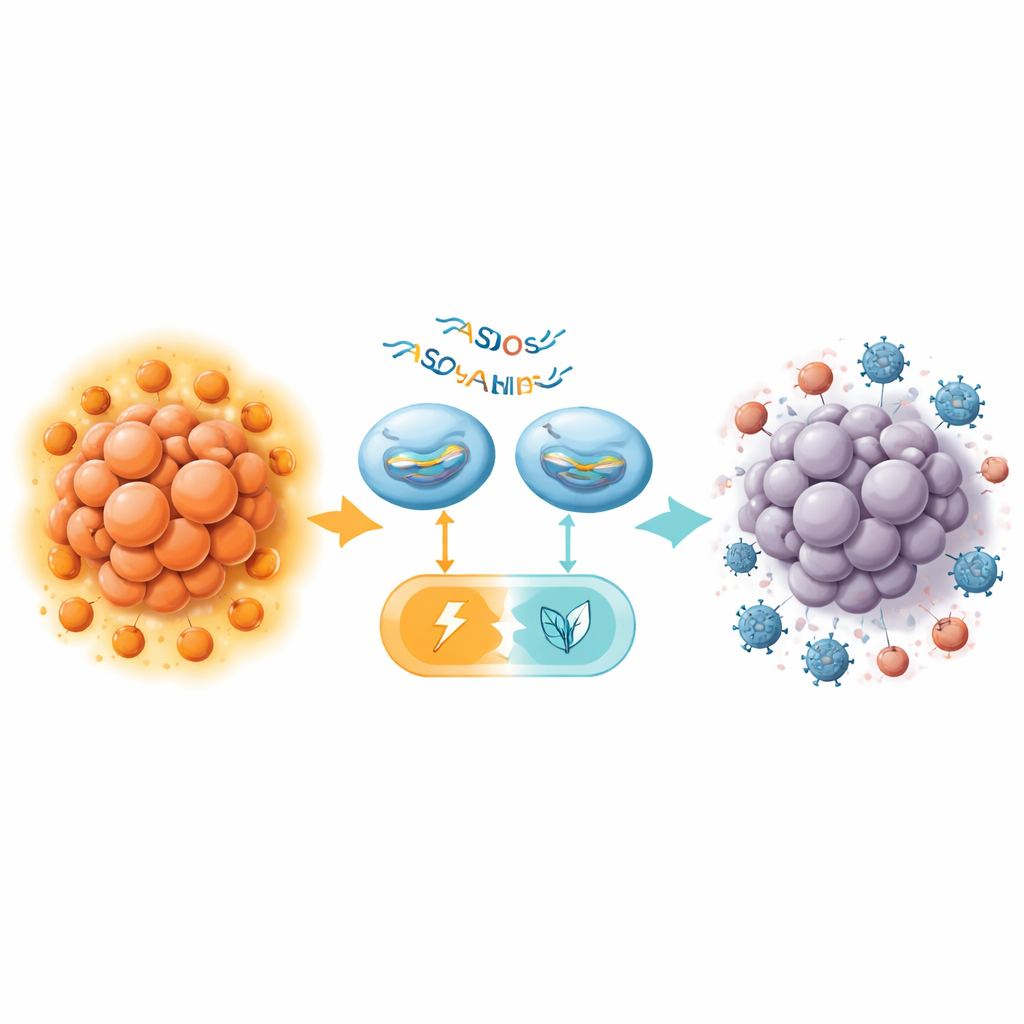
代謝スイッチから強化された免疫療法へ
免疫系が機能しないマウスでは、PKMスプライス切替ASOを体内に投与すると膵臓腫瘍の成長が遅延し、腫瘍細胞死が増加し、解糖が低下しましたが、肝臓や腎臓などの感受性の高い臓器に明らかな毒性は認められませんでした。ただし、その効果は肝がんでの以前の結果に比べると控えめでした。重要な進展は免疫が正常に働くマウスで得られ、ここでは強力なマウス用ASO(MOE16)と制御性T細胞を標的とするチェックポイント阻害薬である抗CTLA-4抗体を組み合わせました。単独では抗CTLA-4は膵臓腫瘍にほとんど影響を与えず、臨床試験での失望を再現しました。ASO単独でもわずかな利益しか示しませんでした。しかし両者を組み合わせると腫瘍ははるかに効果的に縮小し、検査時にごく小さな残存のみを残すことがありました。
「寒冷」な腫瘍をより応答性の高いものへ
処理を受けたマウス腫瘍を詳しく調べると、PKMのスプライス切替ががん細胞とCD4陽性T細胞の両方の酵素レベルを変化させ、浸潤するTregの数を減少させ、局所代謝を再構築していることが示されました。PKM2駆動の解糖への腫瘍の依存を緩和し、周囲のTregを弱めることで、ASO治療は腫瘍微小環境を抑制的でなく、免疫攻撃により寛容なものに変えているように見えます。より遅い、より現実的なモデルやヒト由来組織での追加検証が必要ですが、これらの知見は単一の代謝スイッチを精密に標的化することで、抵抗性の膵臓腫瘍をついに免疫療法に応答させうることを示唆しています。
引用: Han, L., Gan, L., Schäfer, B. et al. ASO-based PKM splice-switching therapy increases anti-CTLA-4 antibody efficacy in pancreatic ductal adenocarcinoma. Cell Discov 12, 28 (2026). https://doi.org/10.1038/s41421-026-00882-9
キーワード: 膵臓がん, 腫瘍代謝, 免疫療法, 制御性T細胞, アンチセンスオリゴヌクレオチド