Clear Sky Science · ar
العلاج القائم على تغيير الطي بدلالة ASO في PKM يزيد فاعلية الأجسام المضادة المضادة لـ CTLA-4 في سرطان القناة البنكرياسية
إعادة تشغيل دفاعات الجسم
يُعرف سرطان البنكرياس بصعوبة علاجه، جزئياً لأن الأورام تغطي نفسها ببيئة معادية تُثبِط الجهاز المناعي. تستكشف هذه الدراسة استراتيجية ذات شقين: إعادة توصيل طريقة استخدام الورم والخلايا المناعية للسكر، ودمج هذا إعادة الضبط الأيضي مع دواء مناعي موجود. تشير النتائج إلى أن استهداف استقلاب السرطان بدقة يمكن أن يجعل الورم البارد قابلًا أكثر للهجوم المناعي.
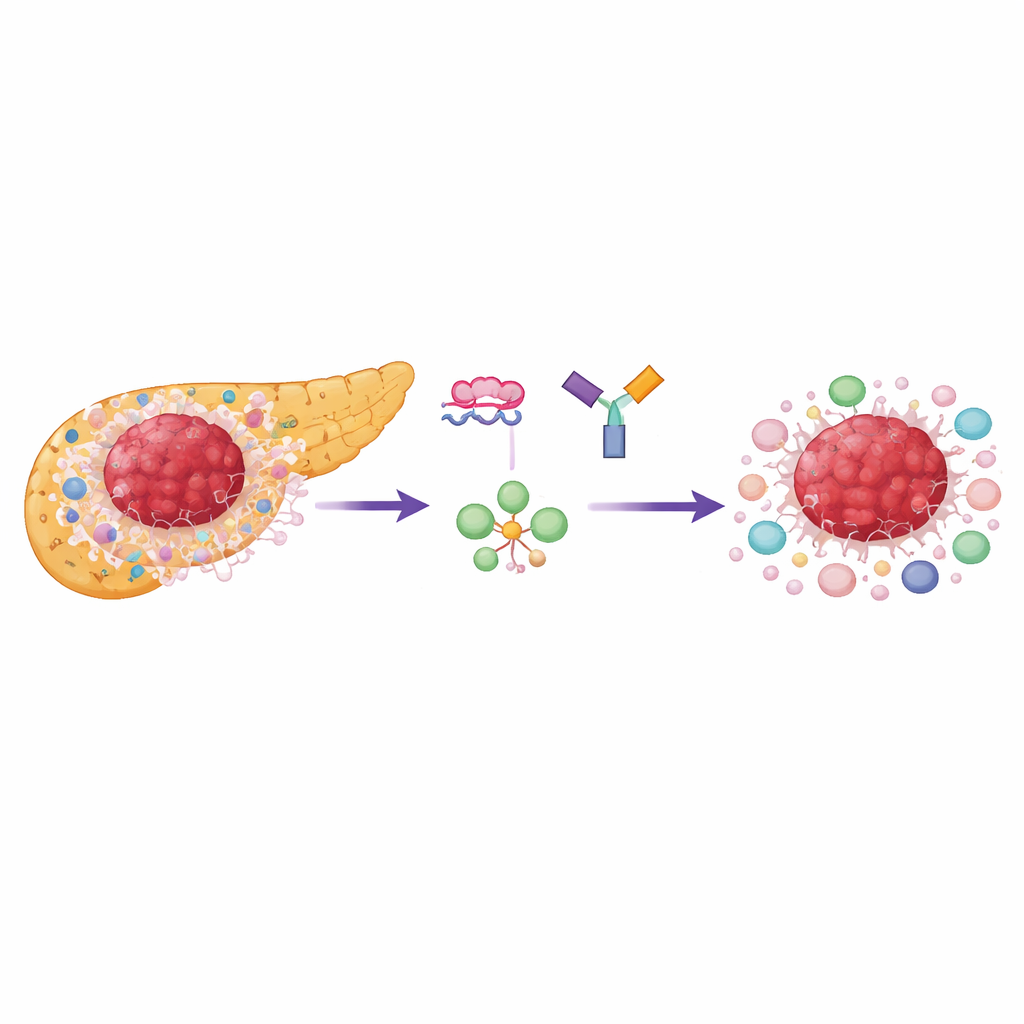
لماذا أورام البنكرياس صعبة جدًا
ينمو سرطان غدد القناة البنكرياسية داخل نسيج كثيف يشبه الندبة ومليء بخلايا داعمة وخلايا مناعية متخصصة تُكبِّح الهجوم، لا سيما الخلايا التائية المنظمة (Tregs). تعتمد كل من خلايا السرطان والعديد من الخلايا المجاورة بشكل كبير على شكل سريع الاحتراق من استخدام السكر يسمى التحلل السكري الهوائي. نقطة تحكم رئيسية في هذه العملية هي إنزيم يُدعى بيروفات كيناز، الذي يوجد في شكلين: PKM1 وPKM2. تستخدم معظم الأنسجة الناضجة الطبيعية PKM1، بينما تفضل الخلايا سريعة الانقسام والخلايا المناعية PKM2، الذي يدعم طاقة سريعة ومقومات للبناء والنمو. وجد الباحثون أن PKM2 مرتفع على نطاق واسع في أورام البنكرياس البشرية ومرتبط ببقاء أسوأ، بينما يظل PKM1 منخفضًا في معظم مناطق الورم.
إعادة توصيل استخدام الورم للسكر بواسطة DNA مصمم
استخدم الفريق سلاسل قصيرة اصطناعية تشبه DNA تُسمى أوليجونيوكليوتيدات مضادة للتعاقب (ASOs) لإجبار الخلايا على صنع المزيد من PKM1 وأقل من PKM2 من نفس الجين. هذا "تبديل الطي" لا يزيل الجين؛ بل يغير أي نسخة من الإنزيم تُنتَج. في زرع الخلايا، حوّلت هذه الـ ASOs خلايا سرطان البنكرياس نحو PKM1 بفعالية، وزادت النشاط الإنزيمي الكلّي، وخفّضت بشكل حاد اللاكتات، منتج التحلل السكري النهائي. كانت خلايا الأورام من النوع القاعدي (basal-like)—وهي نوع أكثر عدوانية—شديدة الحساسية بشكل خاص، إذ تباطأ نموها أكثر من النمط المسمى الكلاسيكي. ومن المهم أن تباطؤ النمو اعتمد أساسًا على تقليل PKM2 لا على مجرد زيادة PKM1، مما يبرز مدى اعتماد الأورام على البرنامج الأيضي المدفوع بـ PKM2.
رسم خريطة بؤرة أيضية حول الورم
لفهم أي الخلايا في بيئة الورم قد تتأثر أيضًا، جمع الباحثون صبغات نسيجية مع خرائط التعبير الجيني الخلوي المفرد والمكاني من سرطانات البنكرياس البشرية. لاحظوا أن العديد من الخلايا غير العصبية التي تُعبِّر عن جين PKM كانت عمليًا تستخدم شكل PKM2. على الخصوص، أظهرت خلايا الأورام القاعدية والخلايا التائية المنظمة المُنشطة المجاورة تعبيرًا عاليًا عن PKM وبصمات أيضية جليكوليتية قوية. كشفت التحليلات المكانية أن أكثر المناطق نشاطًا أيضيًا وحرمانًا من الأكسجين—حيث تميل خلايا السرطان لأن تكون أكثر قاعدية—كانت محاطة بخلايا Tregs المنشط التي تعتمد على التحلل السكري للحفاظ على سلوكها الكابح. مثل هذه الشراكة الفيزيائية والتمثيلية الأيضية الوثيقة بين خلايا الورم وTregs ميَّزت نطاقًا ذي كبت مناعي خاص.
من تبديل أيضي إلى تقوية العلاج المناعي
في فئران تفتقر إلى جهاز مناعي وظيفي، أدى إيصال ASOs المبدلة لطي PKM مباشرةً إلى إبطاء نمو أورام البنكرياس، وزيادة موت خلايا الورم، وخفض التحلل السكري، كل ذلك دون سمية ظاهرة في أعضاء حساسة مثل الكبد والكلى. ومع ذلك، كان التأثير متواضعًا مقارنةً بالنتائج السابقة في سرطان الكبد. جاء التقدم الرئيسي في الفئران المتمتعة بمناعة سليمة، حيث جمع الفريق بين ASO فئري قوي (MOE16) وجسم مضاد مضاد لـ CTLA-4، وهو دواء يوقف نقاط التفتيش موجه ضد Tregs. بمفرده، كان للأجسام المضادة المضادة لـ CTLA-4 تأثير ضئيل على أورام البنكرياس، مكررة خيبة الآمال في التجارب السريرية. أنتجت معالجة الـ ASO وحدها فائدة طفيفة فقط. معًا، مع ذلك، قلّص العلاجان حجم الأورام بفاعلية أكبر بكثير، أحيانًا تاركين بقايا صغيرة فقط عند الفحص.
جعل الورم "البارد" أكثر استجابة
أظهر الفحص الأدق لأورام الفئران المعالجة أن تبديل طي PKM غيّر مستويات الإنزيم داخل كل من خلايا السرطان والخلايا التائية الموجبة لـ CD4، وقلّل عدد Tregs المتسللة، وأعاد تشكيل الأيض المحلي. من خلال تخفيف اعتماد الورم على التحلل السكري المدفوع بـ PKM2 وإضعاف Tregs المحيطة، بدا أن معالجة ASO تجعل بيئة الورم أقل قمعية وأكثر سماحًا بالهجوم المناعي. بينما هناك حاجة لمزيد من العمل في نماذج أبطأ وأكثر واقعية وأنسجة مشتقة من الإنسان، تشير هذه النتائج إلى أن استهداف مفتاح أيضي واحد بدقة يمكن أن يحوّل ورم بنكرياس مقاومًا إلى ورم يستجيب أخيرًا للعلاج المناعي.
الاستشهاد: Han, L., Gan, L., Schäfer, B. et al. ASO-based PKM splice-switching therapy increases anti-CTLA-4 antibody efficacy in pancreatic ductal adenocarcinoma. Cell Discov 12, 28 (2026). https://doi.org/10.1038/s41421-026-00882-9
الكلمات المفتاحية: سرطان البنكرياس, استقلاب الورم, العلاج المناعي, الخلايا التائية المنظمة, أُحماض نووية مضادة للتعاقب (أوليجونيوكليوتيدات مضادة)