Clear Sky Science · es
Terapia de conmutación de empalme de PKM basada en ASO aumenta la eficacia del anticuerpo anti-CTLA-4 en adenocarcinoma ductal pancreático
Volver a activar las defensas del cuerpo
El cáncer de páncreas es notoriamente difícil de tratar, en parte porque los tumores se cubren con un entorno hostil que apaga el sistema inmune. Este estudio explora una estrategia de dos frentes: reconectar la forma en que las células tumorales e inmunitarias consumen azúcar y combinar ese restablecimiento metabólico con un fármaco de inmunoterapia ya existente. El trabajo sugiere que dirigirse con precisión al metabolismo del cáncer puede convertir un tumor “frío” en uno más receptivo al ataque inmunitario.
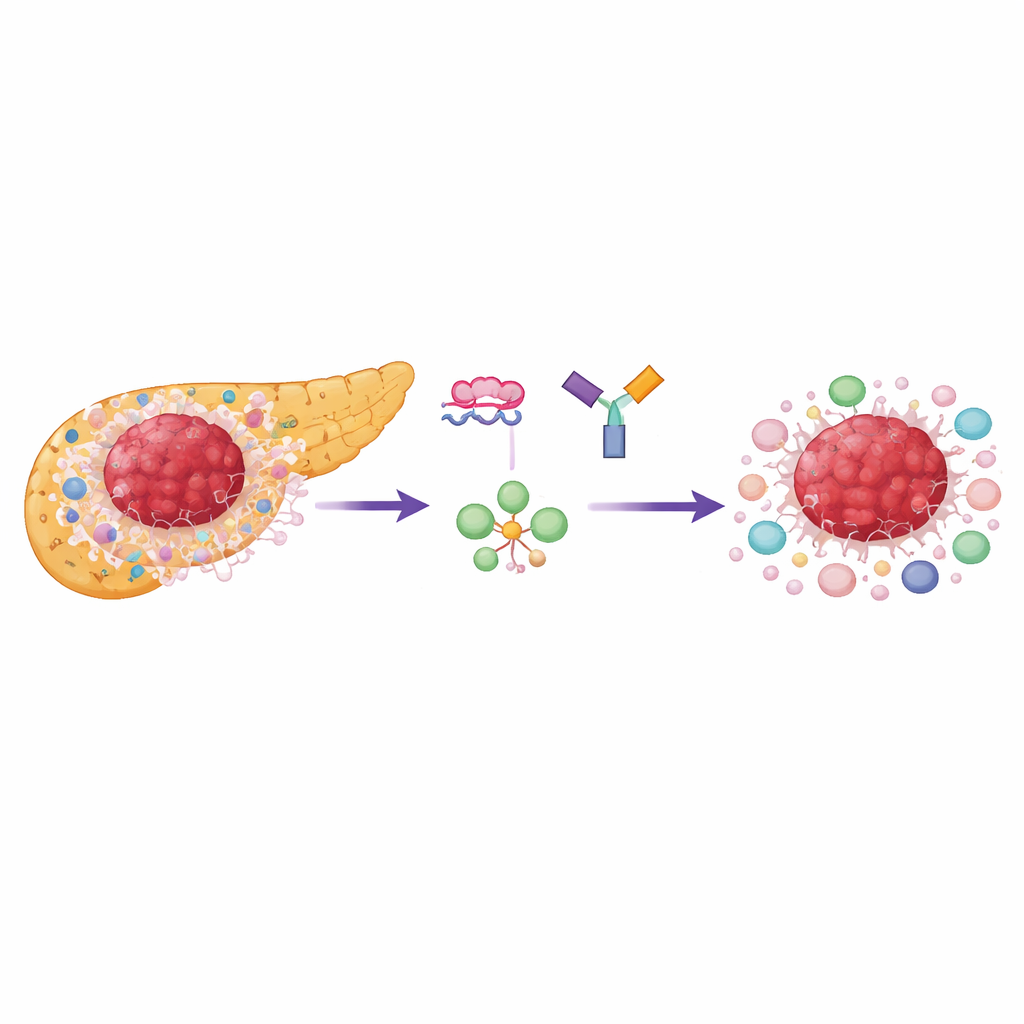
Por qué los tumores pancreáticos son tan resistentes
El adenocarcinoma ductal pancreático crece dentro de un tejido denso, parecido a una cicatriz, repleto de células de soporte y células inmunitarias especializadas que suprimen el ataque, especialmente las células T reguladoras (Tregs). Tanto las células cancerosas como muchos vecinos dependen en gran medida de una forma de uso de azúcar de combustión rápida llamada glucólisis aeróbica. Un punto de control clave en este proceso es una enzima llamada piruvato quinasa, que existe en dos formas: PKM1 y PKM2. La mayoría de los tejidos normales y maduros usan PKM1, pero las células que se dividen rápidamente y las células inmunitarias favorecen PKM2, que soporta energía rápida y sustratos para el crecimiento. Los investigadores encontraron que PKM2 está ampliamente elevada en tumores pancreáticos humanos y se asocia con peor supervivencia, mientras que PKM1 permanece baja en la mayoría de las áreas tumorales.
Reconectar el uso de azúcar del tumor con ADN diseñado
El equipo utilizó hebras cortas y sintéticas de material similar al ADN llamadas oligonucleótidos antisentido (ASO) para obligar a las células a producir más PKM1 y menos PKM2 a partir del mismo gen. Este “cambio de empalme” no elimina el gen; en cambio, altera qué versión de la enzima se produce. En cultivo celular, estos ASO desplazaron eficazmente a las células de cáncer pancreático hacia PKM1, aumentaron la actividad enzimática total y redujeron drásticamente el lactato, producto final de la glucólisis. Las células tumorales de tipo basal, un subtipo más agresivo, fueron especialmente sensibles, reduciendo su crecimiento más que el llamado subtipo clásico. Es importante destacar que la desaceleración del crecimiento dependió principalmente de la reducción de PKM2 en lugar de solo el aumento de PKM1, lo que subraya la fuerte dependencia de los tumores en el programa metabólico impulsado por PKM2.
Mapear un punto caliente metabólico alrededor del tumor
Para entender qué células en el vecindario tumoral también podrían verse afectadas, los investigadores combinaron tinciones tisulares con mapas de expresión génica espacial y de una sola célula procedentes de cánceres pancreáticos humanos. Observaron que muchas células no neuronales que expresaban el gen PKM, en la práctica, estaban usando la forma PKM2. En particular, las células cancerosas de tipo basal y las Tregs activadas cercanas mostraron alta expresión de PKM y fuertes firmas glucolíticas. El análisis espacial reveló que las regiones más metabólicamente activas e hipóxicas—donde las células cancerosas son más de tipo basal—estaban rodeadas por Tregs activadas que dependen de la glucólisis para mantener su comportamiento supresor. Esta estrecha asociación física y metabólica entre las células tumorales y las Tregs marcó un nicho especialmente inmunosupresor.
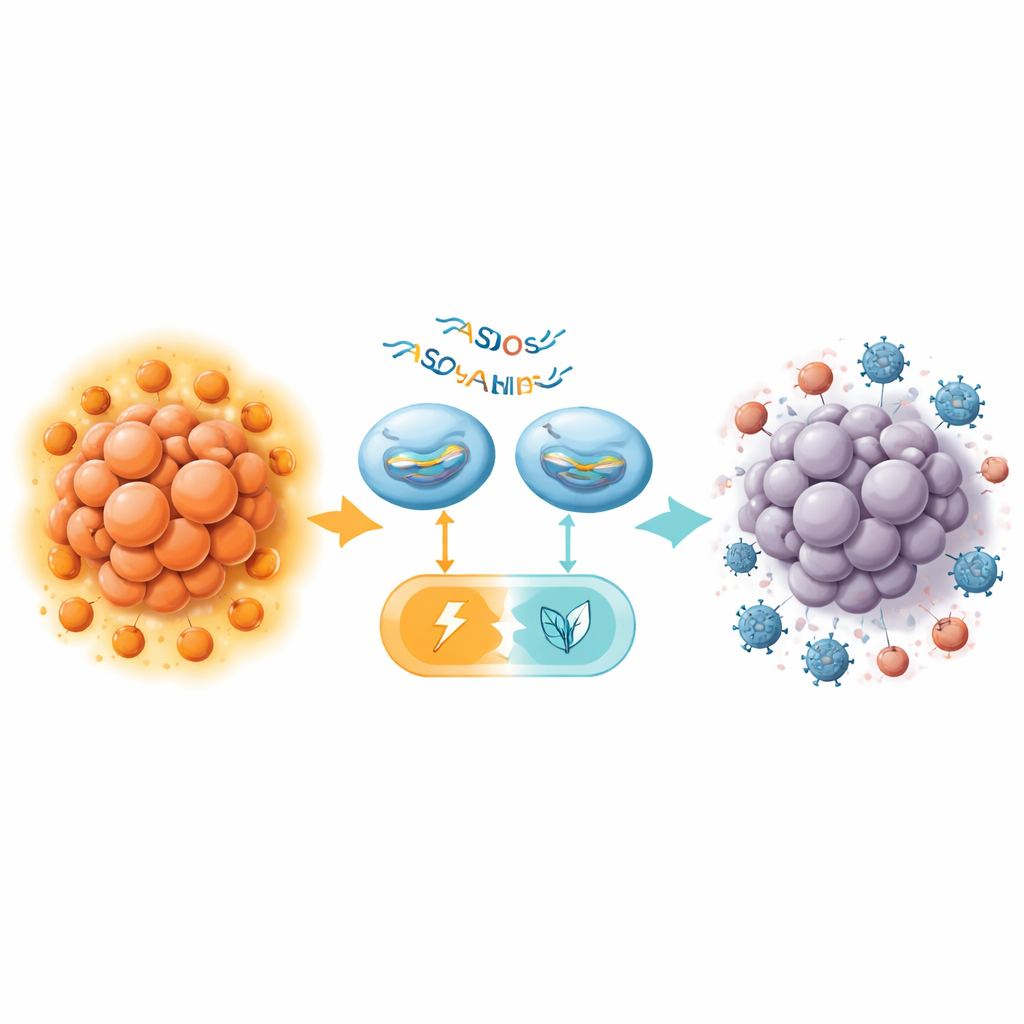
Del cambio metabólico a una inmunoterapia más potente
En ratones carentes de un sistema inmune funcional, la administración de ASO para el cambio de empalme de PKM directamente en el organismo ralentizó el crecimiento tumoral pancreático, aumentó la muerte de células tumorales y redujo la glucólisis, todo ello sin toxicidad aparente en órganos sensibles como hígado y riñón. Sin embargo, el efecto fue modesto en comparación con resultados previos en cáncer de hígado. El avance clave llegó en ratones inmunocompetentes, donde el equipo combinó un ASO potente para ratón (MOE16) con un anticuerpo anti-CTLA-4, un fármaco inhibidor de puntos de control dirigido a las Tregs. Por sí solo, el anti-CTLA-4 tuvo poco impacto en los tumores pancreáticos, en consonancia con ensayos clínicos decepcionantes. El tratamiento con ASO únicamente produjo solo un beneficio leve. Sin embargo, juntos, ambos tratamientos redujeron los tumores de forma mucho más efectiva, a veces dejando solo pequeños restos a la inspección.
Hacer que un tumor “frío” sea más sensible
Un examen más detallado de los tumores de ratón tratados mostró que el cambio de empalme de PKM modificó los niveles de la enzima tanto en las células cancerosas como en las células T CD4 positivas, redujo el número de Tregs infiltrantes y remodeló el metabolismo local. Al aliviar la dependencia del tumor de la glucólisis impulsada por PKM2 y debilitar las Tregs circundantes, el tratamiento con ASO pareció hacer que el microambiente tumoral fuera menos supresor y más permisivo al ataque inmune. Aunque se necesitan más estudios en modelos más lentos y realistas y en tejidos humanos, estos hallazgos sugieren que dirigir con precisión un único interruptor metabólico puede convertir un tumor pancreático resistente en uno que finalmente responde a la inmunoterapia.
Cita: Han, L., Gan, L., Schäfer, B. et al. ASO-based PKM splice-switching therapy increases anti-CTLA-4 antibody efficacy in pancreatic ductal adenocarcinoma. Cell Discov 12, 28 (2026). https://doi.org/10.1038/s41421-026-00882-9
Palabras clave: cáncer de páncreas, metabolismo tumoral, inmunoterapia, células T reguladoras, oligonucleótidos antisentido