Clear Sky Science · de
ASO-basierte PKM-Spleißumschalttherapie erhöht die Wirksamkeit von Anti-CTLA-4-Antikörpern beim duktalen Adenokarzinom der Bauchspeicheldrüse
Das Immunsystem wieder anschalten
Bauchspeicheldrüsenkrebs ist notorisch schwer zu behandeln, unter anderem weil Tumoren sich in einer feindseligen Umgebung verstecken, die das Immunsystem lahmlegt. Diese Studie untersucht eine zweigleisige Strategie: das Umbiegen des Zuckerstoffwechsels von Tumor- und Immunzellen und die Kombination dieses metabolischen Resets mit einem bereits verfügbaren Immuntherapeutikum. Die Arbeit legt nahe, dass eine gezielte Beeinflussung des Krebsstoffwechsels einen ansonsten „kalten“ Tumor empfindlicher für einen Immunangriff machen kann.
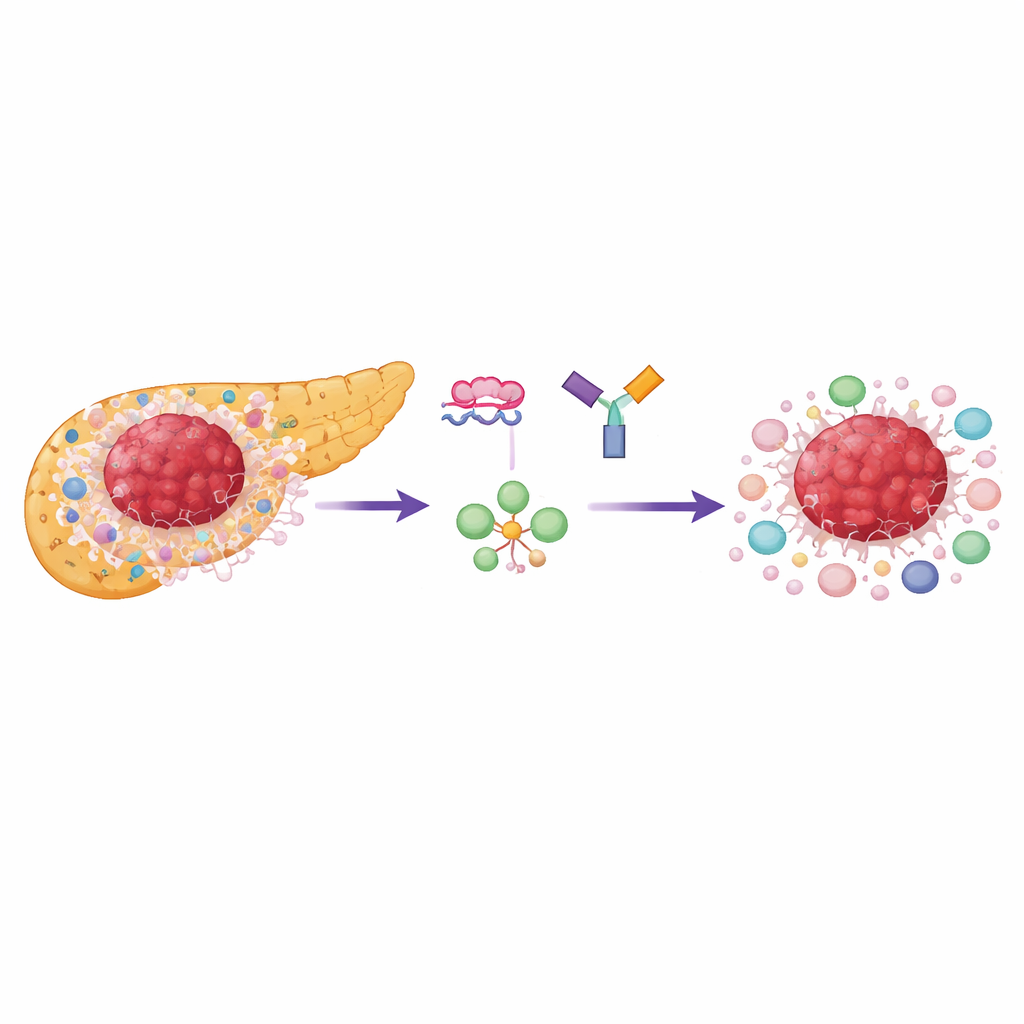
Warum Bauchspeicheldrüsentumoren so widerstandsfähig sind
Das duktale Adenokarzinom der Bauchspeicheldrüse wächst in dichtem, narbenähnlichem Gewebe, das mit Stütz- und spezialisierten Immunzellen gefüllt ist, die Angriffe unterdrücken, insbesondere regulatorische T-Zellen (Tregs). Sowohl die Krebszellen als auch viele Nachbarzellen sind stark abhängig von einer schnell ablaufenden Form des Zuckerverbrauchs, der sogenannten aeroben Glykolyse. Ein zentraler Kontrollpunkt in diesem Prozess ist das Enzym Pyruvatkinase, das in zwei Formen vorkommt: PKM1 und PKM2. Die meisten normalen, ausgereiften Gewebe nutzen PKM1, während schnell teilende Zellen und Immunzellen PKM2 bevorzugen, das schnelle Energie und Bausteine für Wachstum bereitstellt. Die Forschenden fanden, dass PKM2 in menschlichen Pankreastumoren weit verbreitet erhöht ist und mit schlechterem Überleben verknüpft ist, während PKM1 in den meisten Tumorbereichen niedrig bleibt.
Den Tumorzucker mit maßgeschneiderter DNA umprogrammieren
Das Team verwendete kurze, synthetische, DNA-ähnliche Stränge, sogenannte Antisense-Oligonukleotide (ASOs), um Zellen dazu zu bringen, von demselben Gen mehr PKM1 und weniger PKM2 herzustellen. Dieses „Spleißumschalten“ entfernt das Gen nicht; es ändert vielmehr, welche Isoform des Enzyms produziert wird. In Zellkulturen verschoben diese ASOs die pankreatischen Krebszellen effektiv hin zu PKM1, erhöhten die Gesamt-Enzymaktivität und verringerten deutlich Lactat, das Endprodukt der Glykolyse. Basal-ähnliche Tumorzellen — ein aggressiveres Subtyp — waren besonders empfindlich und bremsten ihr Wachstum stärker als der sogenannte klassische Subtyp. Wichtig ist, dass die Wachstumsverlangsamung vor allem von der Reduktion von PKM2 und nicht allein von der Erhöhung von PKM1 abhing, was hervorhebt, wie sehr Tumoren auf das PKM2-getriebene Stoffwechselprogramm angewiesen sind.
Kartierung eines metabolischen Hotspots rund um den Tumor
Um zu verstehen, welche Zellen in der Tumornachbarschaft ebenfalls betroffen sein könnten, kombinierten die Forschenden Gewebefärbungen mit Einzelzell- und räumlichen Genexpressionskarten aus menschlichen Pankreaskarzinomen. Sie beobachteten, dass viele Nicht-Nerven-Zellen, die das PKM-Gen exprimierten, in der Praxis die PKM2-Form verwendeten. Insbesondere basal-ähnliche Krebszellen und nahegelegene aktivierte Tregs zeigten sowohl hohe PKM-Expression als auch starke glykolytische Signaturen. Die räumliche Analyse zeigte, dass die stoffwechselaktivsten, hypoxischen Regionen — in denen Krebszellen eher basal-ähnlich sind — von aktivierten Tregs umgeben waren, die zur Aufrechterhaltung ihres suppressiven Verhaltens auf die Glykolyse angewiesen sind. Diese enge physische und metabolische Partnerschaft zwischen Tumorzellen und Tregs kennzeichnete eine besonders immunsuppressive Nische.
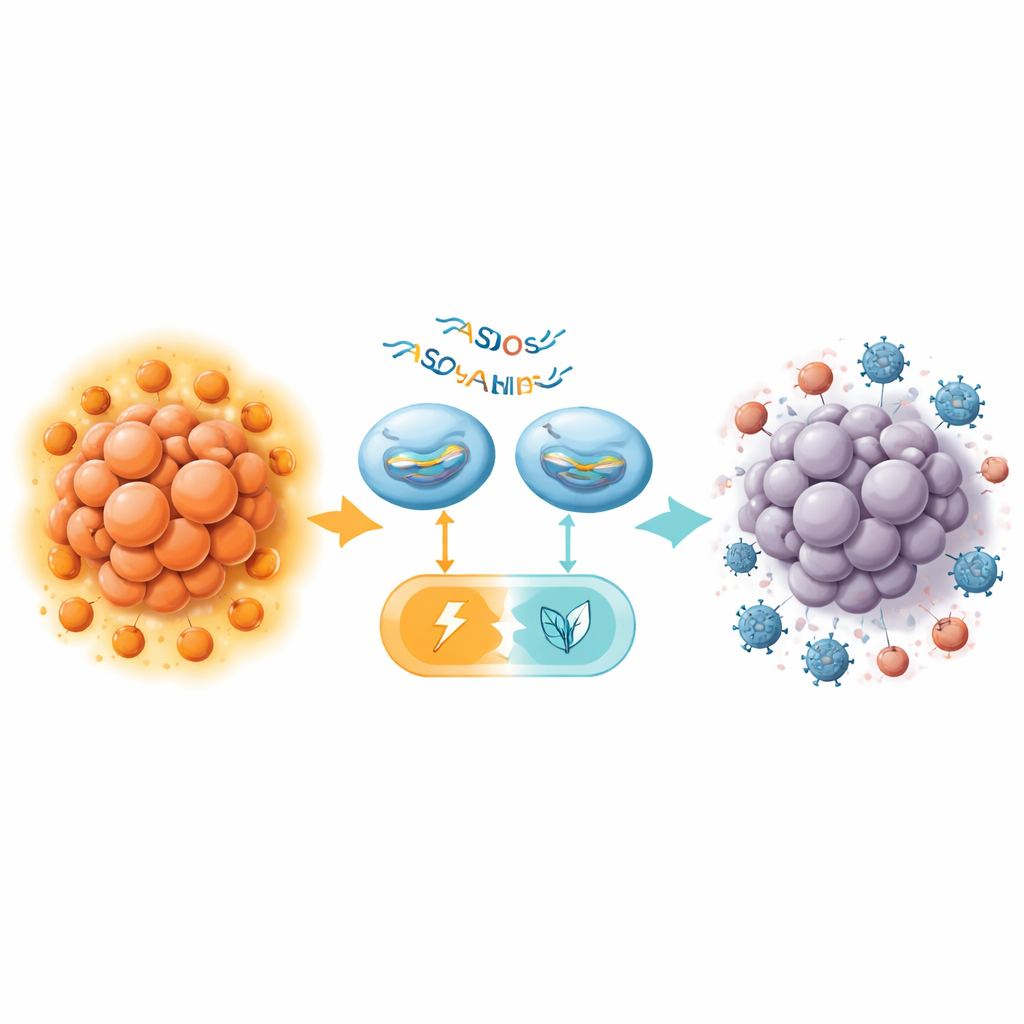
Vom metabolischen Schalter zur stärkeren Immuntherapie
In Mäusen ohne funktionierendes Immunsystem verlangsamte die systemische Verabreichung von PKM-Spleißumschalt-ASOs das Tumorwachstum der Bauchspeicheldrüse, erhöhte den Tumorzelltod und reduzierte die Glykolyse, alles ohne offensichtliche Toxizität in empfindlichen Organen wie Leber und Niere. Die Wirkung war jedoch im Vergleich zu früheren Ergebnissen bei Leberkrebs moderat. Der entscheidende Fortschritt zeigte sich in immunkompetenten Mäusen, in denen das Team ein potentes Maus-ASO (MOE16) mit einem Anti-CTLA-4-Antikörper kombinierte, einem Checkpoint-blockierenden Wirkstoff, der auf Tregs abzielt. Allein hatte Anti-CTLA-4 kaum Auswirkungen auf Pankreastumoren, was enttäuschende klinische Befunde widerspiegelt. Die ASO-Behandlung alleine brachte nur einen geringen Nutzen. Zusammen schrumpften die Tumoren jedoch deutlich stärker und hinterließen bei der Untersuchung manchmal nur noch winzige Reste.
Einen „kalten“ Tumor empfänglicher machen
Eine genauere Untersuchung der behandelten Maus-Tumoren zeigte, dass das PKM-Spleißumschalten die Enzymlevel sowohl in Krebszellen als auch in CD4-positiven T-Zellen veränderte, die Zahl infiltrierender Tregs verringerte und den lokalen Stoffwechsel umgestaltete. Indem die Abhängigkeit des Tumors von der PKM2-gestützten Glykolyse gelockert und die umgebenden Tregs geschwächt wurden, schien die ASO-Behandlung das Tumormikromilieu weniger suppressiv und für einen Immunangriff zugänglicher zu machen. Während weitere Arbeiten in langsameren, realistischeren Modellen und an humanen Geweben erforderlich sind, deuten diese Befunde darauf hin, dass das präzise Ansteuern eines einzelnen metabolischen Schalters einen resistenten Pankreastumor in einen verwandeln kann, der endlich auf Immuntherapie anspricht.
Zitation: Han, L., Gan, L., Schäfer, B. et al. ASO-based PKM splice-switching therapy increases anti-CTLA-4 antibody efficacy in pancreatic ductal adenocarcinoma. Cell Discov 12, 28 (2026). https://doi.org/10.1038/s41421-026-00882-9
Schlüsselwörter: Bauchspeicheldrüsenkrebs, Tumorstoffwechsel, Immuntherapie, regulatorische T-Zellen, Antisense-Oligonukleotide