Clear Sky Science · he
טיפול מעקף-חיתוך של PKM מבוסס ASO מעלה את היעילות של נוגדן אנטי-CTLA-4 בסרטן צינורי של הלבלב
להפעיל מחדש את ההגנות של הגוף
סרטן הלבלב ידוע כקשה לטיפול, בין השאר כיוון שהגידולים מתחפשים בסביבה עוינת שמכבה את המערכת החיסונית. המחקר הזה בוחן אסטרטגיה דו-צדדית: לשנות את האופן שבו תאי הגידול והתאים החיסוניים שורפים סוכר, ולשלב את האיפוס המטבולי הזה עם חומר אימונותרפי קיים. הממצאים מרמזים כי מיקוד מדויק במטבוליזם של הסרטן יכול להפוך גידול שנחשב "קר" לרגיש יותר להתקפה חיסונית.
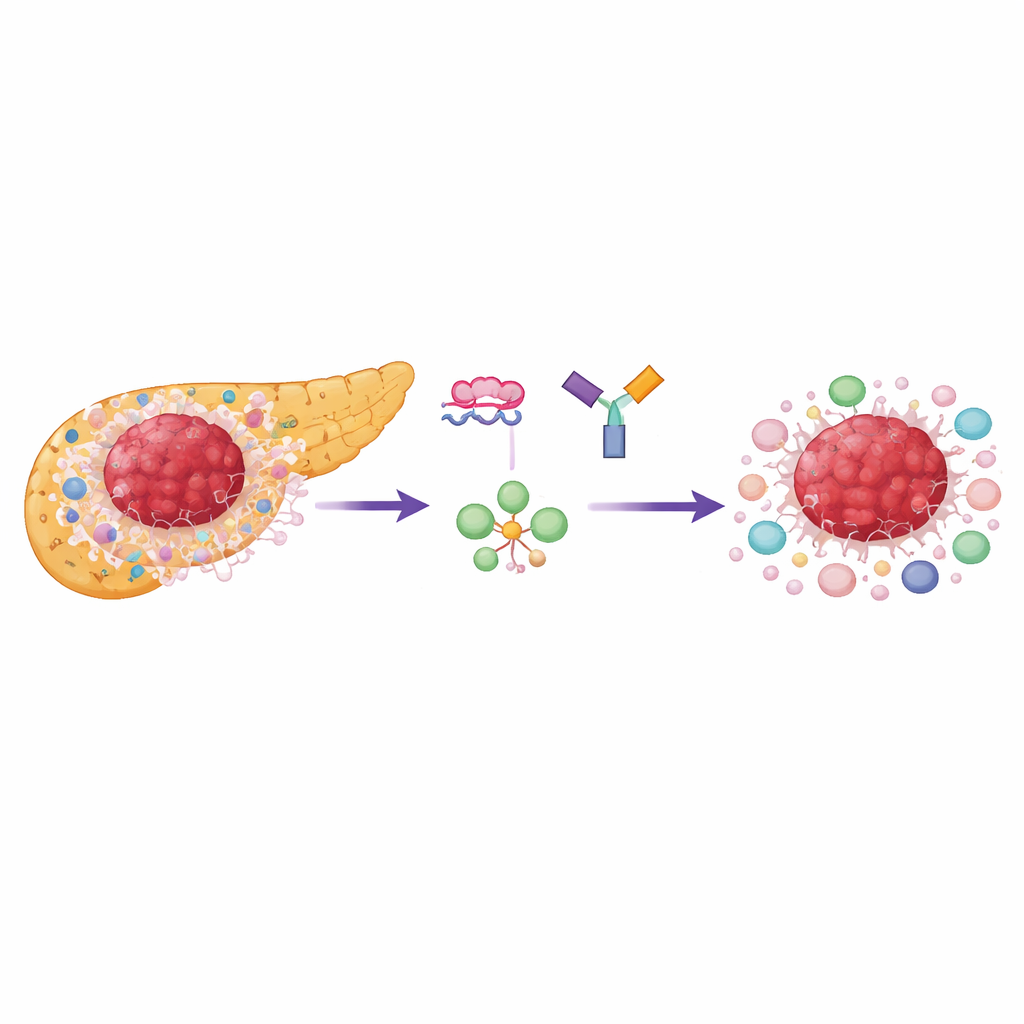
מדוע גידולי הלבלב קשים כל כך
אדנו-קרצינומה דוקטלית של הלבלב צומחת בתוך רקמה צפופה ומחוספסת המלאה בתאי תמיכה ותאי חיסון מיוחדים שמדכאים התקפה, במיוחד תאי T רגולטוריים (Tregs). הן תאי הסרטן והן רבים מהתאים הסמוכים מסתמכים במידה רבה על צורת שימוש מהירה בסוכר שנקראת גליקוליזה אירובית. נקודת בקרה מרכזית בתהליך הזה היא אנזים שנקרא פירובט קינאז, שקיים בשתי צורות: PKM1 ו-PKM2. רוב הרקמות הבשלות הרגילות משתמשות ב-PKM1, אך תאים המחלקים במהירות ותאים חיסוניים מעדיפים את PKM2, התומך באנרגיה מהירה ובחומרי בניין לצמיחה. החוקרים מצאו כי PKM2 מוגבר במידה ניכרת בגידולי לבלב אנושיים ומקושר להישרדות גרועה יותר, בעוד ש-PKM1 נשאר נמוך ברוב אזורי הגידול.
שינוי שימוש הסוכר של הגידול באמצעות DNA מתוכנן
הצוות השתמש בקטעים קצרים וסינתטיים של חומר דמוי-DNA הקרוים אוליגונוקלאוטידים אנטיסנס (ASOs) כדי לכפות על התאים לייצר יותר PKM1 ופחות PKM2 מאותו גן. ה"מעבר באתר החיתוך" הזה אינו מסיר את הגן; במקום זאת הוא משנה איזו גרסה של האנזים מיוצרת. בתרביות תאים, ה-ASO הללו הזיזו ביעילות תאי סרטן לבלב לעבר ביטוי של PKM1, הגבירו את הפעילות הכוללת של האנזים והפחיתו בצורה חדה את הלקטט, תוצר סופי של גליקוליזה. תאי גידול בסוג "בסלי"—תת-סוג אגרסיבי יותר—היו רגישים במיוחד, וצמיחתם האטה יותר מאשר בתת-הסוג הקלאסי. חשוב לציין שהאיטיות בצמיחה תלתה בעיקר בהפחתת PKM2 ולא רק בהגברת PKM1, מה שמדגיש עד כמה הגידולים מסתמכים על תוכנית המטבוליזם המונעת על ידי PKM2.
מיפוי מרכז מטבולי סביב הגידול
כדי להבין אילו תאים בשכונת הגידול עלולים גם להיות מושפעים, החוקרים שילבו צביעת רקמות עם מפות ביטוי גנים יחיד-תאיות ומרחביות מסרטן הלבלב האנושי. הם הבחינו כי תאים רבים שאינם עצביים וביטאו את הגן PKM, בפועל השתמשו בצורה PKM2. במיוחד, תאי סרטן בסוג הבסלי והתאי T רגולטוריים מופעלים סמוכים הציגו ביטוי גבוה של PKM וחתימות גליקוליטיות חזקות. ניתוח מרחבי הראה שהאזורים הפעילים מטבולית ביותר, ההיפוקסיים—שבו תאי הסרטן יותר בסגנון בסלי—היו מקיפים על ידי Tregs מופעלים שתלויים בגליקוליזה לשמר את התנהגותם המדכאת. השותפות הפיזית והמטבולית הצמודה הזו בין תאי הגידול ל-Tregs סימנה נישה שנוטה מאוד לדיכוי חיסוני.
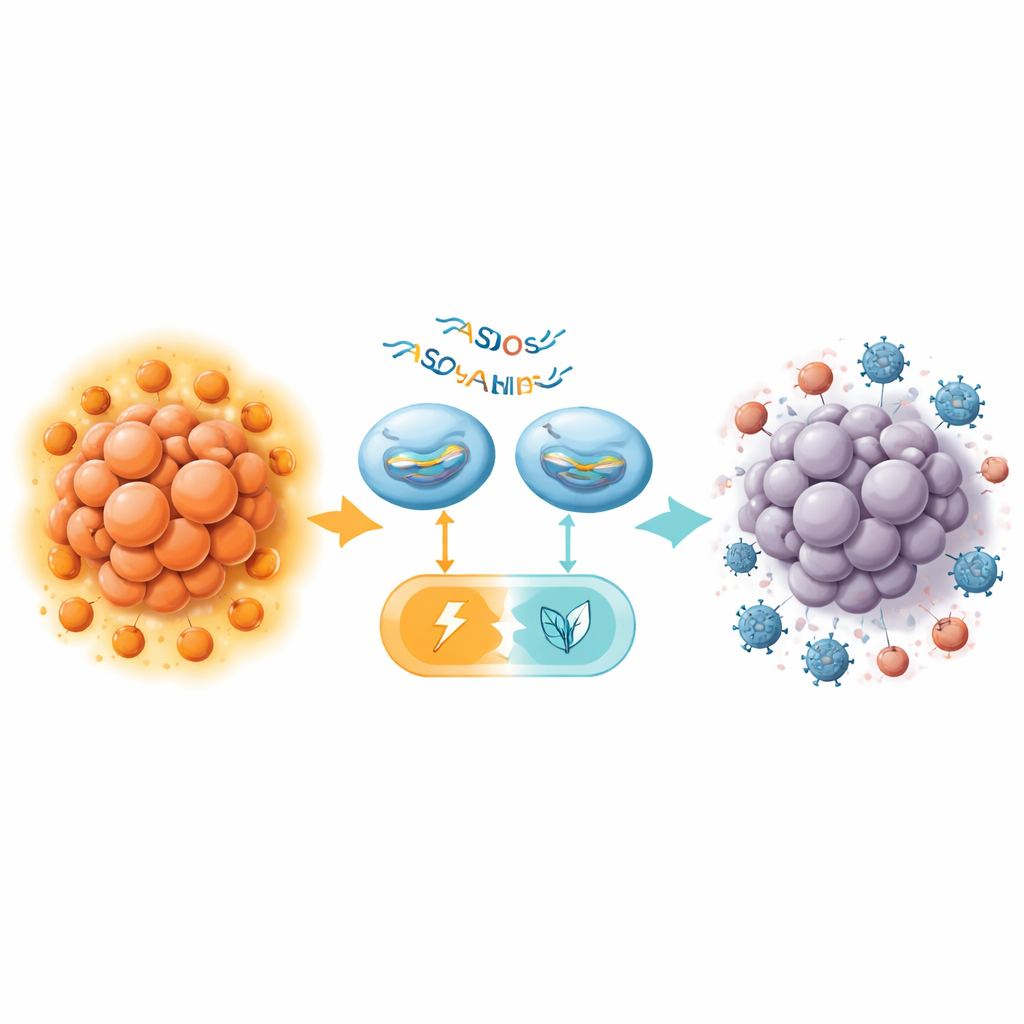
ממעבר מטבולי לאימונותרפיה עוצמתית יותר
בעכברים חסרי מערכת חיסון פונקציונלית, הזרקה ישירה של ASOs המשנים את חיתוך PKM האטה את גדילת גידולי הלבלב, הגבירה את מוות תאי הגידול וחתכה את הגליקוליזה—והכל ללא רעילות נראית לעין באיברים רגישים כמו כבד וכליות. עם זאת, ההשפעה הייתה מתונה בהשוואה לתוצאות מוקדמות בסרטן הכבד. ההתקדמות המכרעת הגיעה בעכברים עם מערכת חיסון תקינה, שם שילב הצוות ASO עוצמתי לעכברים (MOE16) עם נוגדן אנטי-CTLA-4, תרופה החוסמת נקודות בידוד המיועדת ל-Tregs. לבדה, אנטי-CTLA-4 השפיעה מעט על גידולי הלבלב, בדומה לתוצאות מאכזבות בניסויים קליניים. הטיפול ב-ASO לבדו נתן תועלת קלה בלבד. יחדיו, עם זאת, שתי הטיפולים הקטינו את הגידולים ביעילות רבה יותר, לעתים משאירים שרידים זעירים בלבד בבדיקה.
להפוך גידול "קר" לרגיש יותר
בדיקה מדוקדקת יותר של גידולים שטופלו בעכברים הראתה כי מעבר החיתוך של PKM שינה רמות אנזים גם בתוך תאי הסרטן וגם בתאי CD4 חיוביים, צמצם את מספר ה-Tregs החודרים ושינה את המטבוליזם המקומי. על ידי הפחתת התלות של הגידול בגליקוליזה מונעת על ידי PKM2 והחלשת ה-Tregs הסובבים, הטיפול ב-ASO נראה כמי שעושה את מיקרו-הסביבה של הגידול לפחות מדכאת ויותר פתוחה להתקפה חיסונית. בעוד שיש צורך בעבודה נוספת במודלים איטיים וריאליסטיים יותר וברקמות מקור אנושי, הממצאים הללו מצביעים על כך שמיקוד מדויק במתג מטבולי יחיד יכול להפוך גידול לבלתי-תגובה לסריון שמגיב לבסוף לאימונותרפיה.
ציטוט: Han, L., Gan, L., Schäfer, B. et al. ASO-based PKM splice-switching therapy increases anti-CTLA-4 antibody efficacy in pancreatic ductal adenocarcinoma. Cell Discov 12, 28 (2026). https://doi.org/10.1038/s41421-026-00882-9
מילות מפתח: סרטן הלבלב, מטבוליזם הגידול, אימונותרפיה, תאי T רגולטוריים, אוליגונוקלאוטידים אנטיסנס