Clear Sky Science · pt
Terapia de mudança de splicing do PKM baseada em ASO aumenta a eficácia do anticorpo anti‑CTLA‑4 em adenocarcinoma ductal pancreático
Reativando as Defesas do Corpo
O câncer de pâncreas é notoriamente difícil de tratar, em parte porque os tumores se envolvem em um microambiente hostil que desativa o sistema imunológico. Este estudo explora uma estratégia dupla: reprogramar como células tumorais e imunes metabolizam a glicose e combinar esse reajuste metabólico com um medicamento de imunoterapia já existente. O trabalho sugere que direcionar com precisão o metabolismo do câncer pode tornar um tumor “frio” mais sensível ao ataque imune.
Por Que os Tumores Pancreáticos São Tão Difíceis
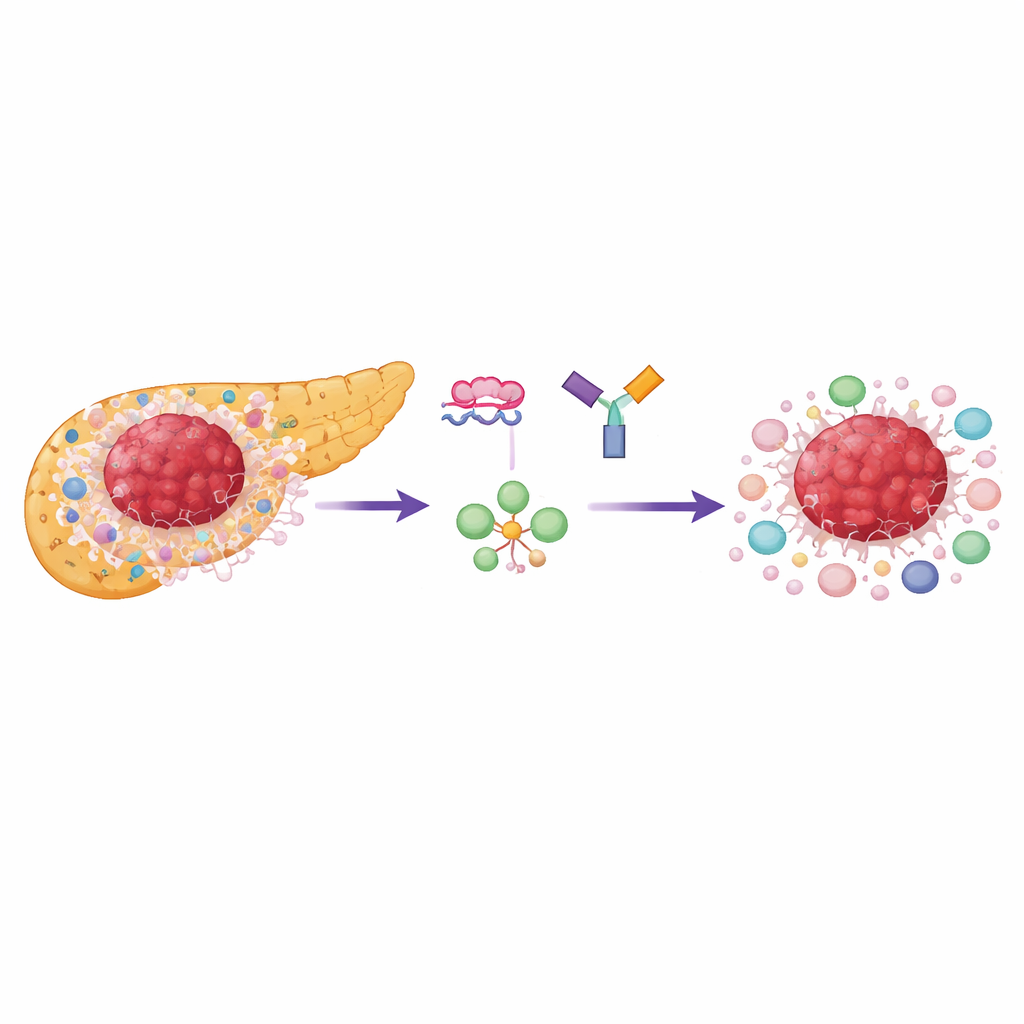
O adenocarcinoma ductal pancreático cresce dentro de um tecido denso, semelhante a cicatriz, repleto de células de suporte e células imunes especializadas que suprimem o ataque, especialmente as células T reguladoras (Tregs). Tanto as células cancerosas quanto muitos vizinhos dependem fortemente de uma forma de uso de açúcar de queima rápida chamada glicólise aeróbica. Um ponto de controle-chave nesse processo é uma enzima chamada piruvato quinase, que existe em duas formas: PKM1 e PKM2. A maioria dos tecidos normais e maduros usa PKM1, mas células em divisão rápida e células imunes favorecem PKM2, que sustenta energia rápida e blocos de construção para crescimento. Os pesquisadores descobriram que PKM2 está amplamente elevada em tumores pancreáticos humanos e associada a pior sobrevida, enquanto PKM1 permanece baixa na maior parte das áreas tumorais.
Reprogramando o Uso de Açúcar do Tumor com DNA Projetado
A equipe usou filamentos curtos e sintéticos de material semelhante ao DNA chamados oligonucleotídeos antissenso (ASOs) para forçar as células a produzirem mais PKM1 e menos PKM2 a partir do mesmo gene. Essa “mudança de splicing” não remove o gene; em vez disso, altera qual versão da enzima é produzida. Em cultura celular, esses ASOs deslocaram efetivamente células de câncer pancreático em direção a PKM1, aumentaram a atividade enzimática total e reduziram fortemente o lactato, produto final da glicólise. Células tumorais do subtipo basal — um subtipo mais agressivo — foram especialmente sensíveis, desacelerando o crescimento mais do que o chamado subtipo clássico. Importante, a desaceleração do crescimento dependia principalmente da redução de PKM2 em vez de apenas do aumento de PKM1, ressaltando o quanto os tumores dependem do programa metabólico dirigido por PKM2.
Mapeando um Ponto Metabólico Ativo em Torno do Tumor
Para entender quais células na vizinhança tumoral também poderiam ser afetadas, os pesquisadores combinaram coloração tecidual com mapas de expressão gênica espacial e em célula única de cânceres pancreáticos humanos. Eles observaram que muitas células não neuronais que expressavam o gene PKM, na prática, estavam usando a forma PKM2. Em particular, células cancerosas do tipo basal e Tregs ativadas próximas mostraram alta expressão de PKM e fortes assinaturas glicolíticas. A análise espacial revelou que as regiões mais metabolicamente ativas e hipóxicas — onde as células cancerosas são mais do tipo basal — eram circundadas por Tregs ativadas que dependem da glicólise para manter seu comportamento supressor. Essa estreita parceria física e metabólica entre células tumorais e Tregs marcou um nicho especialmente imunossupressor.
Da Mudança Metabólica a uma Imunoterapia Mais Eficaz
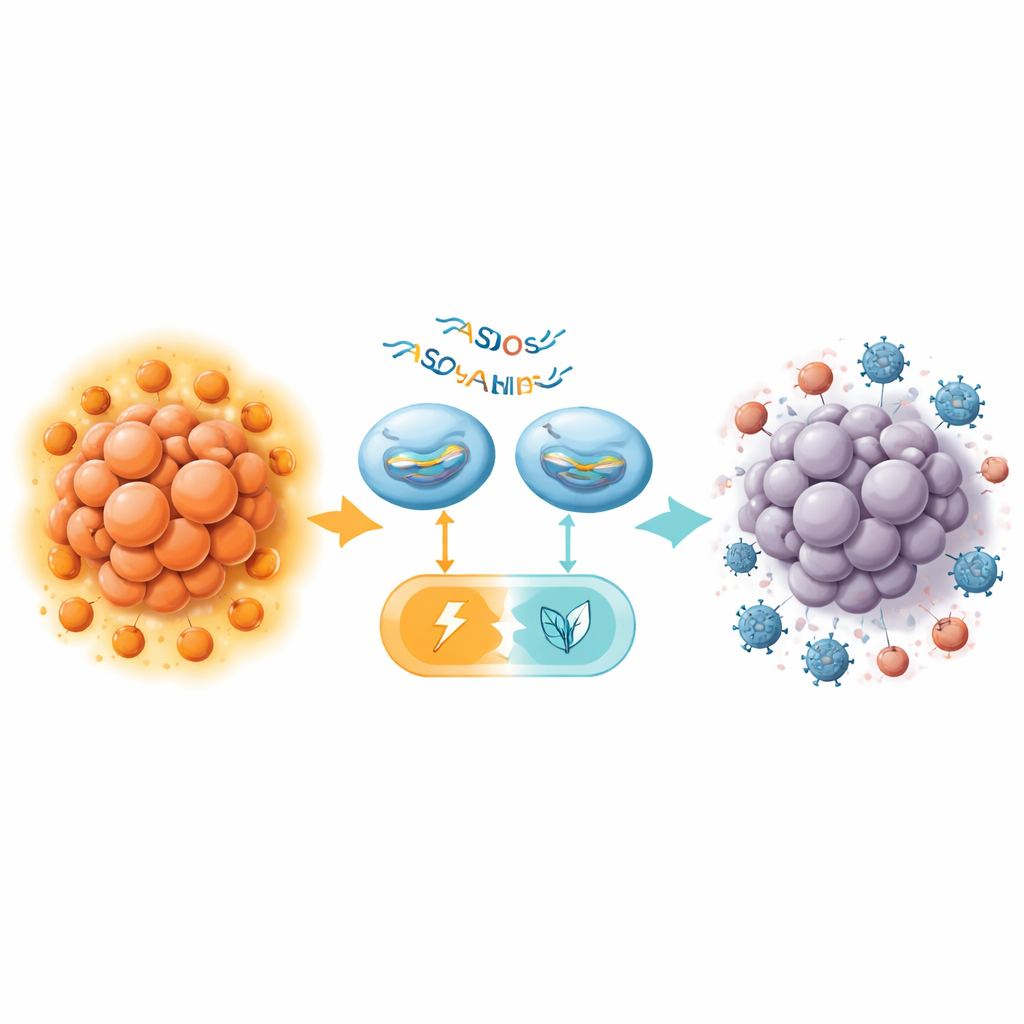
Em camundongos sem um sistema imune funcional, a administração de ASOs que promovem a mudança de splicing do PKM diretamente no organismo retardou o crescimento tumoral pancreático, aumentou a morte de células tumorais e reduziu a glicólise, tudo isso sem toxicidade óbvia em órgãos sensíveis como fígado e rim. No entanto, o efeito foi modesto em comparação com resultados anteriores em câncer de fígado. O avanço-chave veio em camundongos imunocompetentes, onde a equipe combinou um ASO potente para camundongos (MOE16) com um anticorpo anti‑CTLA‑4, um medicamento bloqueador de checkpoint direcionado às Tregs. Isoladamente, o anti‑CTLA‑4 teve pouco impacto nos tumores pancreáticos, ecoando ensaios clínicos decepcionantes. O tratamento com ASO sozinho produziu apenas um benefício leve. Juntos, porém, as duas terapias encolheram os tumores muito mais efetivamente, às vezes deixando apenas pequenos remanescentes à inspeção.
Tornando um Tumor “Frio” Mais Responsivo
Exames mais detalhados dos tumores de camundongo tratados mostraram que a mudança de splicing do PKM alterou os níveis da enzima tanto dentro das células cancerosas quanto nas células T CD4 positivas, reduziu o número de Tregs infiltrantes e remodelou o metabolismo local. Ao reduzir a dependência do tumor da glicólise alimentada por PKM2 e enfraquecer as Tregs ao redor, o tratamento com ASO pareceu tornar o microambiente tumoral menos supressor e mais permissivo ao ataque imune. Embora sejam necessários mais estudos em modelos mais lentos e realistas e em tecidos derivados de humanos, essas descobertas sugerem que direcionar precisamente um único interruptor metabólico pode transformar um tumor pancreático resistente em um que finalmente responde à imunoterapia.
Citação: Han, L., Gan, L., Schäfer, B. et al. ASO-based PKM splice-switching therapy increases anti-CTLA-4 antibody efficacy in pancreatic ductal adenocarcinoma. Cell Discov 12, 28 (2026). https://doi.org/10.1038/s41421-026-00882-9
Palavras-chave: câncer de pâncreas, metabolismo tumoral, imunoterapia, células T reguladoras, oligonucleotídeos antissenso