Clear Sky Science · ru
Терапия переключения сплайсинга PKM на основе ООН увеличивает эффективность антител против CTLA-4 при аденокарциноме протоков поджелудочной железы
Включая защиту организма снова
Рак поджелудочной железы печально знаменит своей трудноизлечимостью, отчасти потому, что опухоли создают враждебную среду, которая подавляет иммунную систему. В этом исследовании рассматривается двухэтапная стратегия: перенастройка использования сахаров в опухолевых и иммунных клетках и сочетание этой метаболической «перезагрузки» с существующим препаратом иммунотерапии. Работа показывает, что точечное воздействие на метаболизм рака может превратить в противоборство с иммунитетом иначе «холодную» опухоль.
Почему опухоли поджелудочной железы так стойки
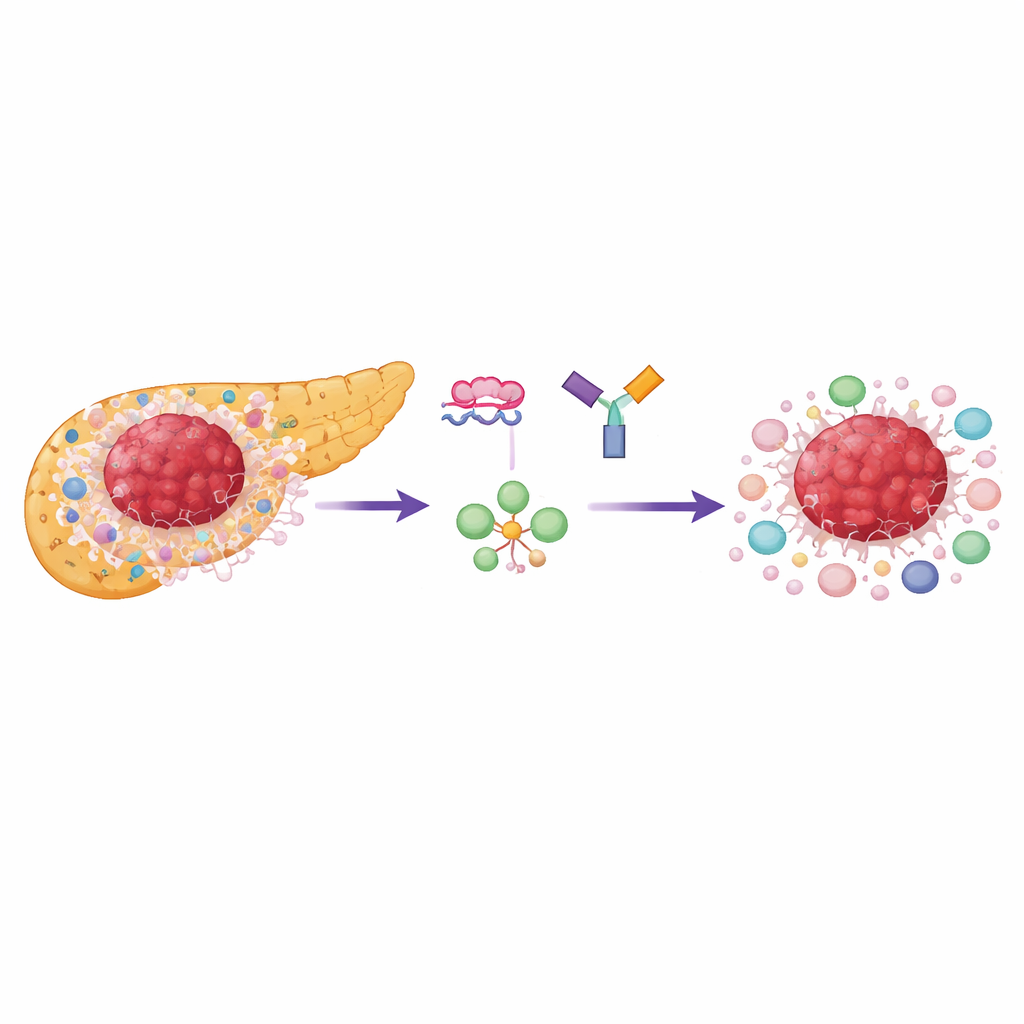
Аденокарцинома протоков поджелудочной железы развивается в плотной, рубцоподобной ткани, насыщенной вспомогательными клетками и специализированными иммунными клетками, подавляющими атаку, особенно регуляторными T-клетками (Tregs). И сами раковые клетки, и многие клетки окружения сильно зависят от быстрого способа использования сахара, называемого аэробным гликолизом. Ключевой контрольный пункт в этом процессе — фермент пируваткиназа, который существует в двух вариантах: PKM1 и PKM2. В большинстве нормальных зрелых тканей доминирует PKM1, тогда как быстро делящиеся клетки и иммунные клетки предпочитают PKM2, поддерживающий быстрое получение энергии и строительных блоков для роста. Исследователи обнаружили, что PKM2 значительно повышен в тканях человеческих опухолей поджелудочной железы и связан с худшей выживаемостью, в то время как PKM1 остается низким в большинстве областей опухоли.
Перенастройка использования сахара в опухоли при помощи дизайнерской ДНК
Команда использовала короткие синтетические цепочки похожего на ДНК материала, называемые антисмысловыми олигонуклеотидами (ASO), чтобы заставить клетки производить больше PKM1 и меньше PKM2 из одного и того же гена. Такое «переключение сплайсинга» не удаляет ген: оно меняет, какая версия фермента синтезируется. В культуре клеток эти ASO эффективно сдвигали панкреатические раковые клетки в сторону PKM1, увеличивали общую активность фермента и резко снижали количество лактата — конечного продукта гликолиза. Базало-подобные (basal-like) опухолевые клетки — более агрессивный подтип — оказались особенно чувствительны и замедляли рост сильнее, чем так называемый классический подтип. Важно, что замедление роста в основном зависело от снижения PKM2, а не просто от увеличения PKM1, что подчеркивает, насколько опухоли опираются на метаболическую программу, управляемую PKM2.
Картирование метаболического «очага» вокруг опухоли
Чтобы понять, какие клетки в окрестности опухоли также могут подвергаться воздействию, исследователи совместили окрашивание тканей с данными единично-клеточной и пространственной транскриптомики человеческих опухолей поджелудочной железы. Они наблюдали, что многие не-нервные клетки, экспрессирующие ген PKM, фактически использовали форму PKM2. В частности, базало-подобные раковые клетки и соседние активированные Tregs показывали высокую экспрессию PKM и выраженные признаки гликолитической активности. Пространственный анализ выявил, что наиболее метаболически активные, гипоксические области — где клетки более базало-подобны — окружены активированными Tregs, которые зависят от гликолиза для поддержания своей супрессивной функции. Это тесное физическое и метаболическое партнерство между опухолевыми клетками и Tregs обозначает особенно иммуносупрессивную нишу.
От метаболического переключения к усиленной иммунотерапии
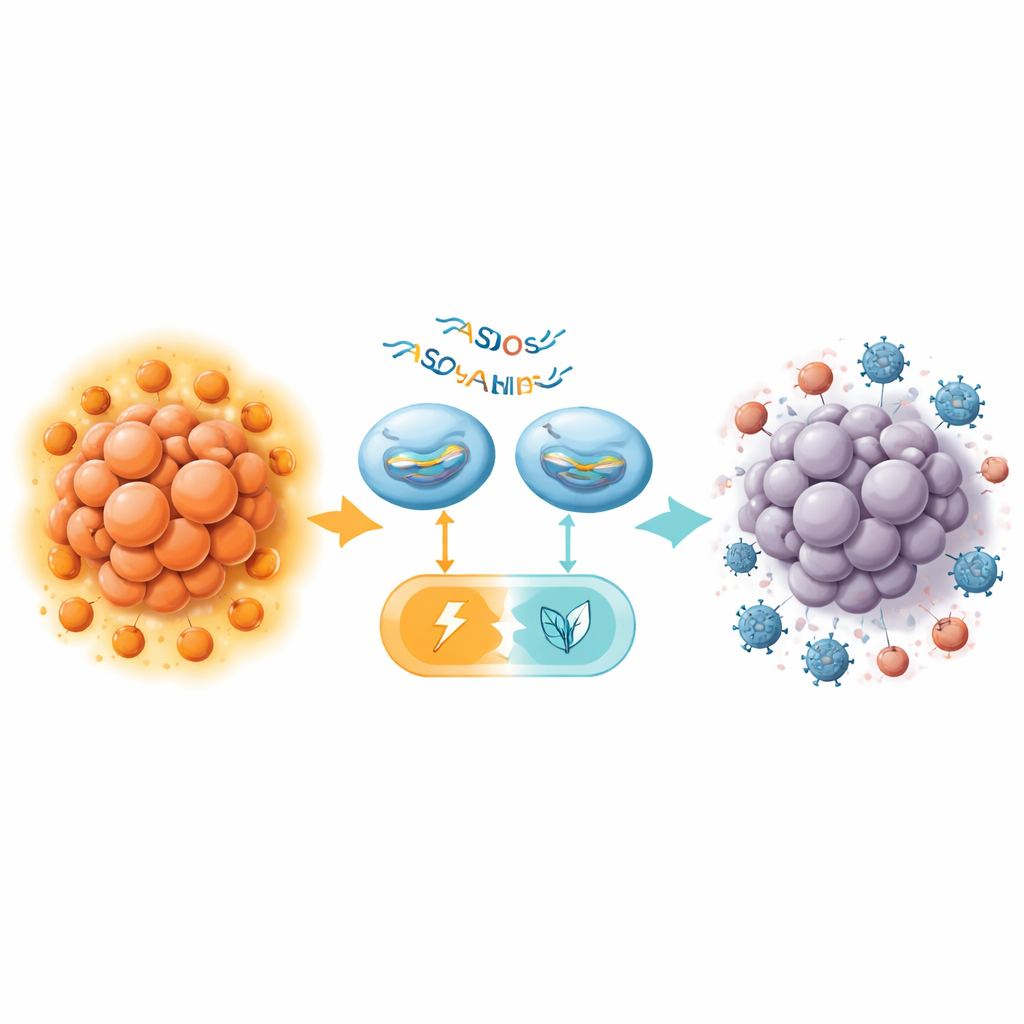
У мышей без функционирующей иммунной системы внутривенное введение ASO для переключения сплайсинга PKM замедляло рост опухолей поджелудочной железы, увеличивало гибель опухолевых клеток и снижало гликолиз, при этом не наблюдалось явной токсичности в чувствительных органах, таких как печень и почки. Однако эффект был умеренным по сравнению с предыдущими результатами в раке печени. Ключевое достижение было получено у иммунокомпетентных мышей, где команда сочетала мощный мышиный ASO (MOE16) с антителом против CTLA-4, ингибитором контрольной точки, нацеленным на Tregs. Само по себе антитело против CTLA-4 мало влияло на опухоли поджелудочной железы, что согласуется с неутешительными клиническими данными. Лечение только ASO давало лишь небольшую пользу. Однако в комбинации оба препарата значительно сократили опухоли, иногда оставляя при осмотре лишь небольшие остатки.
Делая «холодную» опухоль более чувствительной
Более глубокий анализ леченных опухолей у мышей показал, что переключение сплайсинга PKM изменяло уровни фермента как в раковых клетках, так и в CD4-положительных T-клетках, уменьшало число инфильтрирующихся Tregs и перестраивало местный метаболизм. Ослабляя зависимость опухоли от гликолиза, питаемого PKM2, и подрывая окружающие Tregs, лечение ASO делало микросреду опухоли менее супрессивной и более благоприятной для иммунной атаки. Хотя необходимы дополнительные исследования в более медленных, реалистичных моделях и на тканях человеческого происхождения, эти результаты указывают на то, что прицельное вмешательство в один метаболический переключатель может превратить устойчивую опухоль поджелудочной железы в опухоль, наконец отвечающую на иммунотерапию.
Цитирование: Han, L., Gan, L., Schäfer, B. et al. ASO-based PKM splice-switching therapy increases anti-CTLA-4 antibody efficacy in pancreatic ductal adenocarcinoma. Cell Discov 12, 28 (2026). https://doi.org/10.1038/s41421-026-00882-9
Ключевые слова: рак поджелудочной железы, метаболизм опухоли, иммунотерапия, регуляторные T-клетки, антисмысловые олигонуклеотиды