Clear Sky Science · nl
ASO-gebaseerde PKM splice-switching therapie verhoogt de werkzaamheid van anti-CTLA-4-antistoffen bij pancreatische ductale adenocarcinoom
De verdedigingslinie van het lichaam weer activeren
Pancreaskanker is berucht lastig te behandelen, deels omdat tumoren zich omringen met een vijandige omgeving die het immuunsysteem uitschakelt. Deze studie onderzoekt een tweesporenstrategie: het herprogrammeren van hoe tumor- en immuuncellen suiker verbranden, en het combineren van die metabolische reset met een bestaande immunotherapie. Het werk suggereert dat zorgvuldig targeten van kankermetabolisme een anders ‘koude’ tumor gevoeliger kan maken voor immuunaanvallen.
Waarom pancreastumoren zo hardnekkig zijn
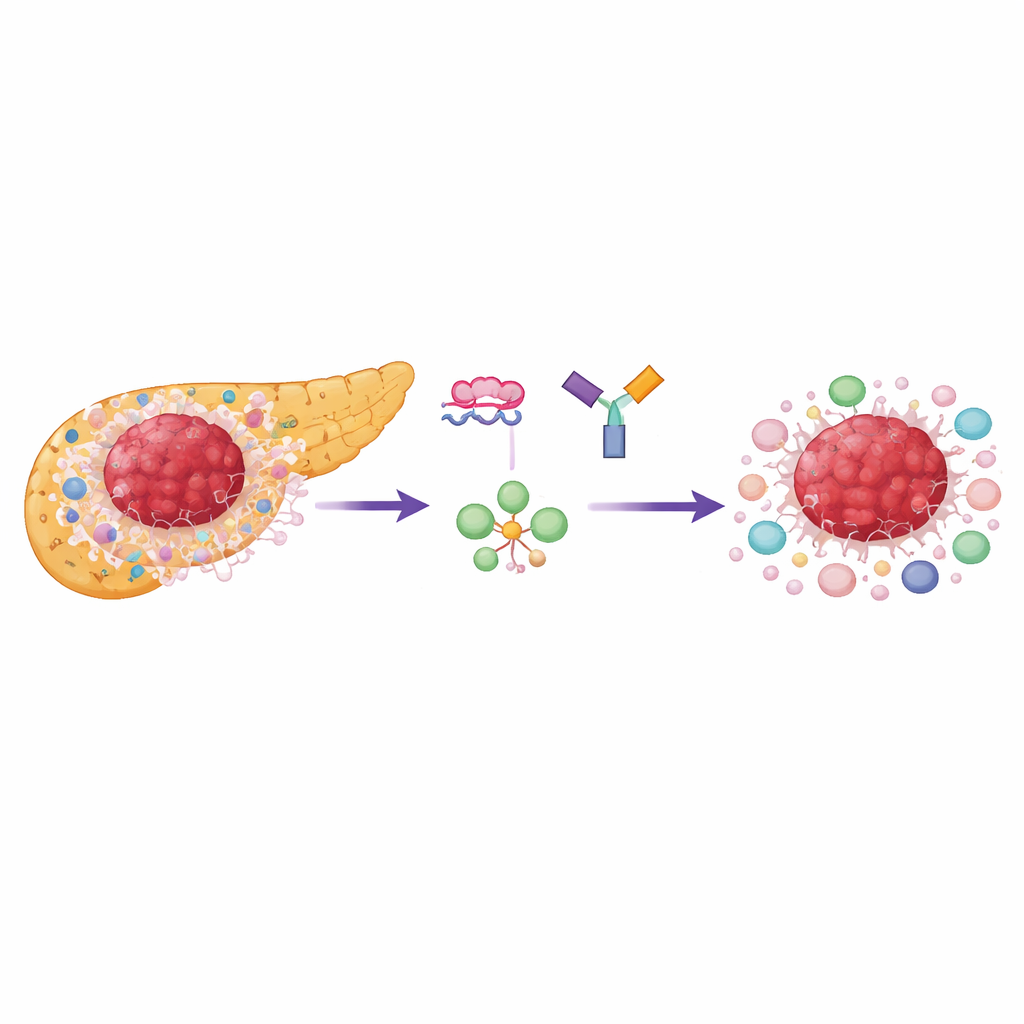
Pancreatisch ductaal adenocarcinoom groeit binnen een dicht, littekenachtig weefsel vol steuncellen en gespecialiseerde immuuncellen die aanvallen onderdrukken, vooral regulatorische T-cellen (Tregs). Zowel de kankercellen als veel buren zijn sterk afhankelijk van een snel brandende vorm van suikergebruik die aerobe glycolyse wordt genoemd. Een belangrijk controlepunt in dit proces is een enzym genaamd pyruvaatkinase, dat in twee vormen voorkomt: PKM1 en PKM2. De meeste normale, volwassen weefsels gebruiken PKM1, maar snel delende cellen en immuuncellen geven de voorkeur aan PKM2, dat snelle energievoorziening en bouwstenen voor groei ondersteunt. De onderzoekers vonden dat PKM2 op grote schaal verhoogd is in menselijke pancreastumoren en geassocieerd met slechtere overleving, terwijl PKM1 in de meeste tumorgebieden laag blijft.
Het herschakelen van suikergebruik in tumoren met ontworpen DNA
Het team gebruikte korte, synthetische strengen van DNA-achtig materiaal, antisense-oligonucleotiden (ASO’s), om cellen te dwingen meer PKM1 en minder PKM2 uit hetzelfde gen te produceren. Deze ‘splice-switching’ verwijdert het gen niet; in plaats daarvan verandert het welke variant van het enzym wordt gemaakt. In kweek verschoven deze ASO’s effectief pancreaskankercellen richting PKM1, verhoogden de totale enzymactiviteit en verminderden sterk het lactaat, het eindproduct van glycolyse. Basale-achtige tumorcellen — een agressievere subtype — waren bijzonder gevoelig en vertraagden hun groei sterker dan het zogenoemde klassieke subtype. Belangrijk is dat de groeivertraging voornamelijk afhing van het verminderen van PKM2 en niet alleen van het verhogen van PKM1, wat benadrukt hoe sterk tumoren leunen op het PKM2-gedreven metabole programma.
Een metabool heet-spot in kaart brengen rond de tumor
Om te begrijpen welke cellen in de tumoromgeving ook beïnvloed zouden kunnen worden, combineerden de onderzoekers weefselkleuring met single-cell en ruimtelijke genexpressiekaarten van menselijke pancreaskankers. Ze observeerden dat veel niet-zenuwcellen die het PKM-gen tot expressie brengen, in de praktijk de PKM2-vorm gebruiken. In het bijzonder vertoonden basale-achtige kankercellen en nabijgelegen geactiveerde Tregs zowel hoge PKM-expressie als sterke glycolytische signaturen. Ruimtelijke analyse onthulde dat de meest metabool actieve, hypoxische regio’s — waar kankercellen meer basaal-achtig zijn — werden omringd door geactiveerde Tregs die afhankelijk zijn van glycolyse om hun onderdrukkende gedrag in stand te houden. Deze nauwe fysieke en metabole samenwerking tussen tumorcellen en Tregs markeerde een bijzonder immunosuppressieve nis.
Van metabole switch naar sterkere immunotherapie
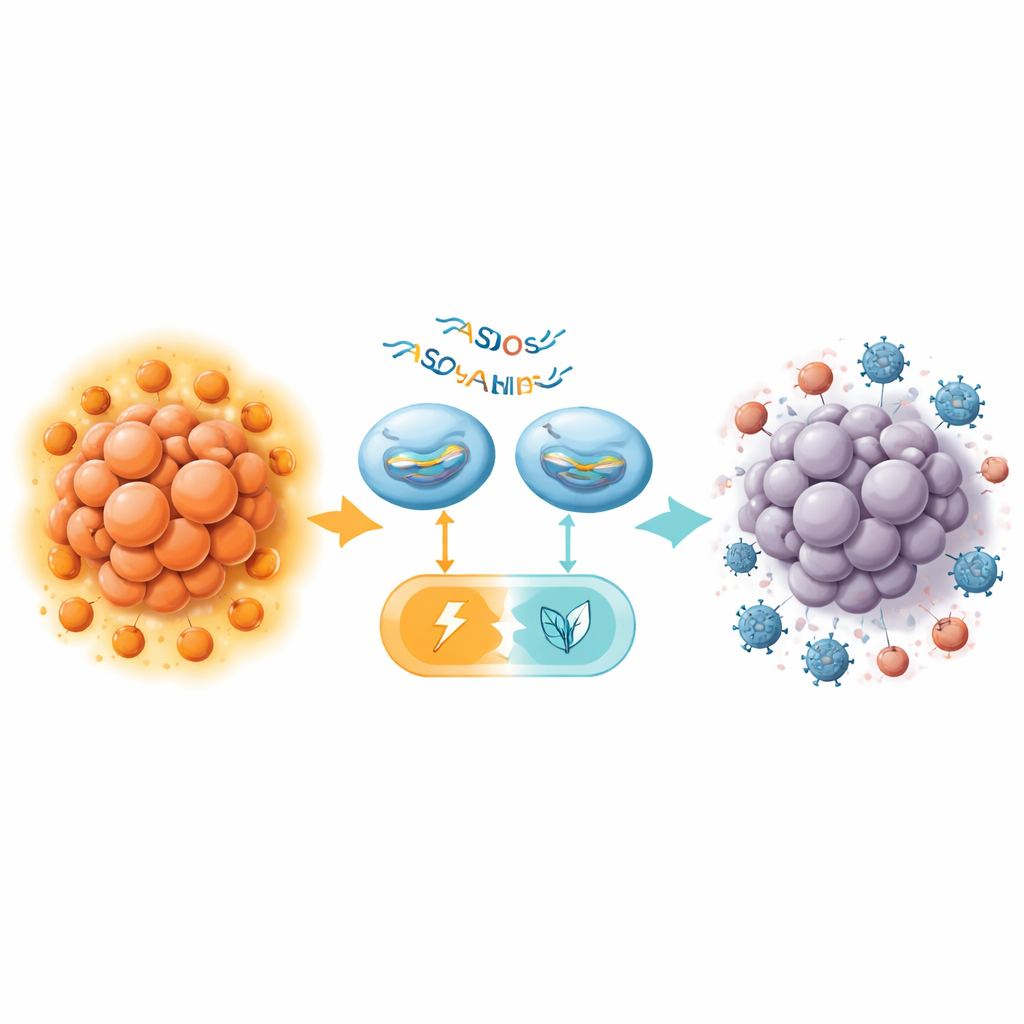
In muizen zonder functioneel immuunsysteem vertraagde het toedienen van PKM splice-switching ASO’s direct in het lichaam de groei van pancreastumoren, verhoogde het aantal afgestorven tumorcellen en verminderde glycolyse, allemaal zonder duidelijke toxiciteit in gevoelige organen zoals lever en nier. Het effect was echter bescheiden vergeleken met eerdere resultaten in leverkanker. De belangrijkste vooruitgang kwam in immuuncompetente muizen, waar het team een krachtige muis-ASO (MOE16) combineerde met een anti-CTLA-4-antistof, een checkpoint-blokkerend middel gericht op Tregs. Op zichzelf had anti-CTLA-4 weinig effect op pancreastumoren, in lijn met teleurstellende klinische proeven. ASO-behandeling alleen gaf slechts een klein voordeel. Samen daarentegen krimpten de twee therapieën tumoren veel effectiever, soms met alleen nog kleine resten bij inspectie.
Een ‘koude’ tumor gevoeliger maken
Nader onderzoek van behandelde muizen tumoren toonde aan dat PKM splice-switching enzymniveaus veranderde binnen zowel kankercellen als CD4-positieve T-cellen, het aantal infiltrerende Tregs verminderde en het lokale metabolisme hervormde. Door de afhankelijkheid van de tumor van PKM2-gedreven glycolyse te versoepelen en de omliggende Tregs te verzwakken, leek de ASO-behandeling de tumor micro-omgeving minder onderdrukkend en meer ontvankelijk voor immuuraanvallen te maken. Hoewel verder werk nodig is in langzamere, realistischer modellen en menselijk afgeleid weefsel, suggereren deze bevindingen dat het precies targeten van één enkele metabole schakel een resistente pancreastumor kan ombuigen naar een tumor die uiteindelijk op immunotherapie reageert.
Bronvermelding: Han, L., Gan, L., Schäfer, B. et al. ASO-based PKM splice-switching therapy increases anti-CTLA-4 antibody efficacy in pancreatic ductal adenocarcinoma. Cell Discov 12, 28 (2026). https://doi.org/10.1038/s41421-026-00882-9
Trefwoorden: pancreaskanker, tumormetabolisme, immunotherapie, regulerende T-cellen, antisense-oligonucleotiden