Clear Sky Science · fr
Thérapie par commutation d’épissage PKM basée sur des AO améliore l’efficacité des anticorps anti-CTLA-4 dans l’adénocarcinome canalaire pancréatique
Rallumer les défenses de l’organisme
Le cancer du pancréas est notoirement difficile à traiter, en partie parce que les tumeurs se camouflent dans un microenvironnement hostile qui neutralise le système immunitaire. Cette étude explore une stratégie en deux volets : reprogrammer la manière dont les cellules tumorales et immunitaires consomment le sucre, et combiner cette remise à zéro métabolique avec un médicament d’immunothérapie existant. Les résultats suggèrent que cibler finement le métabolisme du cancer peut rendre une tumeur autrement « froide » plus réceptive à l’attaque immunitaire.
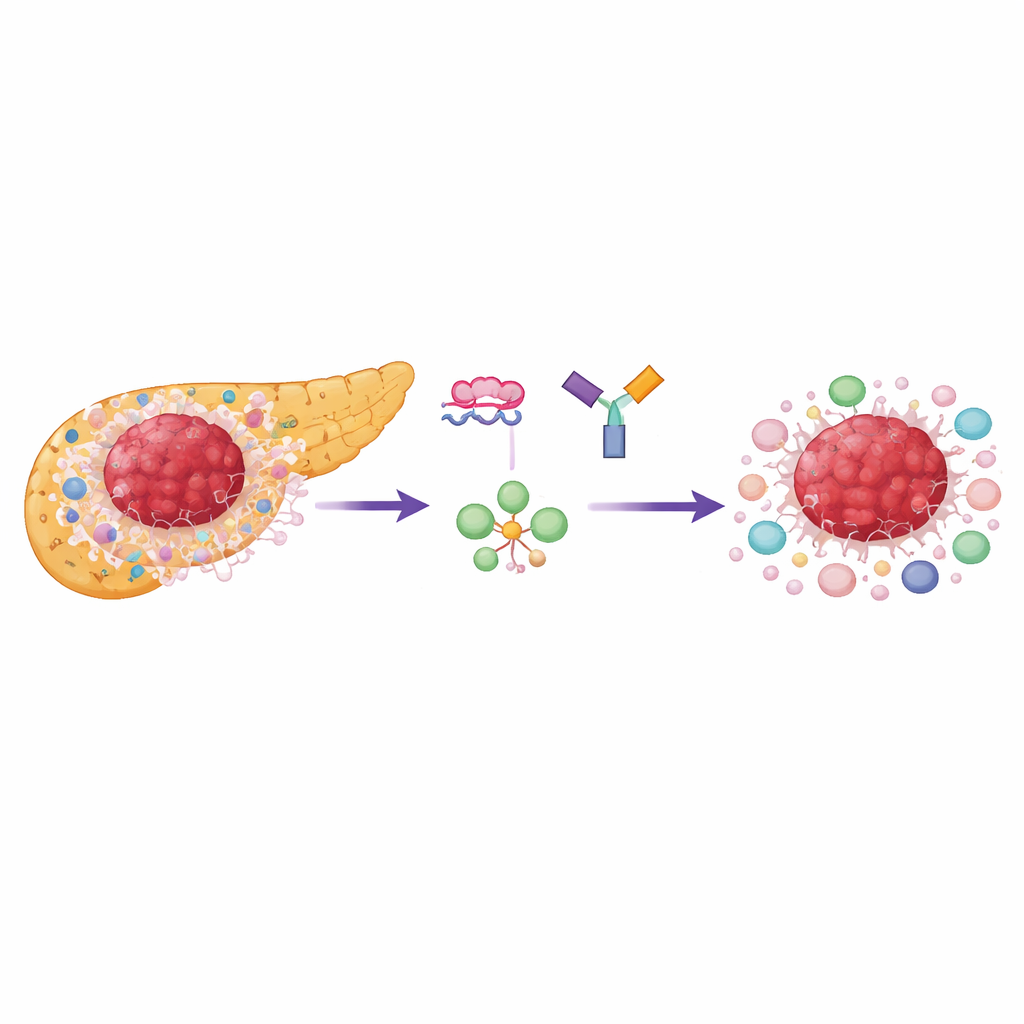
Pourquoi les tumeurs pancréatiques sont si résistantes
L’adénocarcinome canalaire pancréatique se développe au sein d’un tissu dense, cicatriciel, rempli de cellules de soutien et de cellules immunitaires spécialisées qui suppriment les attaques, en particulier les cellules T régulatrices (Tregs). Tant les cellules cancéreuses que nombre de leurs voisines dépendent fortement d’une forme de combustion rapide du sucre appelée glycolyse aérobie. Un point de contrôle clé de ce processus est une enzyme appelée pyruvate kinase, qui existe sous deux formes : PKM1 et PKM2. La plupart des tissus normaux et matures utilisent PKM1, mais les cellules en division rapide et les cellules immunitaires favorisent PKM2, qui soutient une production d’énergie rapide et fournit des éléments de construction pour la croissance. Les chercheurs ont constaté que PKM2 est largement surélevée dans les tumeurs pancréatiques humaines et associée à une survie plus défavorable, tandis que PKM1 reste faible dans la plupart des zones tumorales.
Reprogrammer l’utilisation du sucre tumoral avec de l’ADN sur mesure
L’équipe a utilisé de courtes séquences synthétiques de type ADN appelées oligonucléotides antisens (AO) pour forcer les cellules à produire davantage de PKM1 et moins de PKM2 à partir du même gène. Cette « commutation d’épissage » ne supprime pas le gène ; elle change simplement la version de l’enzyme produite. En culture cellulaire, ces AO ont efficacement orienté les cellules cancéreuses pancréatiques vers PKM1, augmenté l’activité enzymatique totale et réduit fortement le lactate, produit final de la glycolyse. Les cellules tumorales de type basal—un sous-type plus agressif—étaient particulièrement sensibles, ralentissant leur croissance davantage que le sous-type dit classique. Il est important de noter que le ralentissement de la croissance dépendait principalement de la réduction de PKM2 plutôt que de la simple augmentation de PKM1, ce qui souligne à quel point les tumeurs s’appuient sur le programme métabolique dirigé par PKM2.
Cartographier un point chaud métabolique autour de la tumeur
Pour savoir quelles cellules du voisinage tumoral pourraient également être affectées, les chercheurs ont combiné des colorations tissulaires avec des cartes d’expression génique en cellule unique et spatiales provenant de cancers pancréatiques humains. Ils ont observé que de nombreuses cellules non nerveuses exprimant le gène PKM utilisaient en pratique la forme PKM2. En particulier, les cellules tumorales de type basal et les Tregs activés à proximité présentaient toutes deux une expression élevée de PKM et de forts profils glycolytiques. L’analyse spatiale a révélé que les régions les plus métaboliquement actives et hypoxiques—où les cellules cancéreuses sont davantage de type basal—étaient entourées de Tregs activées qui dépendent de la glycolyse pour maintenir leur comportement suppressif. Ce partenariat physique et métabolique étroit entre cellules tumorales et Tregs constituait un créneau particulièrement immunosuppresseur.
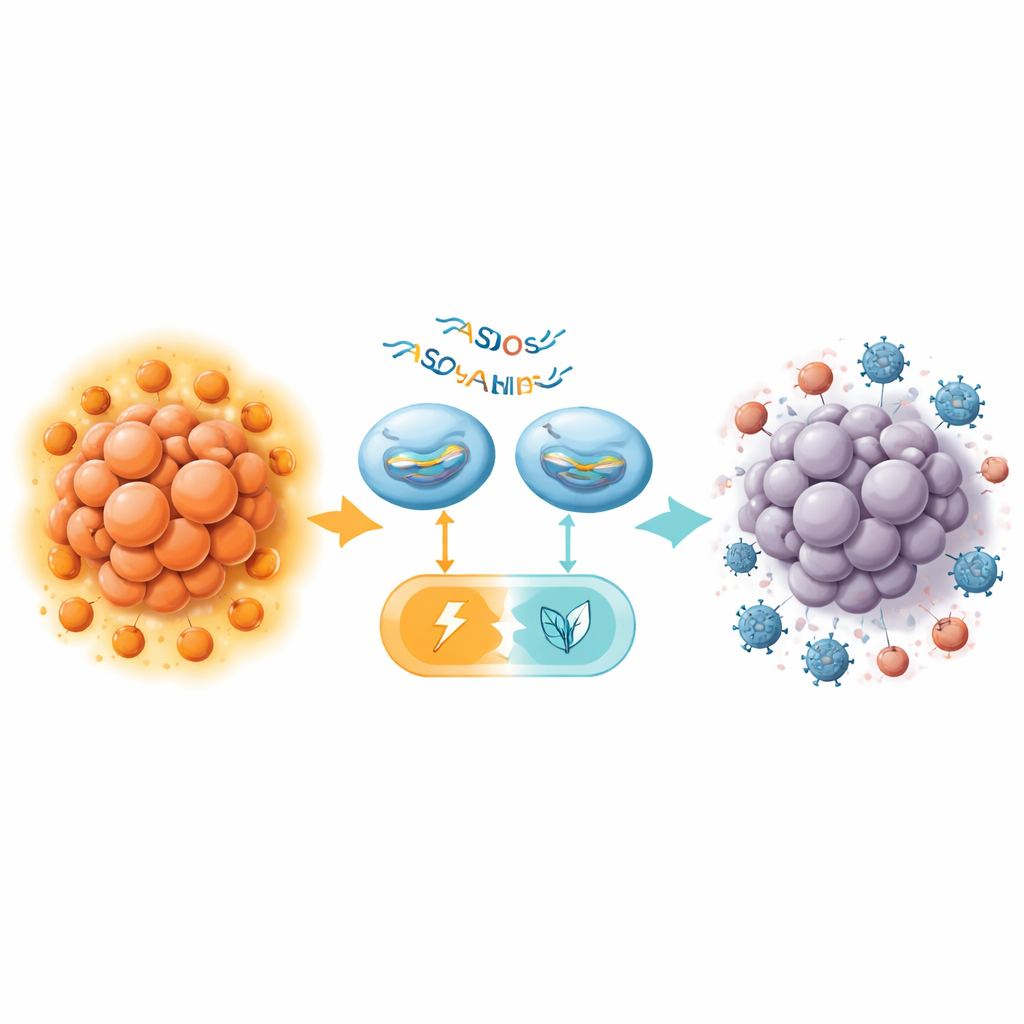
De l’inversion métabolique à une immunothérapie renforcée
Chez des souris dépourvues d’un système immunitaire fonctionnel, l’administration d’AO de commutation d’épissage PKM directement in vivo a ralenti la croissance des tumeurs pancréatiques, augmenté la mort des cellules tumorales et réduit la glycolyse, le tout sans toxicité évidente dans des organes sensibles comme le foie et le rein. Cependant, l’effet était modeste comparé aux résultats antérieurs dans le cancer du foie. L’avancée clé est venue chez des souris immunocompétentes, où l’équipe a combiné un AO murin puissant (MOE16) avec un anticorps anti-CTLA-4, un médicament bloquant un point de contrôle ciblant les Tregs. Pris isolément, l’anti-CTLA-4 avait peu d’impact sur les tumeurs pancréatiques, rappelant des essais cliniques décevants. Le traitement par AO seul produisait seulement un bénéfice limité. Ensemble, cependant, les deux thérapies ont réduit les tumeurs beaucoup plus efficacement, laissant parfois à l’inspection de simples vestiges minimes.
Rendre une tumeur « froide » plus réactive
Un examen plus approfondi des tumeurs traitées chez la souris a montré que la commutation d’épissage de PKM modifiait les niveaux d’enzyme à la fois dans les cellules cancéreuses et dans les cellules T CD4 positives, réduisait le nombre de Tregs infiltrants et remodelait le métabolisme local. En allégeant la dépendance de la tumeur à la glycolyse alimentée par PKM2 et en affaiblissant les Tregs environnants, le traitement par AO sembla rendre le microenvironnement tumoral moins suppressif et plus permissif à l’attaque immunitaire. Bien que des travaux supplémentaires soient nécessaires dans des modèles plus lents et plus réalistes ainsi que sur des tissus humains, ces résultats suggèrent que cibler précisément un seul commutateur métabolique peut transformer une tumeur pancréatique résistante en une tumeur finalement réceptive à l’immunothérapie.
Citation: Han, L., Gan, L., Schäfer, B. et al. ASO-based PKM splice-switching therapy increases anti-CTLA-4 antibody efficacy in pancreatic ductal adenocarcinoma. Cell Discov 12, 28 (2026). https://doi.org/10.1038/s41421-026-00882-9
Mots-clés: cancer du pancréas, métabolisme tumoral, immunothérapie, cells T régulatrices, oligonucléotides antisens