Clear Sky Science · sv
Androgenreceptorn och fettsyreoxidering samverkar för att undvika ferroptos i BRAFi‑resistent melanom
Varför detta är viktigt för behandling av svårbehandlade hudcancerformer
Läkemedel som blockerar muterat BRAF, en viktig tillväxtomkopplare i melanom, har förändrat vården för personer med avancerad hudcancer. Ändå krymper många tumörer initialt bara för att återkomma med ny styrka efter några månader. Denna studie undersöker vad som hjälper dessa återkommande tumörer att överleva och utforskar ett nytt sätt att driva dem mot en självdestruktiv process kallad ferroptos, genom kombination av två redan godkända läkemedel för hjärta respektive prostata.
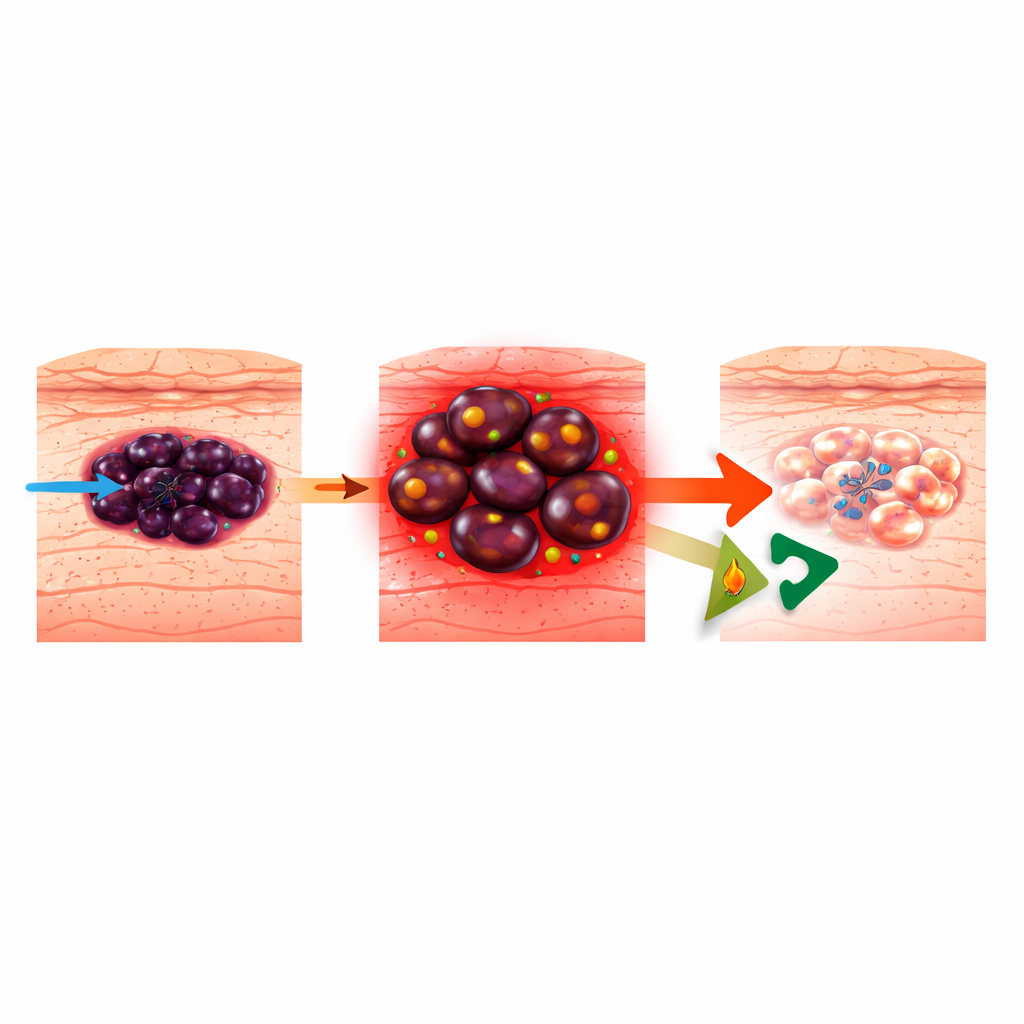
Hur melanom lär sig undvika riktade läkemedel
Melanom uppstår från pigmentbildande celler i huden och står för de flesta dödsfall i hudcancer. Moderna riktade terapier går på det överaktiva BRAF–MEK‑systemet som driver många melanom, men tumörer är anmärkningsvärt anpassningsbara. De kan växla mellan olika ”celltillstånd”, från en mer mogen pigment‑producerande identitet till ett mer primitivt, neural‑crest‑liknande eller odifferentierat tillstånd som är aggressivt och läkemedelsresistent. Tidigare arbete har visat att när melanom blir resistenta mot BRAF‑blockerande läkemedel (BRAFi) så bränner de i allt högre grad fetter i sina mitokondrier, en process kallad fettsyreoxidering (FAO). Att blockera FAO med hjärtmedicinen ranolazin var känt för att bromsa uppkomsten av resistenta celler, men hur detta faktiskt dödade melanomceller var oklart.
En dold sårbarhet: järndrivet fettangrepp
Forskarnas fokus låg på ferroptos, en form av celldöd som utlöses när järn hjälper till att skapa destruktiva kemiska reaktioner i vissa fetter i cellmembran. De fann att BRAFi‑resistenta melanomceller bär många kännetecken som lämnar dem på randen till ferroptos: de har lägre nivåer av antioxidantet glutation, fyller sina membran med långa, skadebenägna fleromättade fettsyror och visar mer oxiderade membranlipider än sina läkemedelskänsliga motsvarigheter. Patientprover från tumörer som utvecklats trots BRAF‑hämmare visade samma mönster, med markörer för både ferroptos och fettförbränningsvägar som ökade samtidigt. Detta antydde att resistenta celler balanserar på en knivsegg—mycket sårbara för järndrivet fettangrepp, men samtidigt uppbyggda för att undertrycka det.
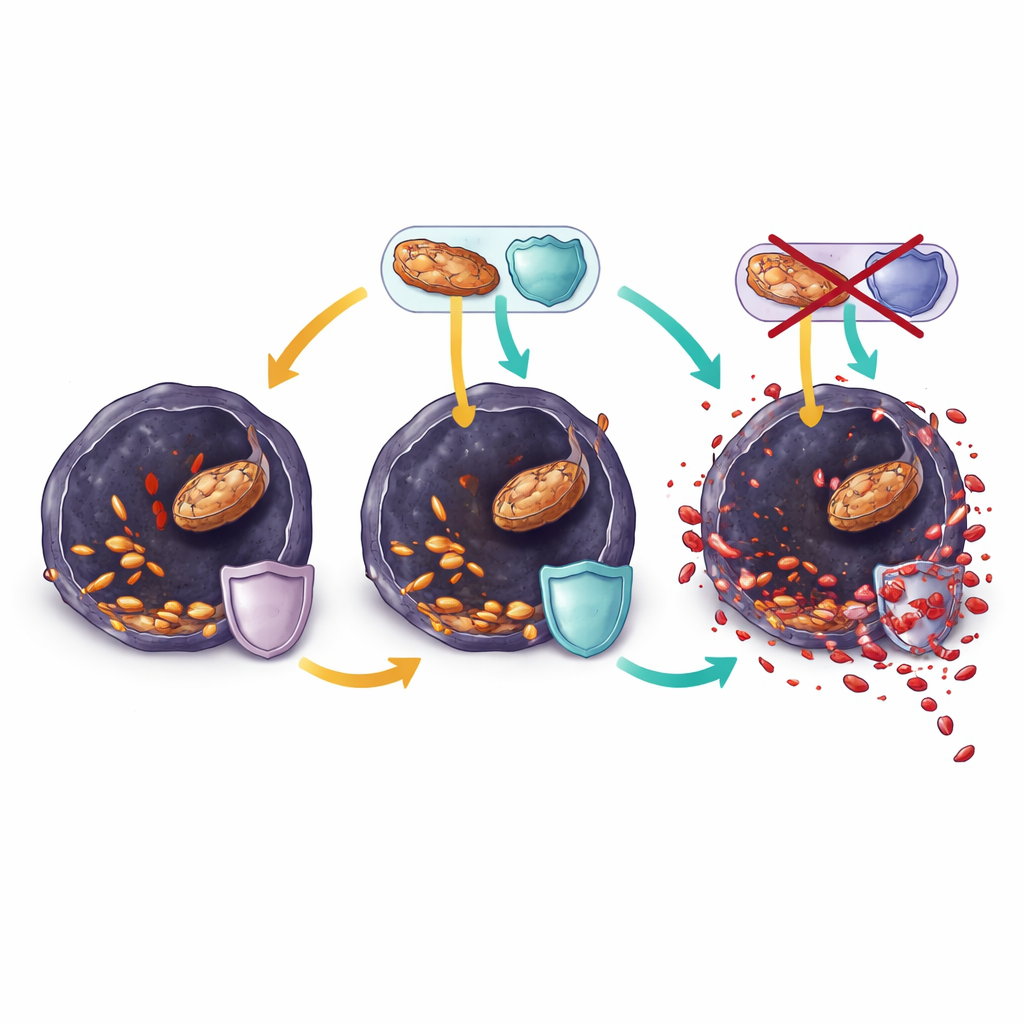
Ranolazin tippar balansen mot celldöd
I resistenta melanomceller odlade i laboratoriet minskade ranolazin snabbt fettförbränningsaktiviteten, tömde viktiga energimolekyler och sänkte ytterligare glutationnivåerna. Samtidigt ökade insättningen av fleromättade fetter i membranlipider och tecken på oxidativ stress och lipidskador steg kraftigt. Dessa förändringar bromsade celltillväxten inom timmar och kunde reverseras av klassiska ferroptoshämmare, vilket visade att ranolazin främst dödade cellerna genom att driva dem över gränsen till ferroptos. När tumörer i möss dock så småningom undkom den kombinerade behandlingen med BRAF‑hämmare och ranolazin, hade deras celler omprogrammerat sig igen. De upprätthöll höga nivåer av enzymer som reparerar oxiderade lipider och återfyller skyddande molekyler, och de omformade sina membran för att innehålla fler motståndskraftiga enkelomättade fetter istället för känsliga fleromättade.
Hormonella signaler hjälper återuppbygga tumörens försvar
Teamet spårade denna membranombyggnad till enzymerna MBOAT1 och MBOAT2, som byter in säkrare fetter vid förnyelse av fosfolipider. Dessa enzymer var starkt ökning i ranolazinresistenta celler och i många patienttumörer som recidiverat på BRAF‑hämmare. Deras aktivitet berodde på androgenreceptorn (AR), en hormonsensor som är mer känd från prostatacancer. AR band till kontrollregioner vid MBOAT1‑ och MBOAT2‑generna och ökade deras aktivitet. När forskarna blockerade AR med prostatacancerläkemedlet enzalutamid sjönk nivåerna av MBOAT1/2 och melanomceller blev betydligt mer känsliga för ferroptos‑inducerande medel. Denna effekt sågs över olika melanom‑celltillstånd, både i primitiva, mycket läkemedelsresistenta celler och i mer differentierade pigmentlika celler.
Att para ihop två gamla läkemedel för att överlista resistenta tumörer
Eftersom FAO och AR‑styrd lipidombyggnad båda hjälper melanomceller att undvika ferroptos, testade författarna om en samtidig träff på båda vore särskilt effektiv. I cellkulturer orsakade kombinationen ranolazin (som blockerar fettförbränning och ökar lipidskador) och enzalutamid (som oskadliggör AR och dess membranskyddande enzymer) omfattande ferroptotisk celldöd, särskilt i celler som var starkt beroende av FAO och hade skiftat till det aggressiva odifferentierade tillståndet. Under förhållanden som tvingar melanomceller att förlita sig mer på fett som bränsle blev denna kombination ännu dödligare. Arbetet tyder på att en dual‑terapistrategi med dessa redan godkända läkemedel både kan fördröja resistens mot BRAF‑riktade behandlingar och göra resistenta tumörer, inklusive sådana som dämpar immunangrepp, mer sårbara genom att tvinga dem in i ferroptos.
Vad detta kan innebära för patienter
Denna forskning ger en detaljerad bild av hur melanomceller, trängda i ett hörn av riktade terapier, omformar sin metabolism och hormonsignalering för att undvika en dödlig form av järn‑ och fettrelaterad celldöd. Genom att avslöja att fettförbränningsvägar och androgenreceptorn samverkar för att hålla ferroptos i schack, pekar den på ett praktiskt sätt att riva bort det skyddsnätet. Kliniska prövningar krävs, men idén att återanvända hjärt‑ och prostatamediciner tillsammans med befintliga melanombehandlingar erbjuder en lovande väg till längre varaktiga svar och potentiellt bättre utfall för patienter vars tumörer är benägna att återfalla.
Citering: Redondo-Muñoz, M., Caballe-Mestres, A., Reisz, J.A. et al. Androgen receptor and fatty acid oxidation cooperate in ferroptosis evasion in BRAFi resistant melanoma. Cell Death Dis 17, 338 (2026). https://doi.org/10.1038/s41419-026-08578-4
Nyckelord: melanom, ferroptos, fettsyreoxidering, androgenreceptor, Läkemedelsresistens