Clear Sky Science · pl
Receptor androgenowy i utlenianie kwasów tłuszczowych współpracują w unikaniu ferroptozy w melanomie opornej na inhibitory BRAF
Dlaczego to ma znaczenie dla leczenia opornych nowotworów skóry
Leki blokujące zmutowany BRAF, kluczowy przełącznik wzrostu w czerniaku, zrewolucjonizowały opiekę nad osobami z zaawansowanym rakiem skóry. Jednak wiele guzów początkowo się kurczy, by po kilku miesiącach znów gwałtownie odrosnąć. Badanie to zagłębia się w mechanizmy umożliwiające przetrwanie tych nawrotowych guzów i bada nowy sposób wymuszenia w nich trybu samobójczego zwanego ferroptozą, stosując w połączeniu dwa istniejące leki: kardiologiczny i stosowany w raku prostaty.
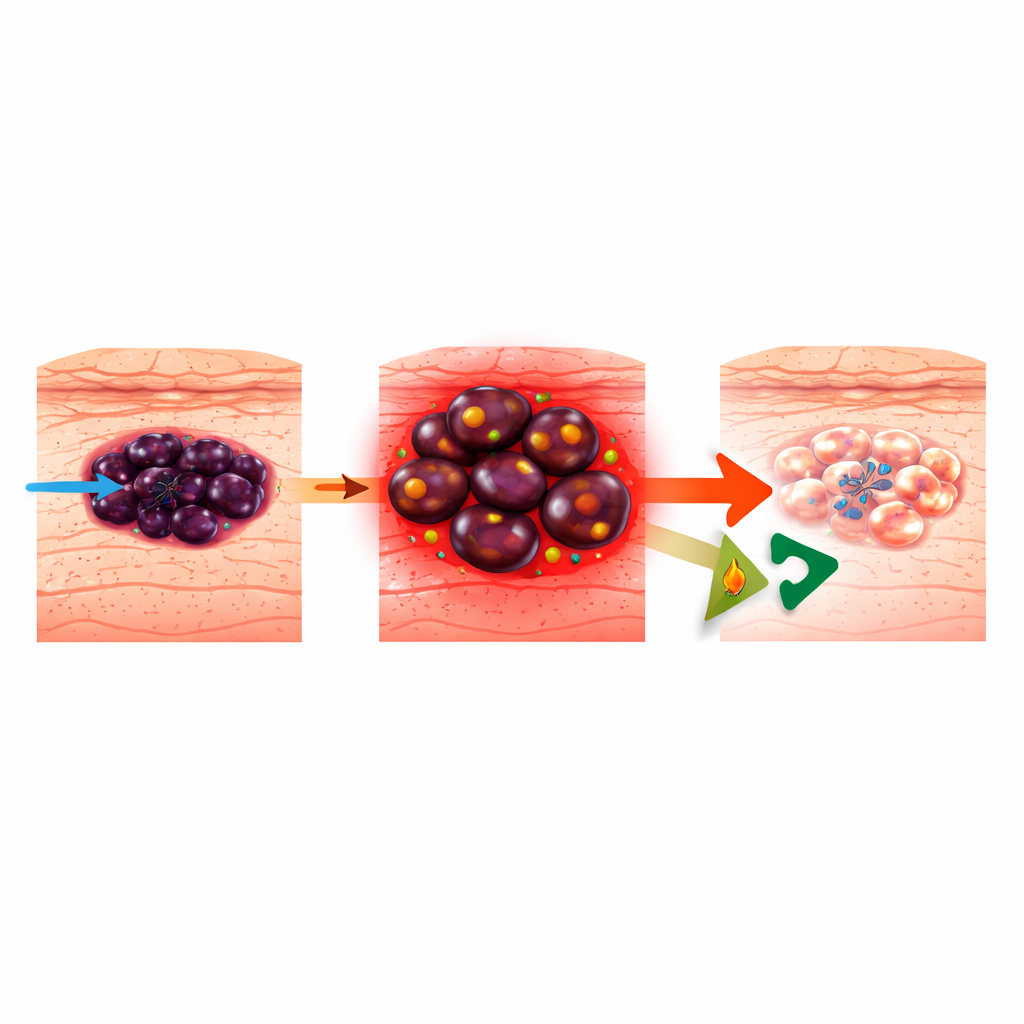
Jak czerniak uczy się unikać terapii celowanych
Czerniak powstaje z komórek produkujących barwnik w skórze i odpowiada za większość zgonów z powodu raka skóry. Nowoczesne terapie celowane uderzają w nadaktywne szlaki BRAF–MEK napędzające wiele czerniaków, ale guzy są niezwykle plastyczne. Potrafią przełączać się między różnymi „stanami komórkowymi”, od bardziej dojrzałej, produkującej pigment tożsamości, do bardziej prymitywnego, przypominającego grzebień nerwowy lub niedojrzałego stanu, który jest agresywny i odporny na leki. Wcześniejsze prace wykazały, że w miarę nabywania oporności na inhibitory BRAF (BRAFi), czerniaki coraz częściej zasilają się spalaniem tłuszczów w mitochondriach, procesem zwanym utlenianiem kwasów tłuszczowych (FAO). Blokowanie FAO lekiem stosowanym w kardiologii, ranolazyną, było znane z opóźniania wzrostu komórek opornych, ale mechanizm prowadzący do śmierci komórek czerniaka pozostawał niejasny.
Ukryta słabość: żelazem napędzane uszkodzenie tłuszczów
Naukowcy skoncentrowali się na ferroptozie, formie śmierci komórki wywoływanej, gdy żelazo sprzyja powstawaniu destrukcyjnych reakcji chemicznych w niektórych tłuszczach w błonach komórkowych. Odkryli, że komórki czerniaka odporne na BRAFi mają wiele cech wystawiających je na krawędź ferroptozy: niższe poziomy antyoksydacyjnej glutationu, błony bogate w długie, łatwo ulegające uszkodzeniu wielonienasycone kwasy tłuszczowe oraz wyższe stężenia zoksydowanych lipidów błonowych niż komórki wrażliwe na leki. Próbki guzów od pacjentów, u których choroba postępowała mimo inhibitorów BRAF, pokazały ten sam wzorzec — markery zarówno ferroptozy, jak i szlaków spalania tłuszczów rosły równocześnie. Sugerowało to, że komórki oporne balansują na cienkiej linii — silnie narażone na żelazozależne uszkodzenie tłuszczów, a jednocześnie wyposażone w mechanizmy, które to tłumiają.
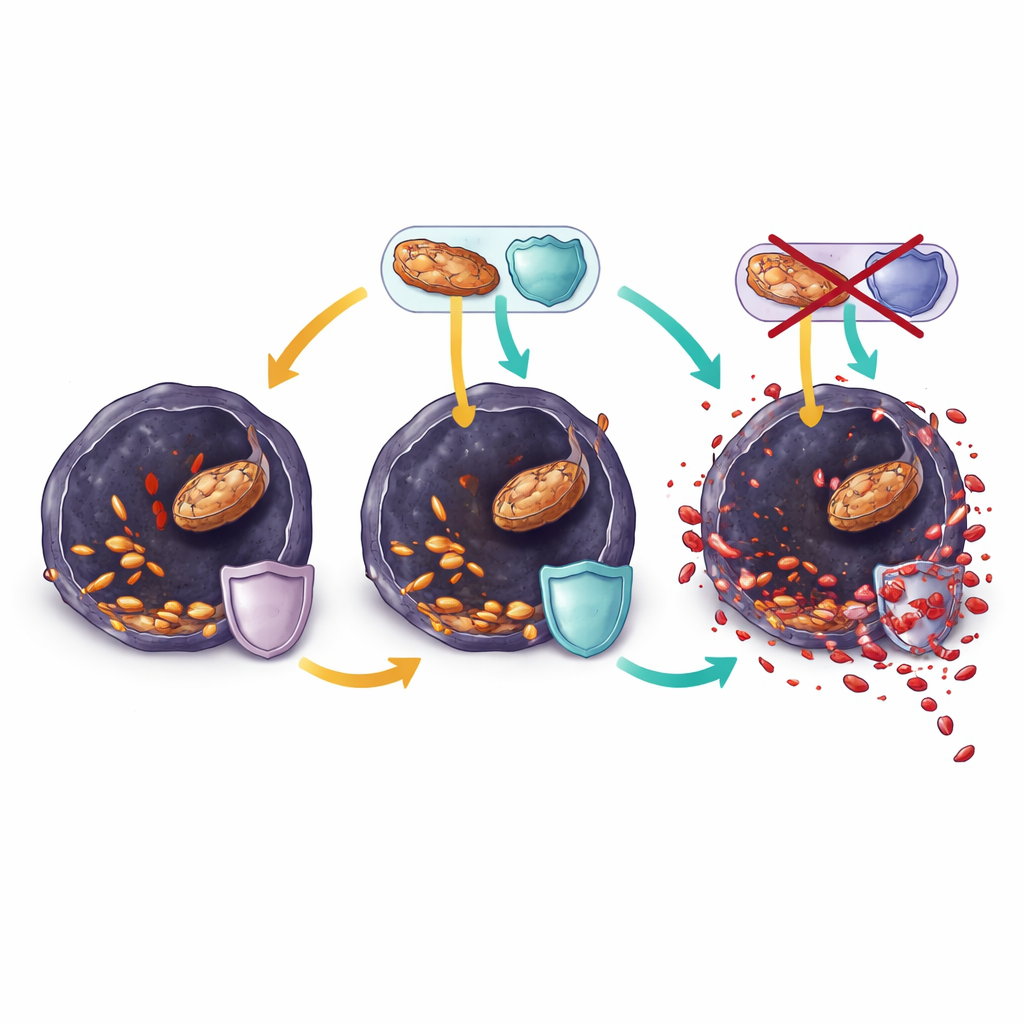
Ranolazyna przechyla szalę w kierunku śmierci komórki
W hodowlach komórkowych opornych komórek czerniaka ranolazyna szybko obniżała aktywność spalania tłuszczów, wyczerpywała kluczowe cząsteczki energetyczne i dodatkowo zmniejszała poziomy glutationu. Równocześnie do błon włączano więcej wielonienasyconych kwasów tłuszczowych, a oznaki stresu oksydacyjnego i uszkodzeń lipidów gwałtownie wzrastały. Zmiany te hamowały wzrost komórek w ciągu kilku godzin i można je było odwrócić klasycznymi blokerami ferroptozy, co wskazywało, że ranolazyna zabija komórki głównie poprzez pchnięcie ich za próg ferroptozy. Jednak gdy guzy u myszy ostatecznie wymykały się skojarzonej terapii BRAF i ranolazyną, ich komórki ponownie się przestawiły. Utrzymywały wysokie poziomy enzymów naprawiających zoksydowane lipidy i uzupełniających cząsteczki ochronne oraz przebudowywały błony, zawierając więcej odpornego jednonienasyconego tłuszczu zamiast podatnych wielonienasyconych kwasów.
Sygnały hormonalne pomagają odbudować obronę guza
Zespół przypisał tę przebudowę błon enzymom MBOAT1 i MBOAT2, które w czasie odnawiania fosfolipidów wymieniają na bezpieczniejsze kwasy tłuszczowe. Enzymy te były silnie zwiększone w komórkach opornych na ranolazynę i w wielu próbkach guzów pacjentów, którzy nawroty przeszli pomimo inhibitorów BRAF. Ich aktywność zależała od receptora androgenowego (AR), czujnika hormonalnego bardziej znanego z raka prostaty. AR wiązał się z regionami kontrolnymi genów MBOAT1 i MBOAT2 i zwiększał ich ekspresję. Gdy badacze zablokowali AR lekiem stosowanym w raku prostaty, enzalutamidem, poziomy MBOAT1/2 spadły, a komórki czerniaka stały się znacznie bardziej wrażliwe na środki wywołujące ferroptozę. Efekt ten obserwowano w różnych stanach komórkowych czerniaka, zarówno w prymitywnych, silnie opornych komórkach, jak i w bardziej zróżnicowanych, pigmentopodobnych komórkach.
Połączenie dwóch starych leków, by przechytrzyć oporne guzy
Ponieważ FAO i kontrolowana przez AR przebudowa lipidów każdy z osobna pomagały komórkom czerniaka unikać ferroptozy, autorzy sprawdzili, czy równoczesne uderzenie w oba szlaki będzie szczególnie skuteczne. W hodowli komórek połączenie ranolazyny (blokującej spalanie tłuszczów i zwiększającej uszkodzenia lipidów) z enzalutamidem (unieszkodliwiającym AR i jego enzymy chroniące błony) wywołało rozległą śmierć ferroptotyczną, zwłaszcza w komórkach mocno zależnych od FAO i przełączonych w agresywny, niedojrzały stan. W warunkach zmuszających komórki czerniaka do większej zależności od tłuszczu jako paliwa, to połączenie było jeszcze bardziej zabójcze. Praca sugeruje, że strategia terapii podwójnej przy użyciu już zatwierdzonych leków mogłaby zarówno opóźnić rozwój oporności na terapie celowane przeciw BRAF, jak i uczynić guzy oporne — w tym te osłabiające odpowiedź immunologiczną — bardziej podatnymi przez wymuszenie ferroptozy.
Co to może znaczyć dla pacjentów
Badania te przedstawiają szczegółowy obraz tego, jak komórki czerniaka, zepchnięte w narożnik terapią celowaną, przekształcają swój metabolizm i sygnalizację hormonalną, by uniknąć śmierci komórki zależnej od żelaza i tłuszczów. Ujawniając, że szlaki spalania tłuszczów i receptor androgenowy współdziałają, by powstrzymać ferroptozę, wskazują praktyczny sposób na usunięcie tej sieci bezpieczeństwa. Choć konieczne będą badania kliniczne, koncepcja ponownego zastosowania leków sercowych i przeciwko rakowi prostaty obok istniejących terapii czerniaka oferuje obiecującą drogę do dłużej utrzymujących się odpowiedzi i potencjalnie lepszych wyników dla pacjentów, których guzy mają skłonność do nawrotów.
Cytowanie: Redondo-Muñoz, M., Caballe-Mestres, A., Reisz, J.A. et al. Androgen receptor and fatty acid oxidation cooperate in ferroptosis evasion in BRAFi resistant melanoma. Cell Death Dis 17, 338 (2026). https://doi.org/10.1038/s41419-026-08578-4
Słowa kluczowe: czerniak, ferroptoza, utlenianie kwasów tłuszczowych, receptor androgenowy, oporność na leki