Clear Sky Science · fr
Le récepteur des androgènes et l’oxydation des acides gras coopèrent pour échapper à la ferroptose dans le mélanome résistant aux inhibiteurs de BRAF
Pourquoi cela compte pour le traitement des cancers de la peau difficiles
Les médicaments qui bloquent la BRAF mutée, un interrupteur clé de croissance dans le mélanome, ont transformé la prise en charge des personnes atteintes de cancers cutanés avancés. Pourtant, de nombreuses tumeurs rétrécissent d’abord puis repoussent quelques mois plus tard. Cette étude explore ce qui permet à ces tumeurs récurrentes de survivre et examine une nouvelle façon de les pousser vers un mode d’autodestruction appelé ferroptose, en combinant deux médicaments déjà utilisés pour des maladies cardiaques et prostatiques.
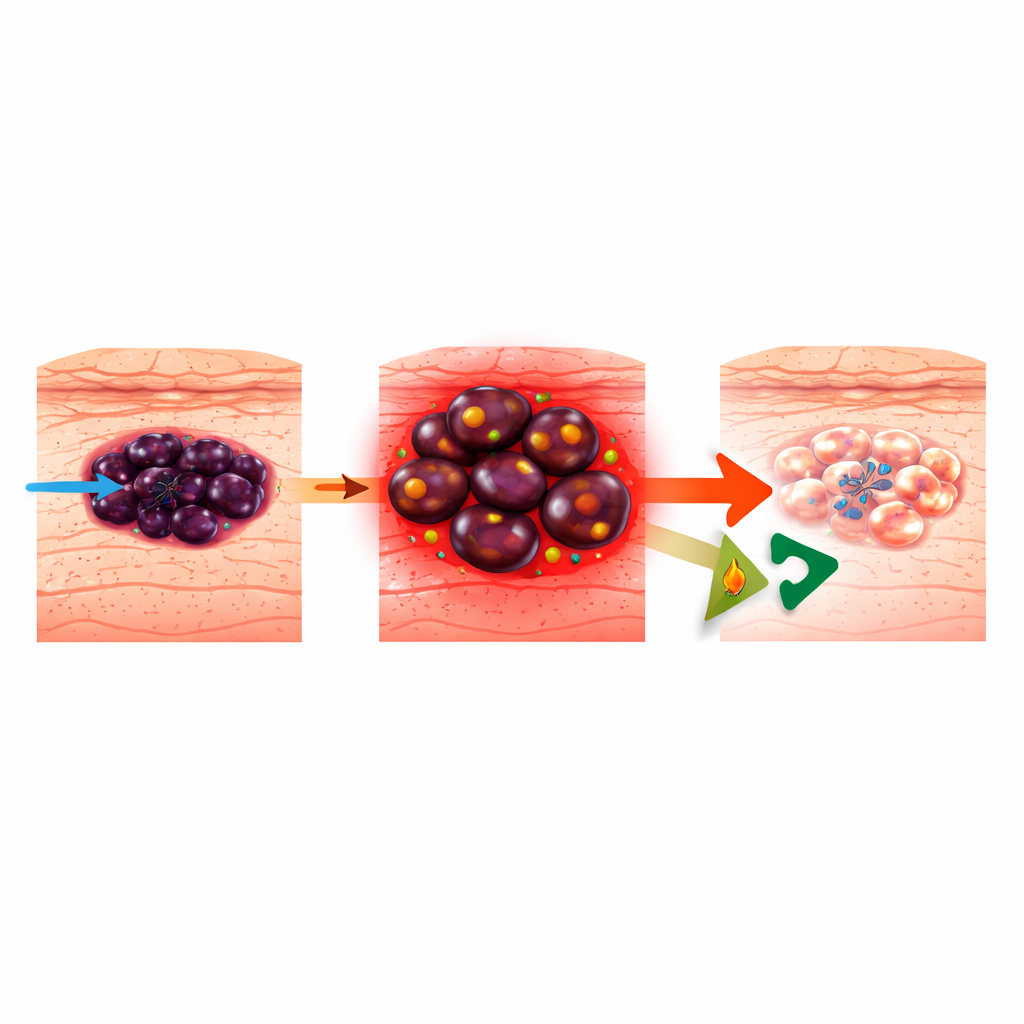
Comment le mélanome apprend à esquiver les thérapies ciblées
Le mélanome provient des cellules productrices de pigments de la peau et est responsable de la majorité des décès par cancer cutané. Les thérapies ciblées modernes attaquent la voie BRAF–MEK hyperactive qui alimente de nombreux mélanomes, mais les tumeurs sont remarquablement adaptables. Elles peuvent basculer entre différents « états cellulaires », d’une identité plus mature productrice de pigments à un état plus primitif, de type crête neurale ou indifférencié, qui est agressif et résistant aux médicaments. Des travaux antérieurs ont montré qu’à mesure que les mélanomes deviennent résistants aux inhibiteurs de BRAF (BRAFi), ils s’alimentent de plus en plus en brûlant des graisses dans leurs mitochondries, un processus appelé oxydation des acides gras (FAO). Bloquer la FAO avec le médicament cardiaque ranolazine ralentissait l’essor des cellules résistantes, mais le mécanisme exact de leur mort restait flou.
Une vulnérabilité cachée : dommages lipidiques pilotés par le fer
Les chercheurs se sont focalisés sur la ferroptose, une forme de mort cellulaire déclenchée lorsque le fer favorise des réactions chimiques destructrices au sein de certains lipides des membranes cellulaires. Ils ont constaté que les cellules de mélanome résistantes aux BRAFi présentent de nombreux traits qui les placent au bord de la ferroptose : elles ont des niveaux réduits du puissant antioxydant glutathion, leurs membranes sont enrichies en acides gras polyinsaturés longs et susceptibles d’être endommagés, et elles montrent plus de lipides membranaires oxydés que leurs homologues sensibles au traitement. Des échantillons tumoraux de patients ayant progressé sous inhibiteurs de BRAF montraient le même schéma, avec une augmentation conjointe des marqueurs de la ferroptose et des voies de combustion des graisses. Cela suggère que les cellules résistantes marchent sur une corde raide — très vulnérables aux dommages lipidiques induits par le fer, tout en étant simultanément câblées pour les réprimer.
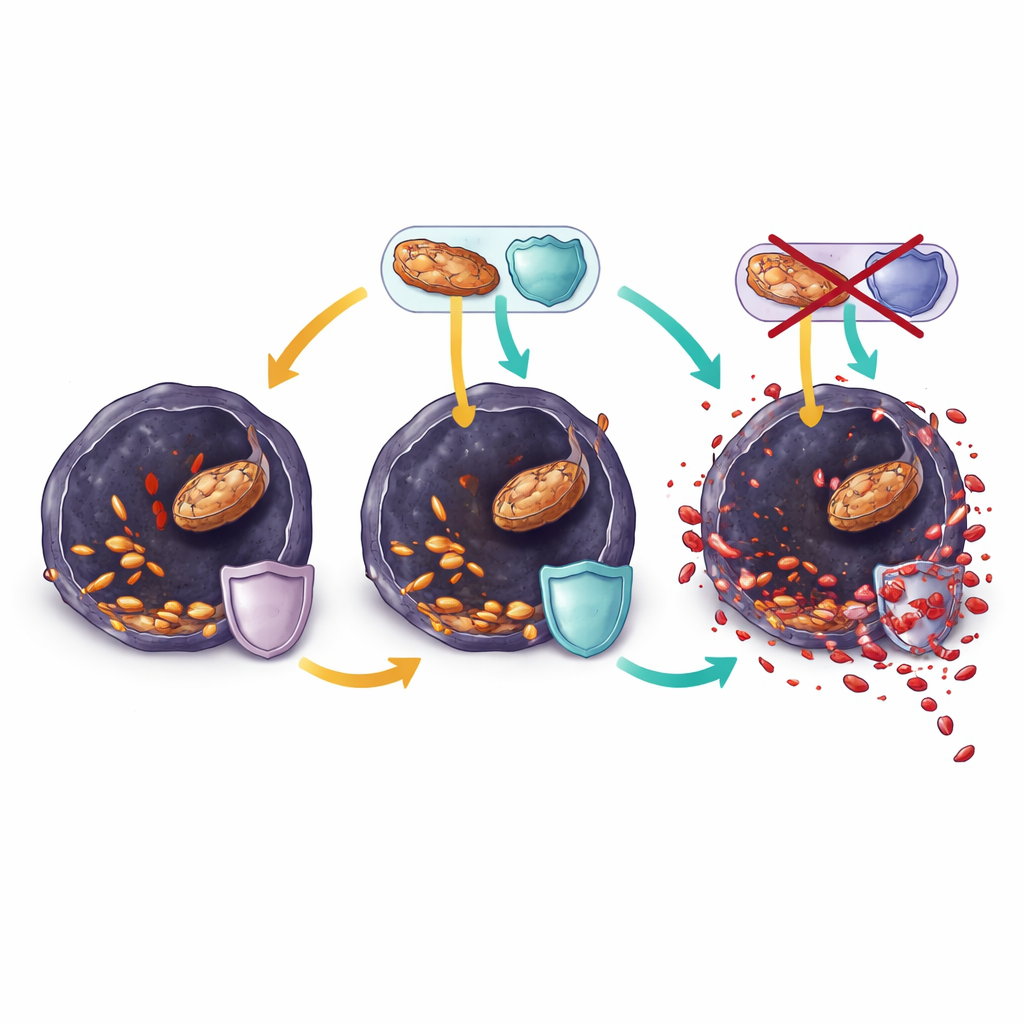
La ranolazine fait pencher la balance vers la mort cellulaire
In vitro, dans des cellules de mélanome résistantes cultivées en laboratoire, la ranolazine réduisait rapidement l’activité de combustion des graisses, vidait des molécules énergétiques clés et abaissait encore le glutathion. Parallèlement, davantage d’acides gras polyinsaturés étaient incorporés dans les phospholipides membranaires, et les signes de stress oxydatif et de dommages lipidiques augmentaient fortement. Ces changements ralentissaient la croissance cellulaire en quelques heures et pouvaient être inversés par des bloqueurs classiques de la ferroptose, montrant que la ranolazine tuait principalement les cellules en les poussant au-delà du seuil de ferroptose. Cependant, quand des tumeurs chez la souris échappaient finalement au traitement combiné BRAF + ranolazine, leurs cellules s’étaient reprogrammées à nouveau. Elles maintenaient des niveaux élevés d’enzymes réparant les lipides oxydés et renouvelant les molécules protectrices, et remodelaient leurs membranes pour contenir davantage d’acides gras monoinsaturés résistants plutôt que d’acides gras polyinsaturés vulnérables.
Les signaux hormonaux aident à reconstruire les défenses tumorales
L’équipe a relié ce remodelage membranaire à des enzymes appelées MBOAT1 et MBOAT2, qui remplacent les lipides par des graisses plus sûres lors du renouvellement des phospholipides. Ces enzymes étaient fortement augmentées dans les cellules résistantes à la ranolazine et dans de nombreuses tumeurs de patients ayant rechuté sous inhibiteurs de BRAF. Leur activité dépendait du récepteur des androgènes (AR), un senseur hormonal mieux connu dans le cancer de la prostate. L’AR se liait aux régions de contrôle des gènes MBOAT1 et MBOAT2 et stimulait leur expression. Lorsque les chercheurs bloquaient l’AR avec l’anti-androgène utilisé en prostate, l’enzalutamide, les niveaux de MBOAT1/2 chutaient et les cellules de mélanome devenaient beaucoup plus sensibles aux agents induisant la ferroptose. Cet effet était visible dans différents états cellulaires du mélanome, tant dans les cellules primitives, fortement résistantes, que dans les cellules plus différenciées ressemblant à des cellules productrices de pigments.
Associer deux vieux médicaments pour déjouer les tumeurs résistantes
Parce que la FAO et le remodelage lipidique contrôlé par l’AR aident chacun à faire échec à la ferroptose, les auteurs ont testé si cibler les deux simultanément serait particulièrement efficace. En culture cellulaire, la combinaison de la ranolazine (qui bloque la combustion des graisses et accentue les dommages lipidiques) et de l’enzalutamide (qui neutralise l’AR et ses enzymes protectrices de la membrane) provoquait une mort cellulaire ferroptotique extensive, surtout dans les cellules fortement dépendantes de la FAO et passées à l’état indifférencié agressif. Dans des conditions forçant les cellules de mélanome à dépendre davantage des lipides comme carburant, cette combinaison devenait encore plus létale. Ces résultats suggèrent qu’une stratégie thérapeutique double utilisant ces médicaments déjà approuvés pourrait à la fois retarder l’apparition de la résistance aux traitements ciblant BRAF et rendre les tumeurs résistantes, y compris celles qui atténuent l’attaque immunitaire, plus vulnérables en les forçant dans la ferroptose.
Ce que cela pourrait signifier pour les patients
Cette recherche dresse un panorama détaillé de la façon dont les cellules de mélanome, acculées par une thérapie ciblée, remodèlent leur métabolisme et leur signalisation hormonale pour éviter une forme mortelle de mort cellulaire basée sur le fer et les lipides. En révélant que les voies de combustion des graisses et le récepteur des androgènes coopèrent pour maintenir la ferroptose sous contrôle, elle pointe une voie pratique pour supprimer ce filet de sécurité. Si des essais cliniques seront nécessaires, l’idée de réutiliser des médicaments cardiaques et prostatiques en association avec les traitements actuels du mélanome offre une piste prometteuse pour des réponses plus durables et potentiellement de meilleurs résultats pour les patients dont les tumeurs ont tendance à rechuter.
Citation: Redondo-Muñoz, M., Caballe-Mestres, A., Reisz, J.A. et al. Androgen receptor and fatty acid oxidation cooperate in ferroptosis evasion in BRAFi resistant melanoma. Cell Death Dis 17, 338 (2026). https://doi.org/10.1038/s41419-026-08578-4
Mots-clés: mélanome, ferroptose, oxydation des acides gras, récepteur des androgènes, résistance aux médicaments