Clear Sky Science · pt
Receptor de andrógeno e oxidação de ácidos graxos cooperam na evasão da ferroptose em melanoma resistente a BRAFi
Por que isso importa para tratar cânceres de pele persistentes
Medicamentos que bloqueiam BRAF mutante, um interruptor de crescimento chave no melanoma, transformaram o tratamento de pessoas com câncer de pele avançado. Ainda assim, muitos tumores encolhem inicialmente apenas para voltar com força meses depois. Este estudo investiga o que ajuda esses tumores de retorno a permanecerem vivos e explora uma nova maneira de empurrá-los a um modo de autodestruição chamado ferroptose, usando em combinação dois medicamentos já aprovados para coração e próstata.
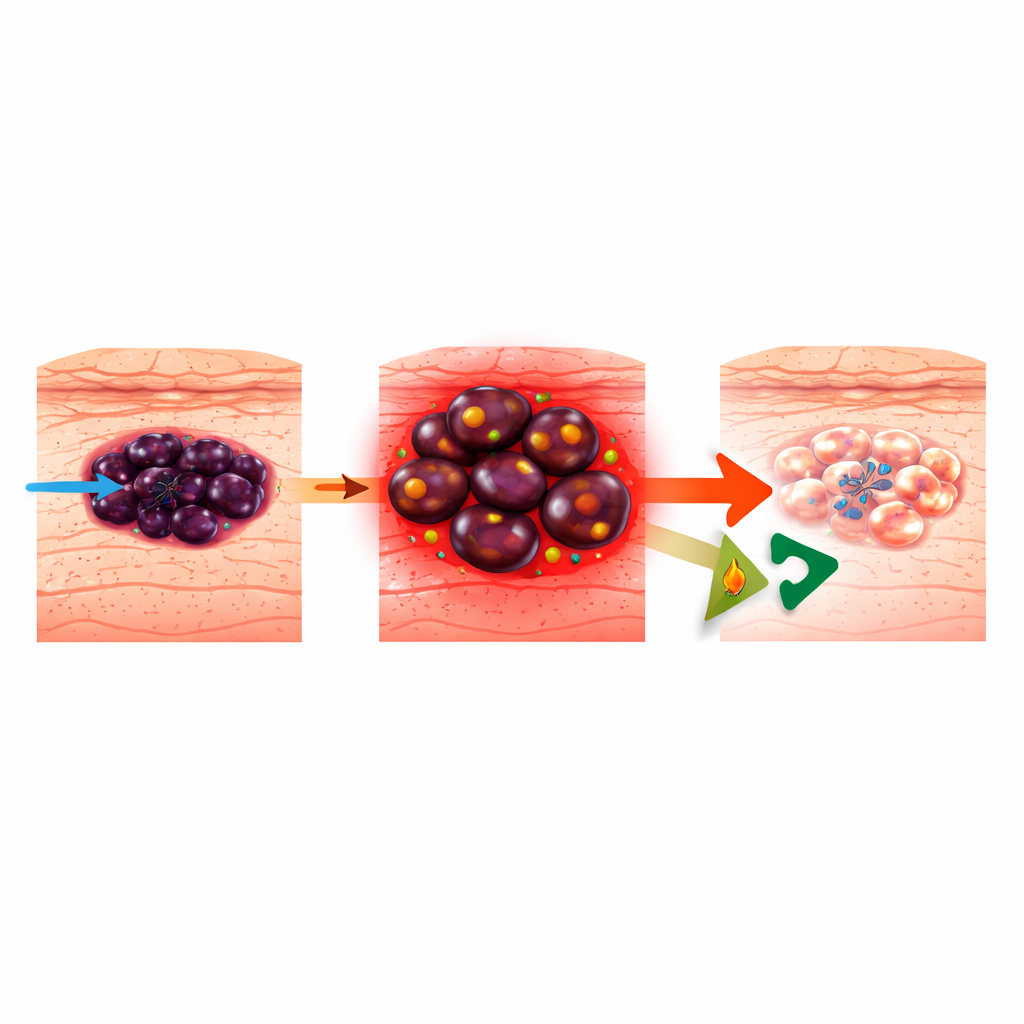
Como o melanoma aprende a driblar drogas alvo
O melanoma surge de células produtoras de pigmento na pele e é responsável pela maioria das mortes por câncer de pele. As terapias alvo modernas atacam a via BRAF–MEK hiperativa que impulsiona muitos melanomas, mas os tumores são notavelmente adaptáveis. Podem alternar entre diferentes “estados celulares”, de uma identidade mais madura de produção de pigmento para um estado mais primitivo, semelhante à crista neural ou indiferenciado, que é agressivo e resistente a medicamentos. Trabalhos anteriores mostraram que, à medida que os melanomas se tornam resistentes aos bloqueadores de BRAF (BRAFi), eles cada vez mais se abastecem queimando gorduras nas mitocôndrias, um processo chamado oxidação de ácidos graxos (FAO). Bloquear a FAO com o medicamento cardíaco ranolazina já havia mostrado retardar a ascensão de células resistentes, mas não estava claro como isso realmente matava as células do melanoma.
Uma vulnerabilidade oculta: dano lipídico impulsionado por ferro
Os pesquisadores focaram na ferroptose, uma forma de morte celular desencadeada quando o ferro ajuda a gerar reações químicas destrutivas em certas gorduras dentro das membranas celulares. Eles descobriram que as células de melanoma resistentes a BRAFi exibem muitas características que as deixam à beira da ferroptose: apresentam níveis mais baixos do antioxidante glutationa, empilham suas membranas com gorduras poli-insaturadas longas e suscetíveis a danos, e mostram mais lipídios de membrana oxidados do que suas contrapartes sensíveis ao medicamento. Amostras de tumores de pacientes que progrediram durante inibidores de BRAF mostraram o mesmo padrão, com marcadores tanto de ferroptose quanto de vias de queima de gordura aumentando juntos. Isso sugeriu que as células resistentes caminham em uma corda bamba — altamente vulneráveis ao dano lipídico mediado por ferro, mas simultaneamente configuradas para suprimí-lo.
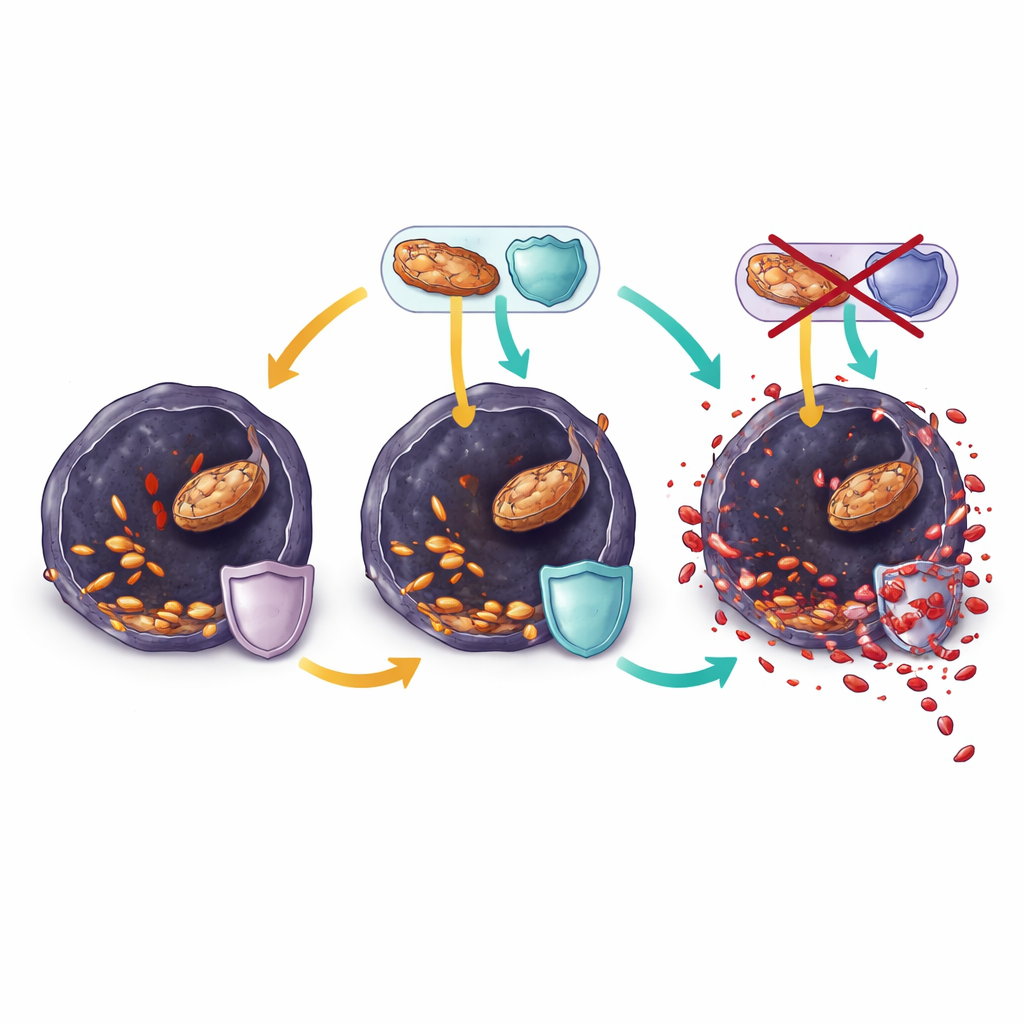
Ranolazina inclina a balança em direção à morte celular
Em células de melanoma resistentes cultivadas em laboratório, a ranolazina reduziu rapidamente a atividade de queima de gordura, esgotou moléculas energéticas essenciais e reduziu ainda mais a glutationa. Ao mesmo tempo, mais gorduras poli-insaturadas foram incorporadas aos lipídios de membrana, e sinais de estresse oxidativo e dano lipídico aumentaram. Essas mudanças desaceleraram o crescimento celular em poucas horas e puderam ser revertidas por bloqueadores clássicos de ferroptose, mostrando que a ranolazina matava as células principalmente ao empurrá-las para a ferroptose. Porém, quando tumores em camundongos eventualmente escaparam do tratamento combinado com BRAF e ranolazina, suas células haviam se reconfigurado novamente. Mantinham altos níveis de enzimas que reparam lipídios oxidados e reabastecem moléculas protetoras, e remodelaram suas membranas para conter mais gorduras monoinsaturadas resistentes em vez das poli-insaturadas vulneráveis.
Sinais hormonais ajudam a reconstruir as defesas do tumor
A equipe rastreou essa remodelação de membrana até enzimas chamadas MBOAT1 e MBOAT2, que trocam por gorduras mais seguras durante a renovação de fosfolipídios. Essas enzimas estavam fortemente aumentadas em células resistentes à ranolazina e em muitos tumores de pacientes que haviam recidivado com inibidores de BRAF. Sua atividade dependia do receptor de andrógeno (AR), um sensor hormonal mais conhecido no câncer de próstata. O AR ligava-se a regiões de controle dos genes MBOAT1 e MBOAT2 e aumentava sua atividade. Quando os pesquisadores bloquearam o AR com o medicamento para câncer de próstata enzalutamida, os níveis de MBOAT1/2 caíram e as células de melanoma ficaram muito mais sensíveis a agentes que induzem ferroptose. Esse efeito foi observado em diferentes estados celulares do melanoma, incluindo tanto células primitivas e altamente resistentes a medicamentos quanto células mais diferenciadas semelhantes a pigmento.
Combinar dois medicamentos antigos para superar tumores resistentes
Porque a FAO e a remodelação lipídica controlada pelo AR ajudam cada uma a escapar da ferroptose, os autores testaram se atingir ambas ao mesmo tempo seria particularmente eficaz. Em cultura celular, a combinação de ranolazina (que bloqueia a queima de gordura e aumenta o dano lipídico) com enzalutamida (que desarma o AR e suas enzimas protetoras de membrana) causou extensa morte celular ferroptótica, especialmente em células que dependiam fortemente da FAO e haviam mudado para o estado indiferenciado agressivo. Sob condições que forçam as células de melanoma a depender mais de gordura como combustível, essa combinação tornou-se ainda mais letal. O trabalho sugere que uma estratégia de dupla terapia usando esses medicamentos já aprovados poderia tanto atrasar a resistência aos tratamentos direcionados a BRAF quanto tornar tumores resistentes, incluindo aqueles que blateiam o ataque imune, mais vulneráveis ao forçá-los à ferroptose.
O que isso pode significar para pacientes
Esta pesquisa descreve em detalhe como células de melanoma, encurraladas pela terapia alvo, remodelam seu metabolismo e sinalização hormonal para escapar de uma forma letal de morte celular baseada em ferro e gordura. Ao revelar que vias de queima de gordura e o receptor de andrógeno cooperam para manter a ferroptose sob controle, aponta para um caminho prático para retirar essa rede de segurança. Embora testes clínicos sejam necessários, a ideia de reutilizar medicamentos para coração e próstata juntamente com tratamentos existentes para melanoma oferece uma rota promissora para respostas mais duradouras e possivelmente melhores resultados para pacientes cujos tumores tendem a recidivar.
Citação: Redondo-Muñoz, M., Caballe-Mestres, A., Reisz, J.A. et al. Androgen receptor and fatty acid oxidation cooperate in ferroptosis evasion in BRAFi resistant melanoma. Cell Death Dis 17, 338 (2026). https://doi.org/10.1038/s41419-026-08578-4
Palavras-chave: melanoma, ferroptose, oxidação de ácidos graxos, receptor de andrógeno, resistência a medicamentos