Clear Sky Science · nl
Androgeenreceptor en vetzuuroxidatie werken samen bij het ontwijken van ferroptose in BRAFi-resistente melanoom
Waarom dit belangrijk is voor de behandeling van hardnekkige huidkankers
Geneesmiddelen die de gemuteerde BRAF blokkeren, een belangrijke groeischakel in melanoom, hebben de zorg voor mensen met gevorderde huidkanker veranderd. Toch krimpen veel tumoren aanvankelijk slechts om maanden later weer terug te komen. Deze studie onderzoekt wat die teruggekeerde tumoren helpt overleven en verkent een nieuwe manier om ze in een zelfdestructiemodus, ferroptose genoemd, te duwen door twee bestaande hart- en prostaatmiddelen in combinatie te gebruiken.
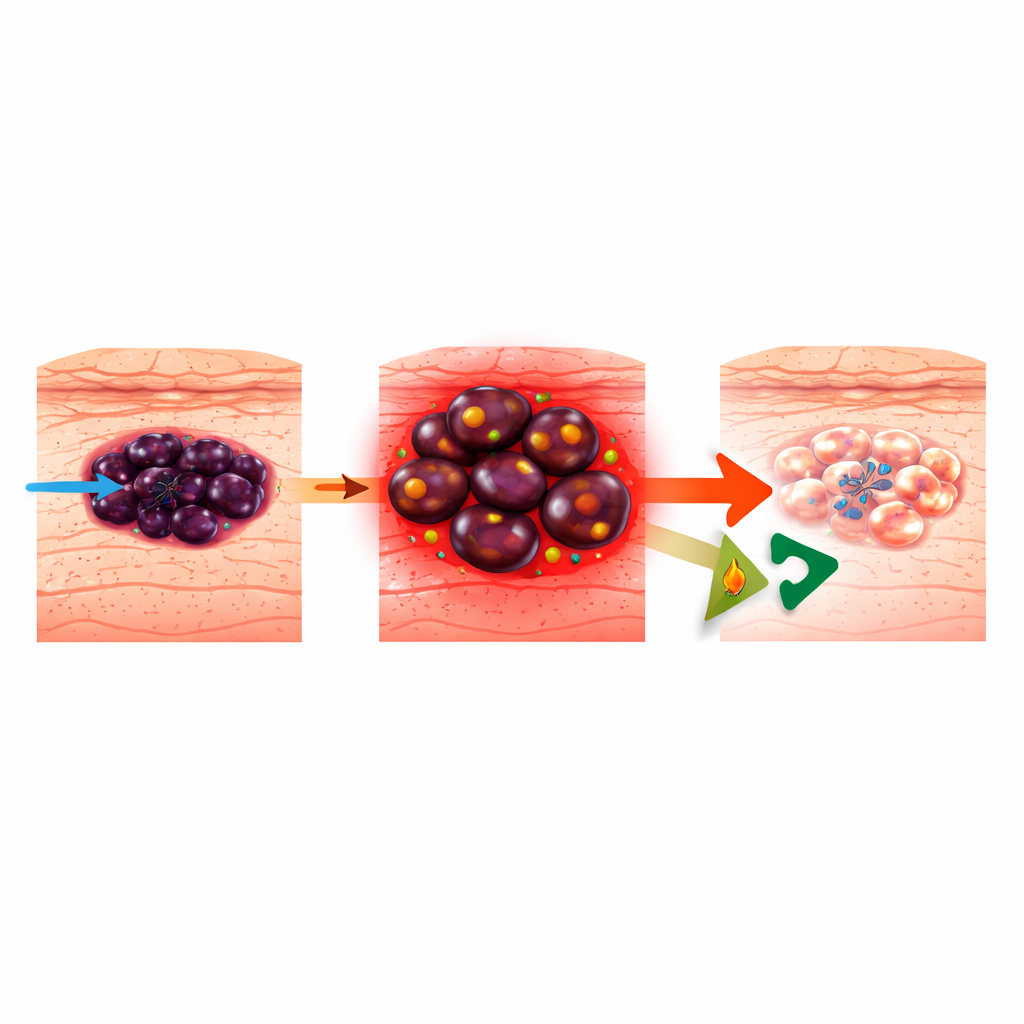
Hoe melanoom leert gerichte medicijnen te ontwijken
Melanoom ontstaat uit pigmentproducerende cellen in de huid en is verantwoordelijk voor de meeste sterfgevallen door huidkanker. Moderne gerichte therapieën richten zich op het overactieve BRAF–MEK-pad dat veel melanomen aandrijft, maar tumoren zijn buitengewoon aanpasbaar. Ze kunnen schakelen tussen verschillende “celtoestanden”, van een meer rijpe, pigmentproducerende identiteit naar een meer primitieve, neural-crest-achtige of ongedifferentieerde staat die agressief en medicijnresistent is. Eerder werk toonde aan dat wanneer melanomen resistent worden tegen BRAF-blokkerende middelen (BRAFi), ze zichzelf steeds meer voeden door vetten in hun mitochondriën te verbranden, een proces dat vetzuuroxidatie (FAO) wordt genoemd. FAO blokkeren met het hartmedicijn ranolazine bleek de opkomst van resistente cellen te vertragen, maar hoe dit precies melanoomcellen doodde, was onduidelijk.
Een verborgen kwetsbaarheid: door ijzer aangedane vetten
De onderzoekers richtten zich op ferroptose, een vorm van celdood die wordt getriggerd wanneer ijzer destructieve chemische reacties op bepaalde vetten in celmembranen helpt genereren. Ze ontdekten dat BRAFi-resistente melanoomcellen veel kenmerken dragen die hen op de rand van ferroptose zetten: ze hebben lagere niveaus van het antioxidant glutathion, vullen hun membranen met lange, schadegevoelige meervoudig onverzadigde vetten, en tonen meer geoxideerde membraanlipiden dan hun medicijngevoelige tegenhangers. Patiëntentumormonsters die waren gevorderd tijdens behandeling met BRAF-remmers lieten hetzelfde patroon zien, met markers van zowel ferroptose als vetverbrandingspaden die gelijktijdig toenamen. Dit suggereerde dat resistente cellen op een slappe koord lopen—ze zijn sterk kwetsbaar voor door ijzer aangedane vetten, maar tegelijk bekabeld om dit onderdrukken.
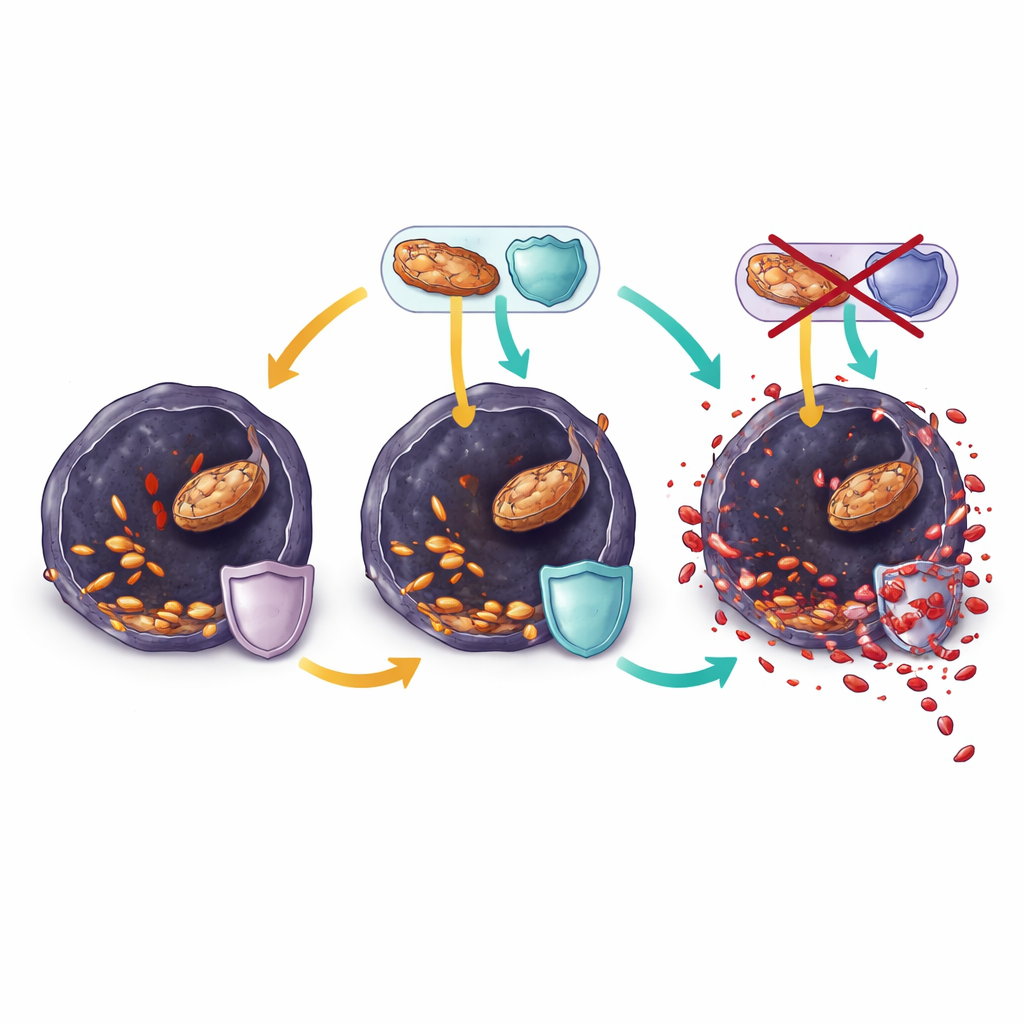
Ranolazine kantelt de balans naar celdood
In resistente melanoomcellen gekweekt in het laboratorium verminderde ranolazine snel de vetverbrandingsactiviteit, putte het belangrijke energiemoleculen uit en verlaagde het verder glutathion. Tegelijkertijd werden meer meervoudig onverzadigde vetten ingebouwd in membraanlipiden en namen tekenen van oxidatieve stress en lipideschade toe. Deze veranderingen vertraagden de celdeling binnen enkele uren en konden worden teruggedraaid met klassieke ferroptoseblokkers, wat laat zien dat ranolazine cellen voornamelijk doodde door ze over de rand in ferroptose te duwen. Wanneer tumoren in muizen uiteindelijk echter ontkwamen aan gecombineerde BRAF- en ranolazinebehandeling, hadden hun cellen zich opnieuw bekabeld. Ze behielden hoge niveaus van enzymen die geoxideerde lipiden herstellen en beschermende moleculen aanvullen, en herstructureerden hun membranen om meer resistente enkelvoudig onverzadigde vetten te bevatten in plaats van kwetsbare meervoudig onverzadigde vetten.
Hormonale signalen helpen de verdediging van de tumor herbouwen
Het team bracht deze membraanherstructurering terug tot enzymen genaamd MBOAT1 en MBOAT2, die tijdens fosfolipidenvernieuwing veiligere vetten inzetten. Deze enzymen waren sterk verhoogd in ranolazine-resistente cellen en in veel patiëntentumoren die waren teruggevallen op BRAF-remmers. Hun activiteit hing af van de androgeenreceptor (AR), een hormoonsensor die bekender is uit prostaatkanker. AR bond aan controlegebieden van de MBOAT1- en MBOAT2-genen en versterkte hun activiteit. Toen de onderzoekers AR blokkeerden met het prostaatkankermedicijn enzalutamide, daalden de niveaus van MBOAT1/2 en werden melanoomcellen veel gevoeliger voor ferroptose-inducerende middelen. Dit effect werd gezien in verschillende melanoomceltoestanden, zowel in primitieve, hoog resistente cellen als in meer gedifferentieerde pigmentachtige cellen.
Twee oude medicijnen combineren om resistente tumoren te slim af te zijn
Aangezien FAO en AR-gestuurde lipidenherstructurering elk melanoomcellen helpen ferroptose te ontlopen, testten de auteurs of het tegelijk aanvallen van beide bijzonder effectief zou zijn. In celkweek veroorzaakte de combinatie van ranolazine (dat vetverbranding blokkeert en lipideschade versterkt) met enzalutamide (dat AR en zijn membraanbeschermende enzymen uitschakelt) uitgebreide ferroptotische celdood, vooral in cellen die zwaar op FAO vertrouwden en waren overgegaan naar de agressieve ongedifferentieerde staat. Onder omstandigheden die melanoomcellen dwingen meer op vet als brandstof te vertrouwen, werd deze combinatie nog dodelijker. Het werk suggereert dat een dubbele-therapiestrategie met deze al goedgekeurde middelen zowel de resistentie tegen BRAF-gerichte behandelingen kan vertragen als resistente tumoren, inclusief diegenen die immuunaanvallen afzwakken, vatbaarder kan maken door ze in ferroptose te dwingen.
Wat dit voor patiënten kan betekenen
Dit onderzoek schetst een gedetailleerd beeld van hoe melanoomcellen, in het nauw gedreven door gerichte therapie, hun metabolisme en hormoonsignaalroutes herschikken om een dodelijke vorm van ijzer- en vetgebaseerde celdood te ontlopen. Door te onthullen dat vetverbrandingsroutes en de androgeenreceptor samenwerken om ferroptose in toom te houden, wijst het op een praktische manier om dat vangnet weg te halen. Hoewel klinische tests nodig zullen zijn, biedt het idee om hart- en prostaatmiddelen te hergebruiken naast bestaande melanoombehandelingen een veelbelovende weg naar langer aanhoudende responsen en mogelijk betere uitkomsten voor patiënten van wie de tumoren geneigd zijn terug te vallen.
Bronvermelding: Redondo-Muñoz, M., Caballe-Mestres, A., Reisz, J.A. et al. Androgen receptor and fatty acid oxidation cooperate in ferroptosis evasion in BRAFi resistant melanoma. Cell Death Dis 17, 338 (2026). https://doi.org/10.1038/s41419-026-08578-4
Trefwoorden: melanoom, ferroptose, vetzuuroxidatie, androgeenreceptor, medicatieresistentie