Clear Sky Science · de
Androgenrezeptor und Fettsäureoxidation kooperieren bei der Umgehung von Ferroptose in BRAFi-resistentem Melanom
Warum das für die Behandlung hartnäckiger Hautkrebsarten wichtig ist
Medikamente, die mutiertes BRAF blockieren – einen zentralen Wachstumsschalter beim Melanom – haben die Versorgung von Menschen mit fortgeschrittener Hautkrebserkrankung grundlegend verändert. Dennoch schrumpfen viele Tumoren zunächst nur, um einige Monate später wieder heftig zurückzukehren. Diese Studie untersucht, was diesen Rückkehrtumoren hilft, am Leben zu bleiben, und beleuchtet einen neuen Weg, sie in einen Selbstzerstörungsmodus namens Ferroptose zu treiben, indem zwei bereits zugelassene Herz- und Prostatamedikamente kombiniert werden.
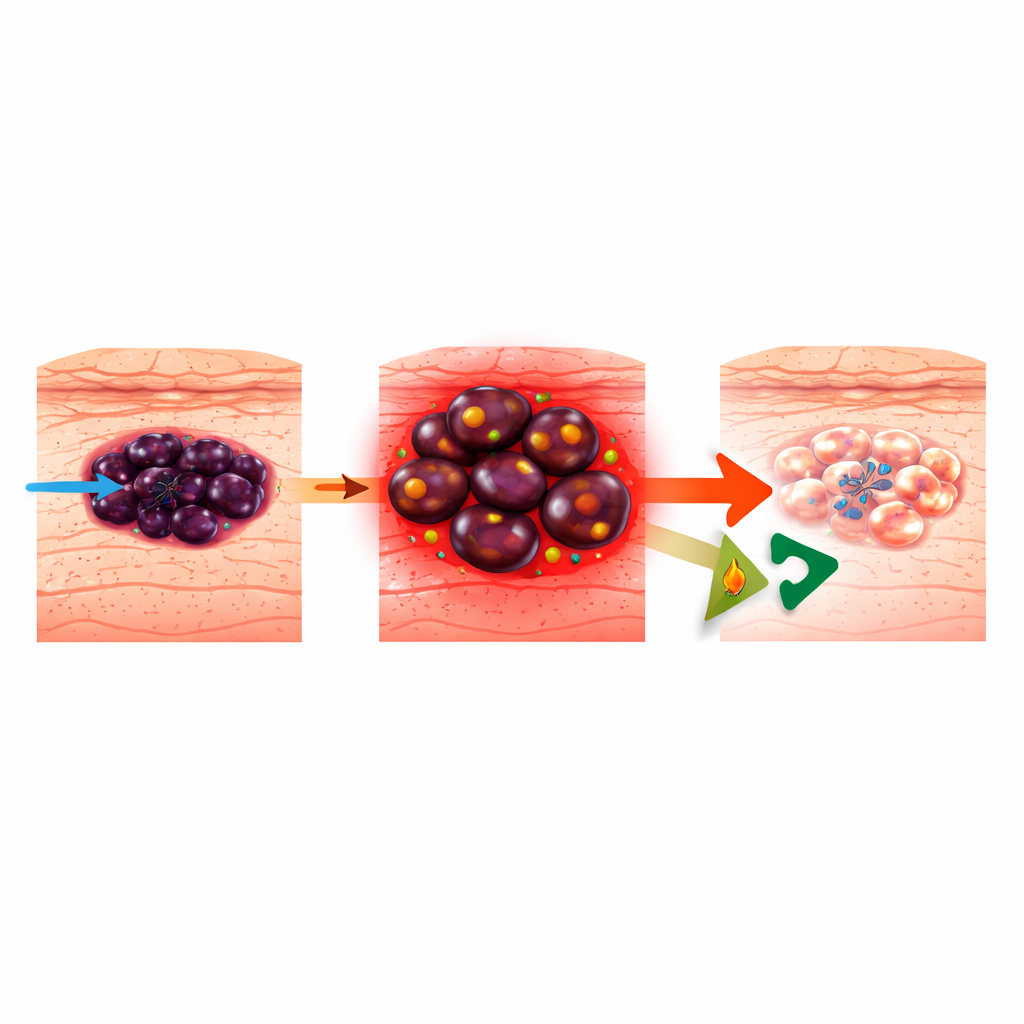
Wie Melanom lernt, gezielte Therapien zu umgehen
Das Melanom entsteht aus pigmentbildenden Zellen der Haut und verursacht die meisten Todesfälle durch Hautkrebs. Moderne zielgerichtete Therapien richten sich gegen den überaktiven BRAF–MEK-Signalweg, der viele Melanome antreibt, doch Tumoren sind bemerkenswert anpassungsfähig. Sie können zwischen unterschiedlichen „Zellzuständen“ wechseln, von einer reiferen, pigmentbildenden Identität zu einem primitiveren, neuralleisteähnlichen oder undifferenzierten Zustand, der aggressiv und medikamentenresistent ist. Frühere Arbeiten zeigten, dass sich Melanome beim Erwerb von Resistenz gegen BRAF-Blocker (BRAFi) zunehmend durch Verbrennen von Fetten in ihren Mitochondrien ernähren, einem Prozess, der als Fettsäureoxidation (FAO) bezeichnet wird. Die FAO mit dem Herzmedikament Ranolazin zu blockieren, war bekanntlich in der Lage, das Anwachsen resistenter Zellen zu verlangsamen, doch wie genau dadurch Melanomzellen zugrunde gingen, war unklar.
Eine verborgene Verwundbarkeit: eisengetriebene Fettschädigung
Die Forscher konzentrierten sich auf Ferroptose, eine Form des Zelltods, die ausgelöst wird, wenn Eisen zerstörerische chemische Reaktionen in bestimmten Fetten der Zellmembranen fördert. Sie fanden heraus, dass BRAFi-resistente Melanomzellen viele Merkmale aufweisen, die sie an den Rand der Ferroptose bringen: Sie haben niedrigere Werte des Antioxidans Glutathion, ihre Membranen sind reich an langen, schadensanfälligen mehrfach ungesättigten Fettsäuren, und sie zeigen mehr oxidierte Membranlipide als ihre medikamentenempfindlichen Gegenstücke. Patiententumorproben, die unter BRAF-Inhibitoren progredient waren, zeigten dasselbe Muster, wobei Marker sowohl der Ferroptose als auch der Fettsäureabbauwege parallel zunahmen. Das deutet darauf hin, dass resistente Zellen auf einem schmalen Grat balancieren – hochgradig verwundbar gegenüber eisengetriebener Fettschädigung, aber gleichzeitig verdrahtet, diese zu unterdrücken.
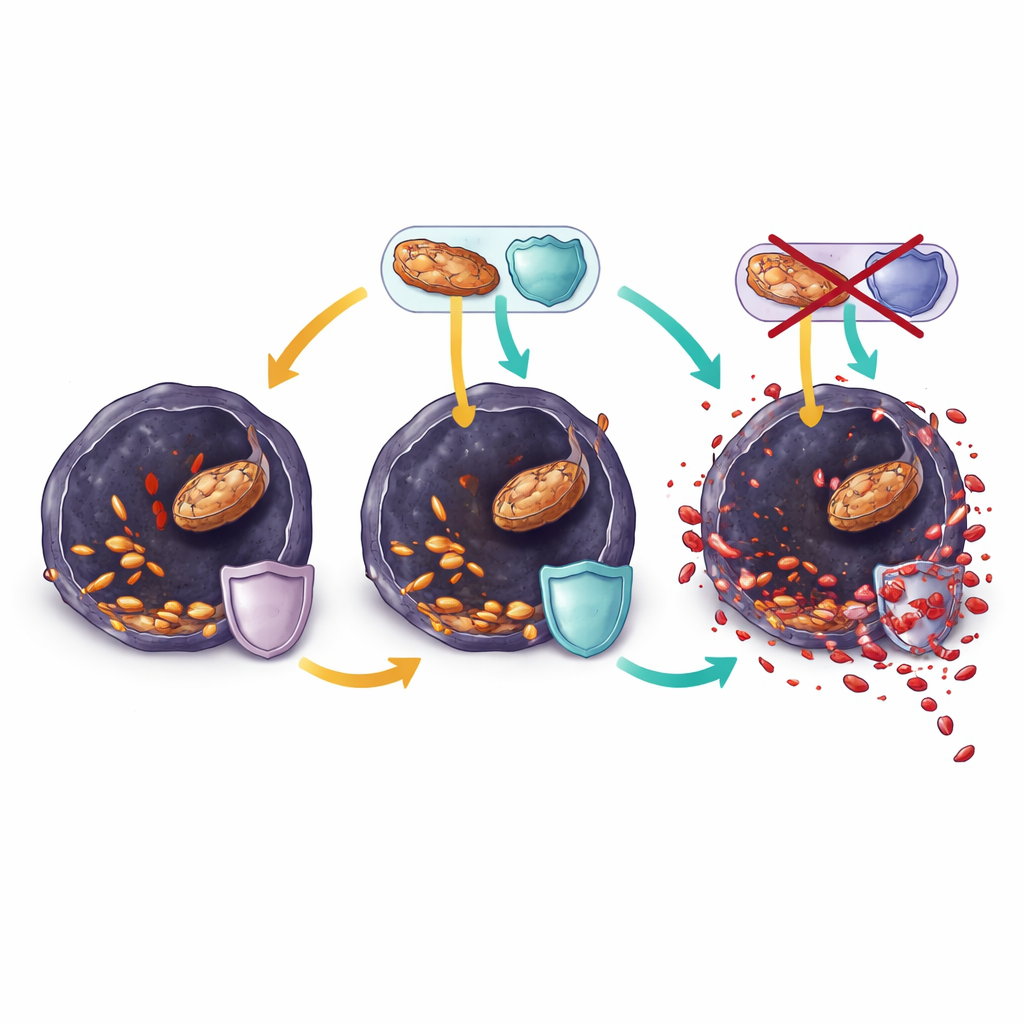
Ranolazin verschiebt das Gleichgewicht zugunsten des Zelltods
In im Labor kultivierten resistenten Melanomzellen senkte Ranolazin schnell die Fettabbauaktivität, entleerte wichtige Energiemoleküle und verringerte zusätzlich das Glutathion. Gleichzeitig wurden mehr mehrfach ungesättigte Fettsäuren in Membranlipide eingebaut, und Anzeichen von oxidativem Stress und Lipidschäden stiegen an. Diese Veränderungen verlangsamten das Zellwachstum innerhalb weniger Stunden und konnten durch klassische Ferroptosehemmer rückgängig gemacht werden, was zeigte, dass Ranolazin die Zellen hauptsächlich tötete, indem es sie über die Schwelle zur Ferroptose trieb. Als Tumoren in Mäusen jedoch schließlich der kombinierten BRAF- und Ranolazin-Behandlung entkamen, hatten sich ihre Zellen erneut umverdrahtet. Sie hielten hohe Spiegel von Enzymen aufrecht, die oxidierte Lipide reparieren und schützende Moleküle wieder auffüllen, und sie remodelten ihre Membranen so, dass mehr resistentere einfach ungesättigte Fettsäuren anstelle der anfälligen mehrfach ungesättigten Fettsäuren enthalten waren.
Hormonsignale helfen, die Verteidigung des Tumors wieder aufzubauen
Das Team führte dieses Membranremodeling auf Enzyme namens MBOAT1 und MBOAT2 zurück, die während der Phospholipid-Erneuerung sicherere Fettsäuren einbauen. Diese Enzyme waren in Ranolazin-resistenten Zellen und in vielen Patientenproben, die unter BRAF-Inhibitoren rezidiviert hatten, stark erhöht. Ihre Aktivität hing vom Androgenrezeptor (AR) ab, einem Hormonsensor, der vor allem aus dem Prostatakrebs bekannt ist. AR band an Kontrollregionen der MBOAT1- und MBOAT2-Gene und steigerte deren Aktivität. Als die Forscher AR mit dem Prostatakrebsmedikament Enzalutamid blockierten, sanken die MBOAT1/2-Spiegel und Melanomzellen wurden deutlich empfindlicher gegenüber ferroptoseauslösenden Mitteln. Dieser Effekt war in verschiedenen Melanomzellzuständen zu beobachten, sowohl in primitiven, hochgradig medikamentenresistenten Zellen als auch in differenzierteren pigmentähnlichen Zellen.
Die Kombination zweier etablierter Medikamente, um resistente Tumoren auszutricksen
Da FAO und AR-kontrolliertes Lipidremodeling jeweils Melanomzellen helfen, Ferroptose zu entkommen, prüften die Autoren, ob das gleichzeitige Treffen beider Prozesse besonders wirksam wäre. In Zellkulturen führte die Kombination von Ranolazin (das Fettverbrennung blockiert und Lipidschäden fördert) mit Enzalutamid (das AR und dessen membranschützende Enzyme außer Kraft setzt) zu umfangreichem ferroptotischem Zelltod, insbesondere in Zellen, die stark auf FAO angewiesen waren und in den aggressiven undifferenzierten Zustand gewechselt hatten. Unter Bedingungen, die Melanomzellen zwingen, vermehrt Fett als Brennstoff zu nutzen, wurde diese Kombination noch tödlicher. Die Arbeit legt nahe, dass eine Dualtherapie mit diesen bereits zugelassenen Medikamenten sowohl die Entstehung von Resistenz gegenüber BRAF‑gerichteten Behandlungen verzögern als auch resistente Tumoren, einschließlich solcher, die Immunangriffen ausweichen, verwundbarer machen könnte, indem sie sie in die Ferroptose zwingt.
Was das für Patientinnen und Patienten bedeuten könnte
Diese Forschung zeichnet ein genaues Bild davon, wie Melanomzellen, die durch gezielte Therapie in die Enge getrieben werden, ihren Stoffwechsel und ihre Hormon‑Signalwege umgestalten, um einer tödlichen Form des eisen‑ und fettbasierten Zelltods zu entgehen. Indem sie zeigt, dass Fettsäureabbaustreifen und der Androgenrezeptor zusammenarbeiten, um Ferroptose in Schach zu halten, weist sie auf einen praktischen Ansatz hin, dieses Sicherheitsnetz zu beseitigen. Klinische Prüfungen sind erforderlich, doch die Idee, Herz‑ und Prostatamedikamente neben bestehenden Melanomtherapien wiederzuverwenden, bietet einen vielversprechenden Weg zu länger anhaltenden Ansprechraten und möglicherweise besseren Ergebnissen für Patientinnen und Patienten mit rezidivgefährdeten Tumoren.
Zitation: Redondo-Muñoz, M., Caballe-Mestres, A., Reisz, J.A. et al. Androgen receptor and fatty acid oxidation cooperate in ferroptosis evasion in BRAFi resistant melanoma. Cell Death Dis 17, 338 (2026). https://doi.org/10.1038/s41419-026-08578-4
Schlüsselwörter: Melanom, Ferroptose, Fettsäureoxidation, Androgenrezeptor, Drogenresistenz