Clear Sky Science · ar
مستقبل الأندروجين وأكسدة الأحماض الدهنية يتعاونا للهروب من الفيروبتوسيس في الميلانوما المقاومة لمثبطات BRAF
لماذا هذا مهم لعلاج سرطانات الجلد العنيدة
حوَّلَت الأدوية التي تُعيق النسخة الطافرة من BRAF، وهو مفتاح تحكم في نمو الميلانوما، رعاية الأشخاص المصابين بسرطان الجلد المتقدم. ومع ذلك، تنكمش العديد من الأورام في البداية ثم تعاود الظهور بقوة بعد شهور. تبحث هذه الدراسة في ما يساعد تلك الأورام المنتكسة على البقاء وتستكشف نهجاً جديداً لدفعها نحو وضع الانتحار الخلوي المسمى الفِيروبتوسيس، باستخدام دواءين مُعتمدين للقلب والبروستات بالتركيب.
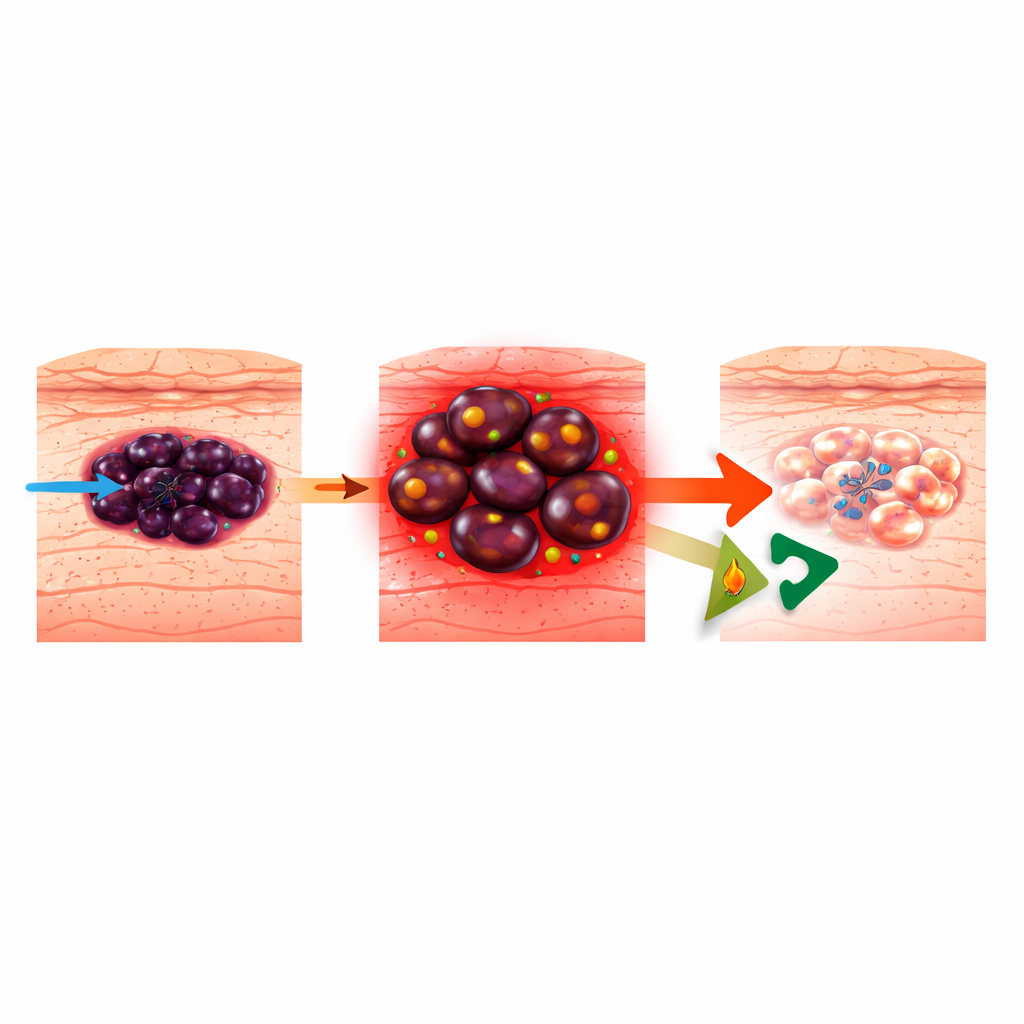
كيف تتعلّم الميلانوما تجنّب العقاقير الموجَّهة
تنشأ الميلانوما من خلايا تصنع الصبغة في الجلد وتُسبّب معظم وفيات سرطان الجلد. تهاجم العلاجات الموجَّهة الحديثة مسار BRAF–MEK المفرط النشاط الذي يدفع العديد من حالات الميلانوما، لكن الأورام مرنة بشكل ملحوظ. يمكنها التبديل بين «حالات خلوية» مختلفة، من هوية ناضجة أكثر في إنتاج الصبغة إلى حالة بدائية أكثر شبيهة بالقِمّة العصبية أو حالة غير متمايزة تكون عدوانية ومقاومة للأدوية. أظهرت أعمال سابقة أنه مع تطور الميلانوما لتصبح مقاومة لمثبطات BRAF (BRAFi)، فإنها تعتمد بشكل متزايد على حرق الدهون في الميتوكوندريا، وهي عملية تُسمى أكسدة الأحماض الدهنية (FAO). كان معروفاً أن حجب FAO بواسطة دواء القلب رانولازين يبطئ صعود الخلايا المقاومة، لكن لم يكن واضحاً كيف يقتل هذا الميلانوما فعلياً.
ضعف خفي: تلف الدهون المدفوع بالحديد
ركّز الباحثون على الفِيروبتوسيس، وهو شكل من أشكال موت الخلايا يُثار عندما يساعد الحديد في توليد تفاعلات كيميائية مدمرة في بعض الدهون داخل أغشية الخلايا. وجدوا أن خلايا الميلانوما المقاومة لمثبطات BRAF تحمل العديد من السمات التي تتركها على حافة الفِيروبتوسيس: مستويات منخفضة من مضاد الأكسدة غلوتاثيون، أغشية محشوة بدهون متعددة غير مشبعة طويلة ومعرضة للتلف، ومستويات أعلى من الدهون الغشائية المؤكسدة مقارنةً بنظيراتها الحساسة للدواء. أظهرت عينات أورام المرضى التي تقدمت أثناء علاجها بمثبطات BRAF نفس النمط، مع ارتفاع علامات كل من الفِيروبتوسيس ومسارات حرق الدهون معاً. وهذا يوحي بأن الخلايا المقاومة تمشي على حبل مشدود—معرضة بشدة لتلف الدهون المدفوع بالحديد، لكنها في الوقت نفسه مُبرمَجة لقمعه.
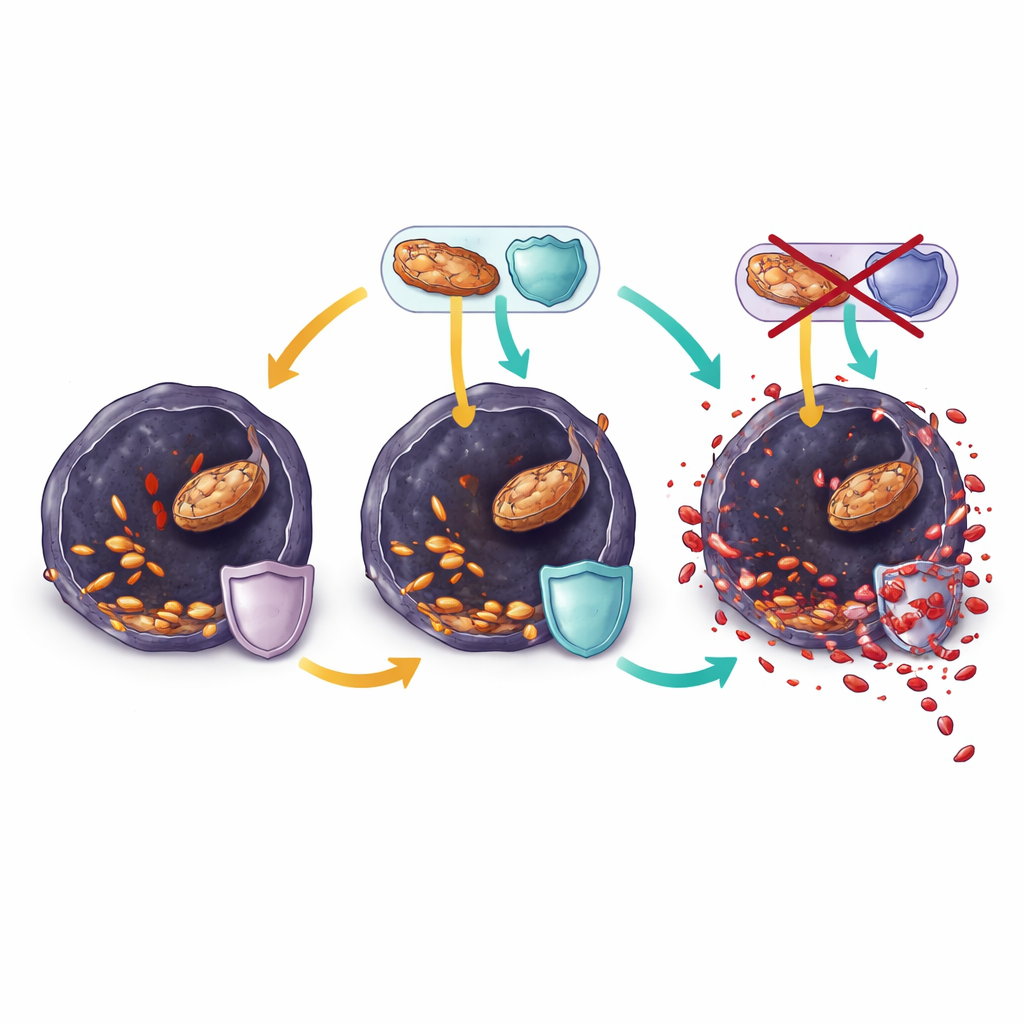
رانولازين يميل الميزان نحو موت الخلايا
في خلايا الميلانوما المقاومة المزروعة في المختبر، خفّض رانولازين بسرعة نشاط حرق الدهون، واستنزف جزيئات الطاقة الأساسية، وخفض الغلوتاثيون أكثر. في الوقت نفسه، تم حشو المزيد من الدهون المتعددة غير المشبعة في دهون الأغشية، وتزايدت علامات الإجهاد التأكسدي وتلف الدهون. أبطأت هذه التغييرات نمو الخلايا في غضون ساعات ويمكن عكسها بواسطة مانعات الفِيروبتوسيس الكلاسيكية، مما أظهر أن رانولازين كان يقتل الخلايا بشكل أساسي بدفعها إلى الفِيروبتوسيس. ومع ذلك، عندما هربت الأورام في الفئران في نهاية المطاف من العلاج المشترك بمثبط BRAF ورانولازين، كانت خلاياها قد أعادت توصيل شبكاتها مجدداً. حافظت على مستويات عالية من الإنزيمات التي تُصلِح الدهون المؤكسدة وتُجدّد الجزيئات الوقائية، وأعادت تشكيل أغشيتها لتحتوي على دهون أحادية غير مُشبعة أكثر مقاومة بدلاً من الدهون متعددة غير المشبعة المعرضة للتلف.
الإشارات الهرمونية تساعد في إعادة بناء دفاعات الورم
تتبّع الفريق إعادة تشكيل الأغشية هذه إلى إنزيمات تُدعى MBOAT1 وMBOAT2، التي تستبدل دهوناً أأمن أثناء تجديد الفوسفاتيد. زادت مستويات هذه الإنزيمات بشدة في الخلايا المقاومة لرانولازين وفي العديد من أورام المرضى التي انتكست أثناء علاجها بمثبطات BRAF. اعتمد نشاطها على مستقبل الأندروجين (AR)، وهو حساس هرموني معروف أكثر بسرطان البروستات. ارتبط AR بمناطق تحكم في جينات MBOAT1 وMBOAT2 وعزّز نشاطها. عندما حجب الباحثون AR باستخدام دواء سرطان البروستات إنزالوتاميد، انخفضت مستويات MBOAT1/2 وأصبحت خلايا الميلانوما أكثر حساسية كثيراً لعوامل تحريض الفِيروبتوسيس. لوحِظ هذا التأثير عبر حالات خلوية ميلانومية مختلفة، بما في ذلك كل من الخلايا البدائية المقاومة بشدة والخلايا المتمايزة الشبيهة بخلايا الصبغة.
مزاوجة دوائين قد تُخدَع الأورام المقاومة
لأن FAO وإعادة تشكيل الدهون المُتحكَّم بها بواسطة AR كلٌ منهما يساعد خلايا الميلانوما على الهروب من الفِيروبتوسيس، اختبر المؤلفون ما إذا كان استهداف كلا المسارين معاً سيكون فعّالاً بشكل خاص. في مزروعات خلوية، أدت موازنة رانولازين (الذي يعرقل حرق الدهون ويعزز تلف الدهون) مع إنزالوتاميد (الذي يعطل AR وإنزيماته الواقية للغشاء) إلى موت خلوي فيربتوتي واسع النطاق، لا سيما في الخلايا التي اعتمدت بشكل كبير على FAO وتحولت إلى الحالة غير المتمايزة العدوانية. تحت ظروف تجبر خلايا الميلانوما على الاعتماد أكثر على الدهون كوقود، أصبح هذا المزيج أكثر فتكاً. تشير هذه النتائج إلى أن استراتيجية علاجية مزدوجة باستخدام هذين الدوائين المعتمدين قد تؤخر مقاومة علاجات BRAF الموجَّهة وتجعل الأورام المقاومة، بما في ذلك تلك التي تُضعِف استجابة الجهاز المناعي، أكثر عرضة بدفعها نحو الفِيروبتوسيس.
ماذا قد يعني هذا للمرضى
ترسم هذه الأبحاث صورة مفصلة عن كيف تعيد خلايا الميلانوما، التي تضطر إلى الزاوية بواسطة العلاج الموجَّه، تشكيل أيضها وإشاراتها الهرمونية لتجنب شكل قاتل من الموت الخلوي القائم على الحديد والدهون. من خلال الكشف أن مسارات حرق الدهون ومستقبل الأندروجين يتعاونان للحفاظ على كبح الفِيروبتوسيس، تشير الدراسة إلى وسيلة عملية لسحب تلك الشبكة الأَمْنِية. بينما سيظل الاختبار السريري ضرورياً، يقدم اقتراح إعادة توظيف أدوية للقلب والبروستات إلى جانب علاجات الميلانوما الحالية مساراً واعداً لتحقيق استجابات أطول أمداً وربما نتائج أفضل للمرضى الذين تكون أورامهم عرضة للانتكاس.
الاستشهاد: Redondo-Muñoz, M., Caballe-Mestres, A., Reisz, J.A. et al. Androgen receptor and fatty acid oxidation cooperate in ferroptosis evasion in BRAFi resistant melanoma. Cell Death Dis 17, 338 (2026). https://doi.org/10.1038/s41419-026-08578-4
الكلمات المفتاحية: الميلانوما, الفِيروبتوسيس, أكسدة الأحماض الدهنية, مستقبل الأندروجين, مقاومة الأدوية