Clear Sky Science · ru
Рецептор андрогенов и окисление жирных кислот сотрудничают в уклонении от ферроптоза при меланоме, резистентной к BRAFi
Почему это важно для лечения упорных кожных опухолей
Препараты, блокирующие мутантный BRAF — ключевой переключатель роста при меланоме — преобразили подход к лечению людей с запущенным раком кожи. Тем не менее многие опухоли сначала сжимаются, а через несколько месяцев вновь бурно растут. В этом исследовании рассматривают, что помогает таким вернувшимся опухолям выживать, и изучают новый способ подтолкнуть их к самоуничтожению — ферроптозу — с помощью комбинации двух уже существующих лекарств, применяемых при сердечных и простатических заболеваниях.
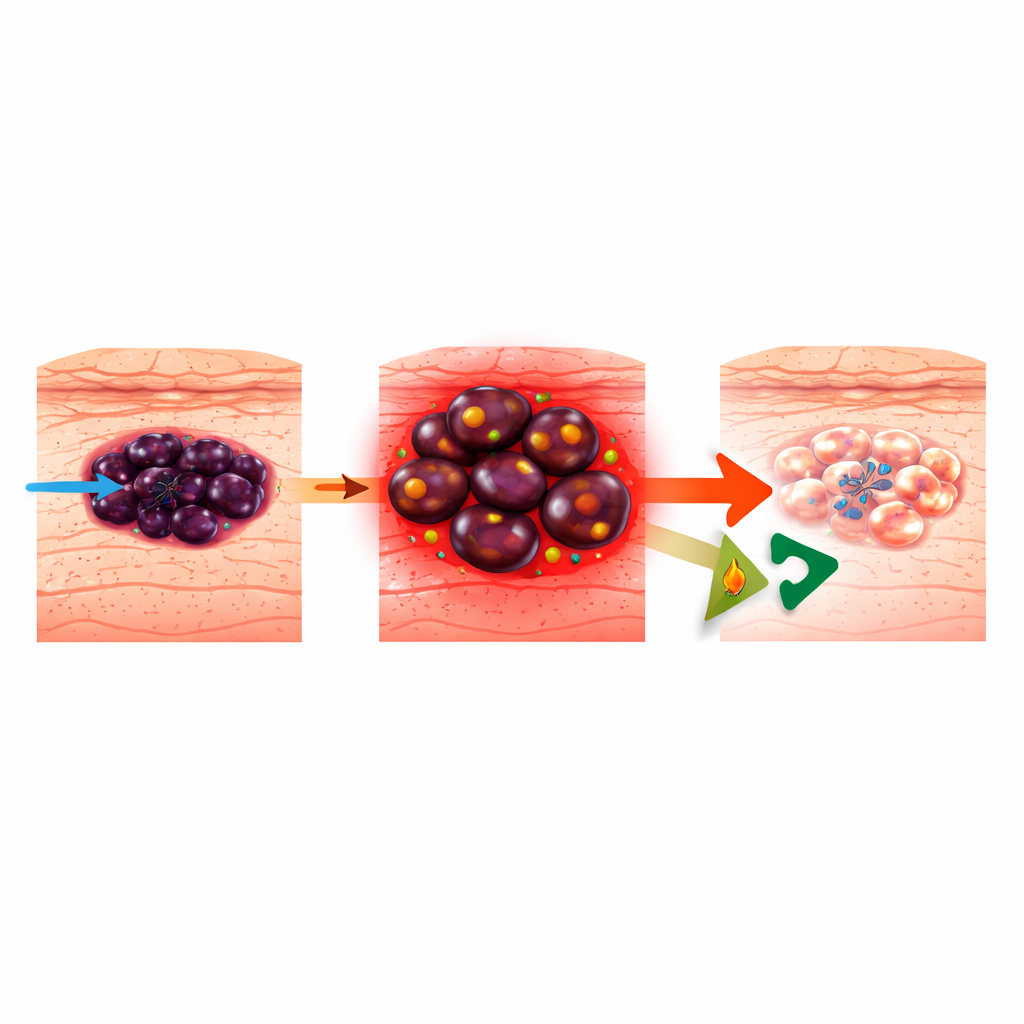
Как меланома учится уклоняться от таргетной терапии
Меланома возникает из клеток, производящих пигмент в коже, и вызывает большинство смертельных случаев рака кожи. Современные таргетные терапии направлены на гиперактивный путь BRAF–MEK, который движет многие меланомы, но опухоли удивительно пластичны. Они могут переключаться между разными «состояниями клеток», от более зрелой пигментпродуцирующей идентичности до более примитивного, напоминающего нейральный гребень или недифференцированного состояния, которое агрессивно и устойчиво к препаратам. Ранее показали, что по мере приобретения резистентности к ингибиторам BRAF (BRAFi) меланомы всё чаще питаются, сжигая жиры в митохондриях — процесс, называемый окислением жирных кислот (FAO). Было известно, что блокада FAO сердечным препаратом ранолазином замедляет рост резистентных клеток, но механизм, приводящий к гибели меланомных клеток, оставался неясным.
Скрытая уязвимость: повреждение жиров под действием железа
Исследователи сосредоточились на ферроптозе — форме гибели клеток, вызванной тем, что железо способствует разрушительным химическим реакциям в определённых жирах мембран. Они обнаружили, что клетки меланомы, резистентные к BRAFi, обладают многими признаками, ставящими их на грань ферроптоза: у них понижены уровни антиоксиданта глутатиона, их мембраны насыщены длинными, склонными к повреждению полиненасыщенными жирными кислотами, и в них наблюдается больше окисленных липидов по сравнению с чувствительными к препаратам клетками. Образцы опухолей пациентов, прогрессировавшие на ингибиторах BRAF, показали ту же картину: маркеры и ферроптоза, и путей сжигания жиров повышались одновременно. Это наводило на мысль, что резистентные клетки идут по тонкой грани — они сильно уязвимы к повреждению жиров под действием железа, но одновременно имеют механизмы, подавляющие это повреждение.
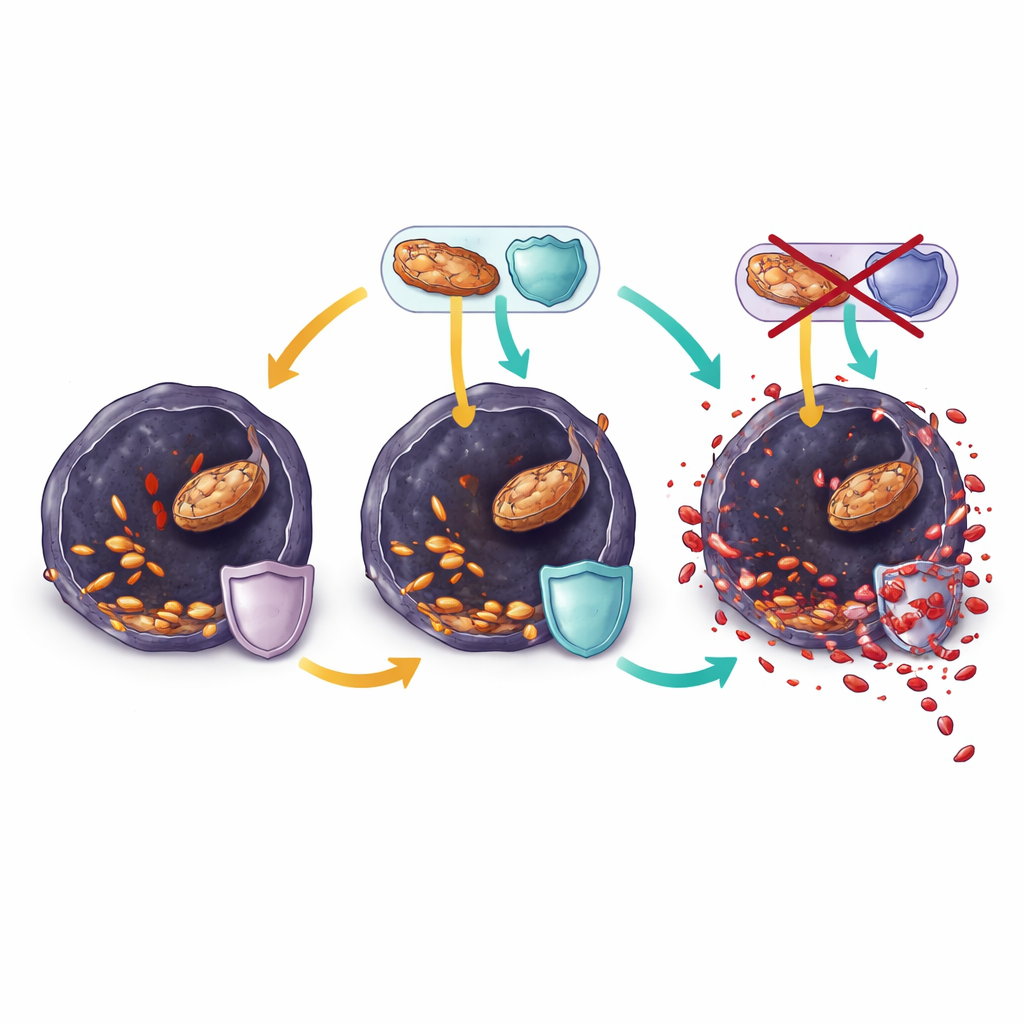
Ранолазин сдвигает баланс в сторону гибели клеток
В резистентных клетках меланомы, выращенных в лаборатории, ранолазин быстро снижал активность сжигания жиров, истощал ключевые энергетические молекулы и ещё больше снижал уровни глутатиона. Одновременно в мембранную фосфолипидную фракцию накапливалось больше полиненасыщенных жирных кислот, а признаки окислительного стресса и повреждения липидов резко возросли. Эти изменения замедляли рост клеток уже в течение нескольких часов и могли быть обращены классическими ингибиторами ферроптоза, что указывает на то, что ранолазин убивал клетки в основном, подталкивая их к ферроптозу. Однако когда опухоли у мышей в конце концов уходили от комбинированного лечения BRAF-ингибитором и ранолазином, их клетки снова перестроились. Они поддерживали высокие уровни ферментов, восстанавливающих окисленные липиды и пополняющих защитные молекулы, и перестраивали свои мембраны так, чтобы содержать больше устойчивых мононенасыщенных жиров вместо уязвимых полиненасыщенных.
Гормональные сигналы помогают восстановить защиту опухоли
Команда проследила это ремоделирование мембран до ферментов MBOAT1 и MBOAT2, которые заменяют в фосфолипидах на более безопасные жирные кислоты при их обновлении. Эти ферменты были значительно повышены в клетках, резистентных к ранолазину, и во многих опухолях пациентов, рецидивировавших на ингибиторах BRAF. Их активность зависела от рецептора андрогенов (AR) — гормонального сенсора, более известного по раку предстательной железы. AR связывался с регуляторными областями генов MBOAT1 и MBOAT2 и усиливал их экспрессию. Когда исследователи блокировали AR препаратом от рака простаты энзалутамидом, уровни MBOAT1/2 падали, и клетки меланомы становились гораздо более чувствительны к агентам, индуцирующим ферроптоз. Этот эффект наблюдался в разных состояниях меланомных клеток, включая как примитивные, сильно резистентные клетки, так и более дифференцированные, похожие на пигментные клетки.
Сочетание двух старых препаратов, чтобы перехитрить резистентные опухоли
Поскольку FAO и контролируемое AR ремоделирование липидов по отдельности помогают клеткам меланомы уклоняться от ферроптоза, авторы проверили, будет ли эффективнее одновременно атаковать обе цели. В культурах клеток комбинирование ранолазина (блокирующего сжигание жиров и усиливающего повреждение липидов) с энзалутамидом (обезвреживающим AR и его мембрано-защитные ферменты) вызывало массовую ферроптотическую гибель клеток, особенно в клетках, сильно зависящих от FAO и перешедших в агрессивное недифференцированное состояние. В условиях, заставляющих клетки меланомы больше зависеть от жиров как топлива, эта комбинация становилась ещё более смертельной. Работа указывает, что стратегия двойной терапии с уже одобренными препаратами может как отсрочить развитие резистентности к таргетным BRAF-препаратам, так и сделать резистентные опухоли, включая те, которые подавляют иммунный ответ, более уязвимыми, вынуждая их к ферроптозу.
Что это может значить для пациентов
Это исследование даёт подробную картину того, как клетки меланомы, загнанные в угол таргетной терапией, перестраивают свой метаболизм и гормональную сигнализацию, чтобы избежать смертельной формы гибели клеток, зависящей от железа и липидов. Показав, что пути сжигания жиров и рецептор андрогенов совместно удерживают ферроптоз под контролем, работа указывает на практический способ убрать эту страховку. Хотя потребуются клинические испытания, идея репозиционирования сердечных и препаратов для простаты в сочетании с существующими методами лечения меланомы выглядит многообещающей для получения более продолжительных ответов и, возможно, лучших исходов для пациентов, опухоли которых склонны к рецидиву.
Цитирование: Redondo-Muñoz, M., Caballe-Mestres, A., Reisz, J.A. et al. Androgen receptor and fatty acid oxidation cooperate in ferroptosis evasion in BRAFi resistant melanoma. Cell Death Dis 17, 338 (2026). https://doi.org/10.1038/s41419-026-08578-4
Ключевые слова: меланома, ферроптоз, окисление жирных кислот, рецептор андрогенов, лекарственная резистентность