Clear Sky Science · he
קולטן האנדרוגן וחמצון חומצות שומן משתפים פעולה בהימנעות מפרופטוזיס במלנומה עמידה ל-BRAFi
מדוע זה חשוב לטיפול בסרטןי עור עקשניים
תרופות החוסמות את BRAF המוטנטי, מתג הצמיחה המרכזי במלנומה, שינו את הטיפול באנשים עם סרטן עור מתקדם. עם זאת, גידולים רבים מצטמצמים בהתחלה רק כדי לחזור בחזרה חודשים לאחר מכן. המאמר חוקר מה עוזר לגידולים שאלה לשרוד ומציע דרך חדשה לדחוף אותם למצב של מוות תאי עצמתי שנקרא פרופטוזיס, באמצעות שילוב של שתי תרופות קיימות המשמשות בלב ובסרטן הערמונית.
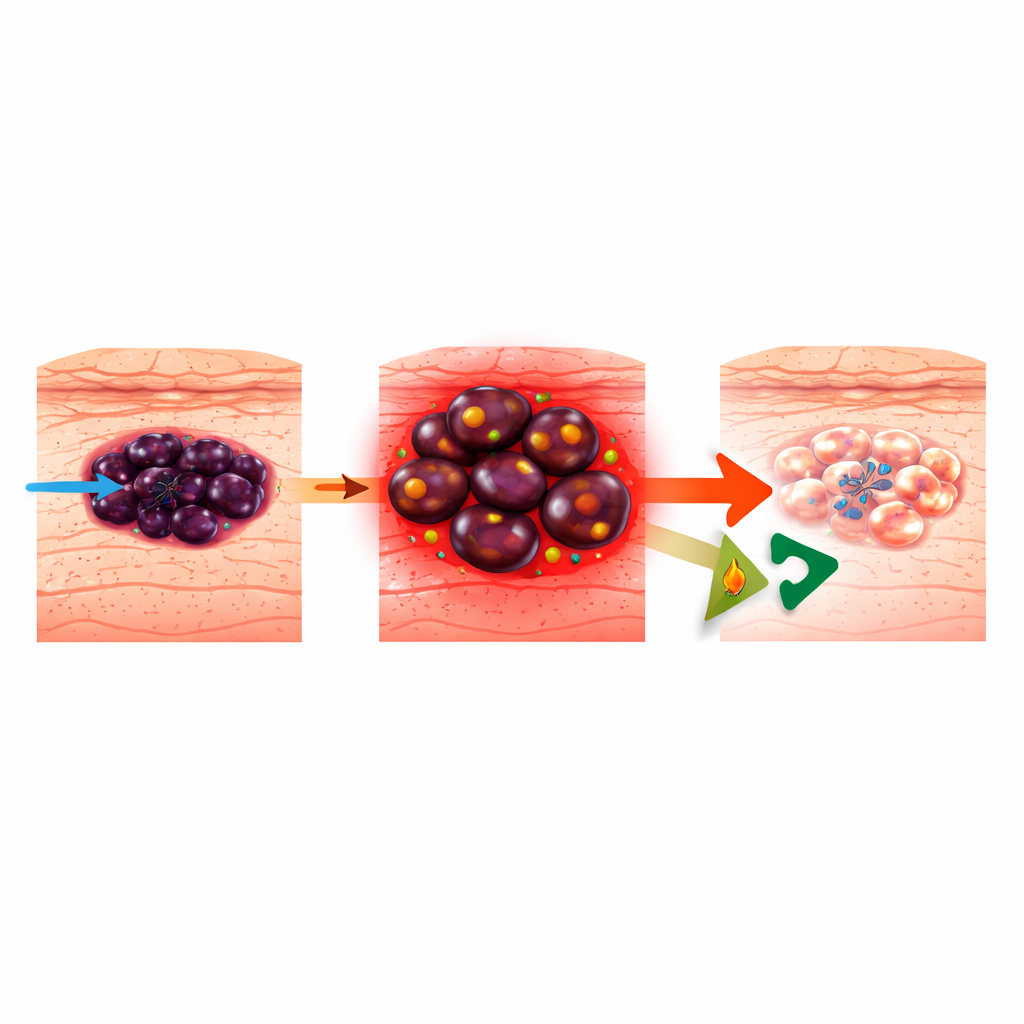
כיצד מלנומה לומדת להתחמק מתרופות ממוקדות
מלנומה נובעת מתאים שמייצרים פיגמנט בעור והיא אחראית לרוב מקרי המוות מסרטן העור. טיפולים מודרניים ממוקדים תוקפים את מסלול BRAF–MEK הפעיל יתר על המידה שמניע רבות מהמלנומות, אך הגידולים גמישים ביותר. הם יכולים לעבור בין "מצבי תא" שונים, מהזהות הבוגרת של יצירת פיגמנט למצב פרימיטיבי יותר, הדומה לנאורל-קרסט או לא-ממוין, שתכונתו תוקפנית ועמידה לתרופות. עבודות קודמות הראו שכאשר מלנומות מפתחות עמידות לתרופות החוסמות BRAF (BRAFi), הן מגדילות את התזונה העצמית באמצעות שריפת שומנים במיטוכונדריה בתהליך שנקרא חמצון חומצות שומן (FAO). חסימת FAO בעזרת תרופת הלב רנולזין הייתה ידועה כמעכבת את עליית התאים העמידים, אך לא היה ברור כיצד הדבר למעשה הורג את תאי המלנומה.
פגיעה חשאית: נזק שומני מונע-ברזל
החוקרים התמקדו בפרופטוזיס, צורה של מוות תאי המופעלת כאשר ברזל מסייע ליצירת תגובות כימיות הרסניות בשומנים מסוימים בממברנות התאים. הם גילו שתאי מלנומה עמידים ל-BRAFi נושאים תכונות רבות שמשאירות אותם על סף פרופטוזיס: רמות נמוכות יותר של הנוגד-חמצון גלוטתיון, ממברנות עשירות בשומנים רב-בלתי-רווים ארוכים הרגישים לנזק, וסימנים רבים יותר לשומנים ממולקקים בחמצון לעומת תאים רגישים לתרופה. דגימות גידול ממטופלים שהתקדמו תחת מעכבי BRAF הראו דפוס דומה, עם סימנים גם לפרופטוזיס וגם למסלולים של שריפת שומנים שעולים יחד. זה מרמז כי התאים העמידים צועדים על חבל דק—פגיעים מאוד לנזק שומני מונע-ברזל, אך במקביל מחוברים במנגנונים שמדכאים זאת.
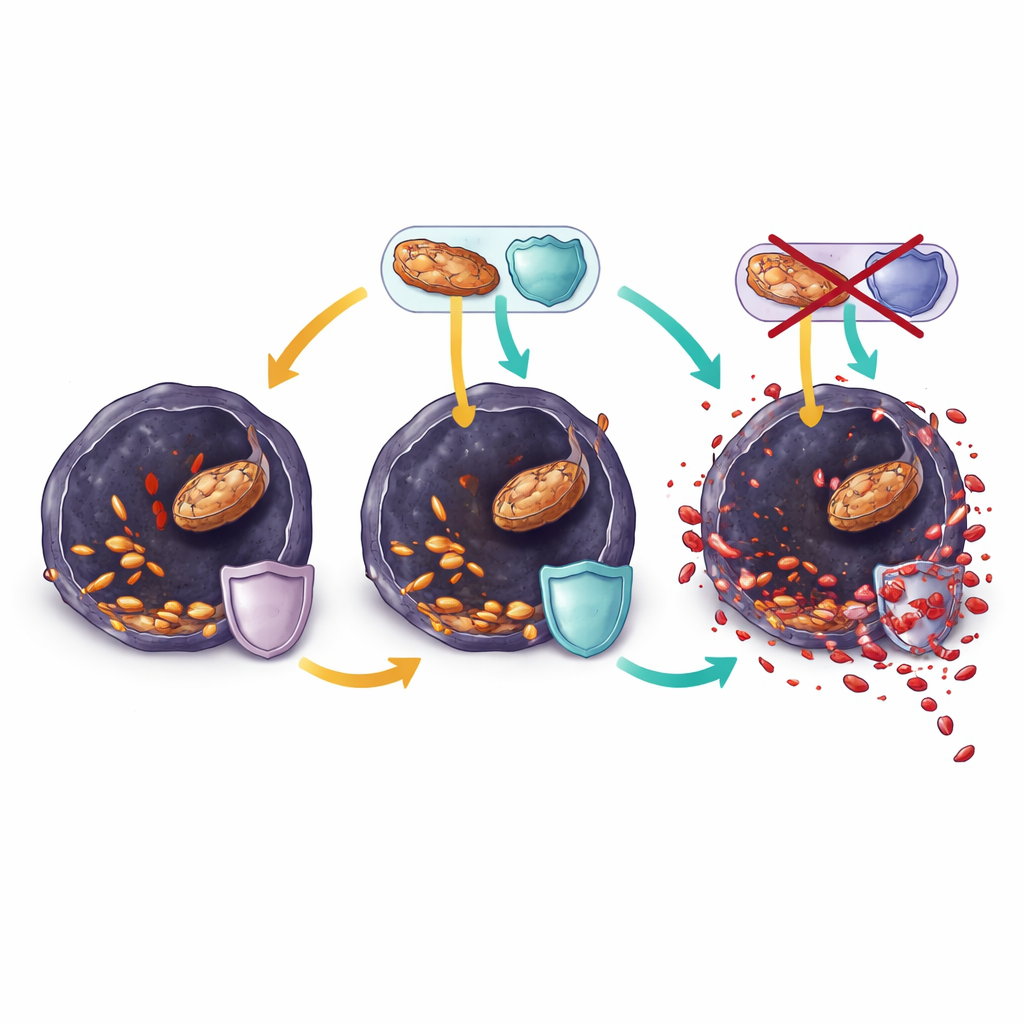
רנולזין מהצדד את המאזן לטובת מוות תאי
בתאי מלנומה עמידים שגודלו במאגר, רנולזין קטע במהירות את פעילות שריפת השומנים, רוקן מולקולות אנרגיה מרכזיות והוריד עוד יותר את רמות הגלוטתיון. במקביל, יותר שומנים רב-בלתי-רווים נשזרו לתוך ליפידים ממברנליים, וסימנים ללחץ חמצוני ונזק לשומנים עלו משמעותית. שינויים אלה האטו את גדילת התאים תוך שעות וניתנו להפיכה על-ידי חוסמי פרופטוזיס קלאסיים, מה שהראה שרנולזין הורג תאים בעיקר על ידי דחיפתם אל מעבר לקצה לפרופטוזיס. עם זאת, כאשר גידולים בעכברים בסופו של דבר התחמקו מטיפול משולב ב-BRAF ורנולזין, תאי הגידול התכווננו מחדש: הם שמרו על רמות גבוהות של אנזימים שמתקנים ליפידים מחומצנים ומשלימים מולקולות מגן, ושינו את הממברנות שלהם כך שיכילו יותר שומנים חד-בלתי-רווים עמידים במקום שומנים רב-בלתי-רווים פגיעים.
אותות הורמונליים מסייעים לבנות מחדש את ההגנה של הגידול
הצוות מיפה את שינוי הממברנה לאנזימים הקרויים MBOAT1 ו-MBOAT2, שמחליפים שומנים בטוחים יותר במהלך חידוש הפוספוליפידים. אנזימים אלה הוגברו בחוזקה בתאים עמידים לרנולזין וברבים מהגידולים של מטופלים שחזרו לאחר טיפול במעכבי BRAF. פעילותם התלוותה בקולטן האנדרוגן (AR), חיישן הורמונלי הידוע יותר ממחלת הערמונית. AR נקשר לאזורי בקרה של גני MBOAT1 ו-MBOAT2 והגביר את פעולתם. כאשר החוקרים חסמו את AR בעזרת תרופת סרטן הערמונית אנזלוטמיד, רמות MBOAT1/2 ירדו ותאי מלנומה הפכו לרגישים הרבה יותר לגורמים שמעוררים פרופטוזיס. השפעה זו נצפתה במגוון מצבי תא של מלנומה, כולל תאים פרימיטיביים מאוד עמידים לתרופות וגם תאים ממוינים יותר בדמיון לפיגמנט.
שילוב שתי תרופות ישנות כדי להקדים גידולים עמידים
מכיוון ש-FAO ותיקון הליפידים הנשלט על ידי AR מסייעים כל אחד בדרכם לתאי המלנומה להימלט מפרופטוזיס, החוקרים בדקו האם פגיעה בשניהם בו-זמנית תהיה יעילה במיוחד. בתרבית תאים, שילוב רנולזין (החוסם שריפת שומן ומגביר נזק לליפידים) עם אנזלוטמיד (המנטרל את AR ואת אנזימיו המגנים על הממברנה) גרם למוות תאי פרופטוטי נרחב, במיוחד בתאים שתלויים מאוד ב-FAO ועברו למצב פרימיטיבי תוקפני. בתנאים שמאלצים תאי מלנומה להסתמך יותר על שומן כדלק, השילוב הזה הפך אפילו קטלני יותר. המחקר מציע שאסטרטגיית טיפול כפולה באמצעות תרופות שאושרו כבר עשויה גם לעכב עמידות לטיפולים ממוקדים ב-BRAF וגם להפוך גידולים עמידים — כולל אלה שמטשטשים התקפות חיסוניות — לפגיעים יותר על ידי דחיפתם לפרופטוזיס.
מה זה יכול להיות עבור מטופלים
המחקר מצייר תמונה מפורטת של האופן שבו תאי מלנומה, שנדחקו לפינה על-ידי טיפול ממוקד, משנים את המטבוליזם ואת איתות ההורמונים שלהם כדי להתחמק מצורת מוות תאי קטלנית המבוססת על ברזל ושומן. על ידי חשיפת העובדה שמסלולי שריפת השומן וקולטן האנדרוגן משתפים פעולה כדי לשמור על פרופטוזיס במצב מדוכא, הוא מצביע על דרך מעשית להסיר רשת הביטחון הזו. אמנם יש צורך בניסויים קליניים, אך הרעיון למנף תרופות לב וכלייה לצד טיפולים קיימים למלנומה מציע מסלול מבטיח לתגובות ארוכות-טווח וייתכן ששיפור התוצאה עבור מטופלים שנוטים לסבול מהישנות הגידול.
ציטוט: Redondo-Muñoz, M., Caballe-Mestres, A., Reisz, J.A. et al. Androgen receptor and fatty acid oxidation cooperate in ferroptosis evasion in BRAFi resistant melanoma. Cell Death Dis 17, 338 (2026). https://doi.org/10.1038/s41419-026-08578-4
מילות מפתח: מלנומה, פרופטוזיס, חמצון חומצות שומן, קולטן אנדרוגן, עמידות לתרופות