Clear Sky Science · es
El receptor de andrógenos y la oxidación de ácidos grasos cooperan en la evasión de la ferroptosis en el melanoma resistente a BRAFi
Por qué esto importa para el tratamiento de cánceres de piel persistentes
Los fármacos que bloquean la BRAF mutada, un interruptor clave del crecimiento en el melanoma, han transformado la atención de personas con cáncer de piel avanzado. Sin embargo, muchos tumores se reducen al principio solo para reaparecer con fuerza meses después. Este estudio investiga qué permite que esos tumores reincidentes sigan vivos y explora una forma nueva de empujarlos hacia un modo de autodestrucción llamado ferroptosis, usando en combinación dos fármacos ya aprobados para el corazón y la próstata.
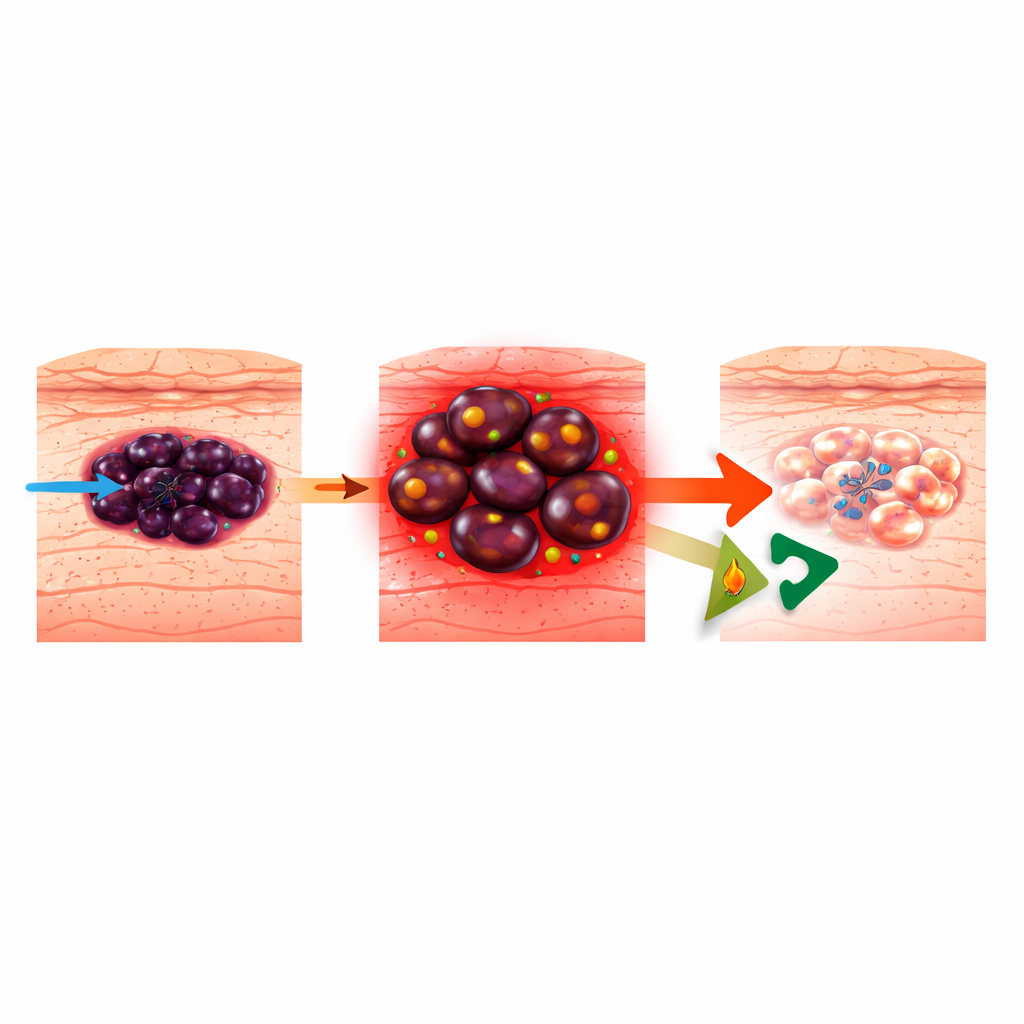
Cómo el melanoma aprende a esquivar fármacos dirigidos
El melanoma surge de células productoras de pigmento en la piel y causa la mayoría de las muertes por cáncer cutáneo. Las terapias dirigidas modernas atacan la vía BRAF–MEK hiperactiva que impulsa muchos melanomas, pero los tumores son extraordinariamente adaptables. Pueden cambiar entre distintos “estados celulares”, desde una identidad más madura productora de pigmento hasta un estado más primitivo, similar a la cresta neural o indiferenciado, que es agresivo y resistente a fármacos. Trabajos previos mostraron que cuando los melanomas vuelven resistentes a los bloqueantes de BRAF (BRAFi), cada vez más se alimentan quemando grasas en sus mitocondrias, un proceso llamado oxidación de ácidos grasos (FAO). Se sabía que bloquear la FAO con el fármaco cardíaco ranolazina ralentizaba el surgimiento de células resistentes, pero no quedaba claro cómo mataba realmente a las células de melanoma.
Una vulnerabilidad oculta: daño en grasas impulsado por hierro
Los investigadores se centraron en la ferroptosis, una forma de muerte celular desencadenada cuando el hierro facilita reacciones químicas destructivas en ciertas grasas de las membranas celulares. Encontraron que las células de melanoma resistentes a BRAFi presentan muchas características que las dejan al borde de la ferroptosis: tienen niveles más bajos del antioxidante glutatión, cargan sus membranas con ácidos grasos poliinsaturados largos y proclives al daño, y muestran más lípidos de membrana oxidados que sus contrapartes sensibles al fármaco. Las muestras de tumores de pacientes que progresaron con inhibidores de BRAF mostraron el mismo patrón, con marcadores tanto de ferroptosis como de vías de combustión de grasas elevándose en conjunto. Esto sugiere que las células resistentes caminan por una cuerda floja: muy vulnerables al daño lipídico impulsado por el hierro, pero al mismo tiempo conectadas para suprimirlo.
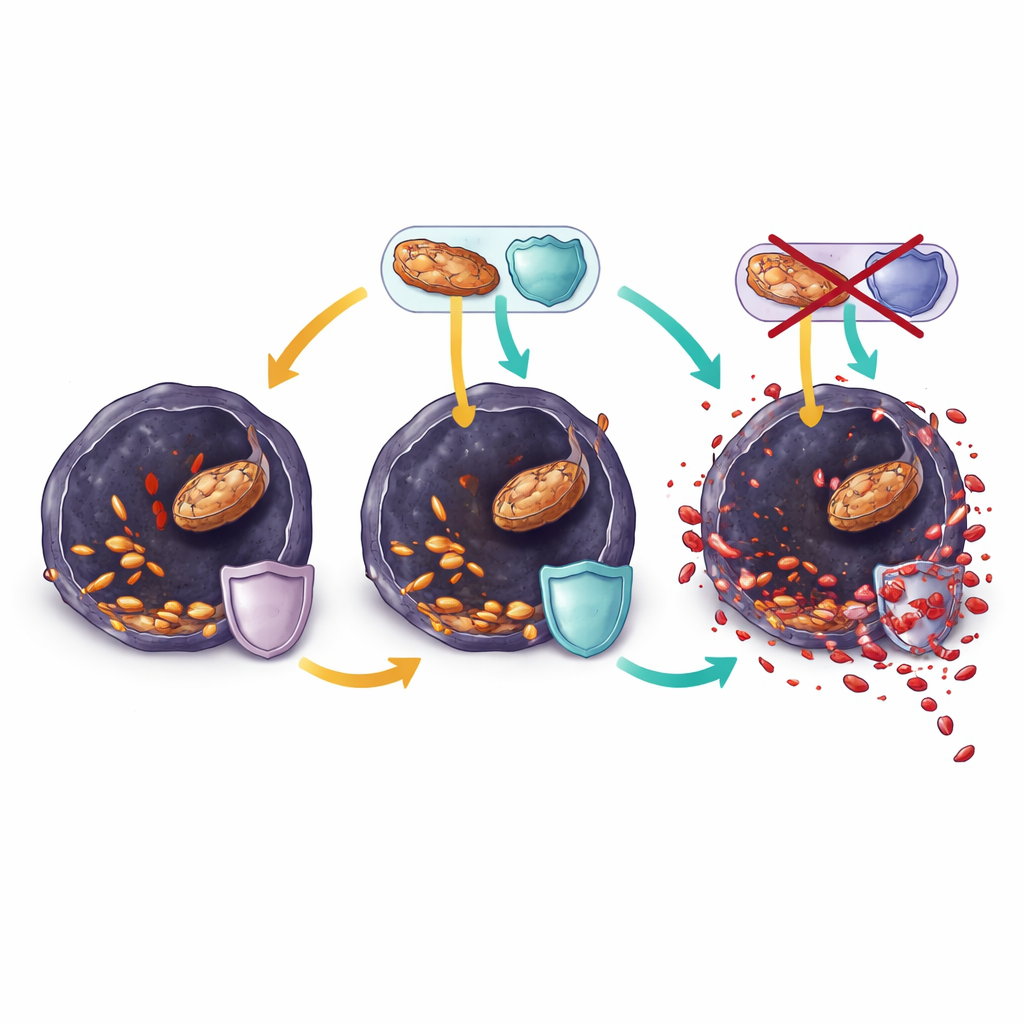
Ranolazina inclina la balanza hacia la muerte celular
En células de melanoma resistentes cultivadas en el laboratorio, la ranolazina redujo rápidamente la actividad de quema de grasas, agotó moléculas clave de energía y bajó aún más el glutatión. Al mismo tiempo, más ácidos grasos poliinsaturados se incorporaron en los lípidos de membrana, y aumentaron las señales de estrés oxidativo y daño lipídico. Estos cambios ralentizaron el crecimiento celular en pocas horas y pudieron revertirse con bloqueadores clásicos de la ferroptosis, lo que mostró que la ranolazina mataba a las células principalmente al empujarlas por el borde hacia la ferroptosis. Sin embargo, cuando los tumores en ratones finalmente escaparon al tratamiento combinado de BRAF y ranolazina, sus células se habían reconectado de nuevo. Mantuvieron niveles altos de enzimas que reparan lípidos oxidados y reponen moléculas protectoras, y remodelaron sus membranas para contener más grasas monoinsaturadas resistentes en lugar de poliinsaturadas vulnerables.
Señales hormonales ayudan a reconstruir las defensas del tumor
El equipo rastreó esta remodelación de membranas hasta enzimas llamadas MBOAT1 y MBOAT2, que intercambian grasas más seguras durante la renovación de fosfolípidos. Estas enzimas aumentaron notablemente en células resistentes a la ranolazina y en muchos tumores de pacientes que habían recaído con inhibidores de BRAF. Su actividad dependía del receptor de andrógenos (AR), un sensor hormonal más conocido en el cáncer de próstata. AR se unía a regiones de control de los genes MBOAT1 y MBOAT2 y aumentaba su actividad. Cuando los investigadores bloquearon AR con el fármaco para cáncer de próstata enzalutamida, los niveles de MBOAT1/2 cayeron y las células de melanoma se hicieron mucho más sensibles a agentes inductores de ferroptosis. Este efecto se observó en distintos estados celulares del melanoma, tanto en células primitivas y altamente resistentes como en células más diferenciadas similares a las productoras de pigmento.
Combinar dos fármacos antiguos para burlar tumores resistentes
Puesto que la FAO y la remodelación lipídica controlada por AR ayudan por separado a que las células de melanoma escapen de la ferroptosis, los autores probaron si golpear ambas vías a la vez sería particularmente efectivo. En cultivos celulares, la combinación de ranolazina (que bloquea la quema de grasas y potencia el daño lipídico) con enzalutamida (que desactiva AR y sus enzimas protectoras de membrana) provocó una muerte celular ferroptótica extensa, especialmente en células que dependían en gran medida de la FAO y que habían cambiado al estado indiferenciado agresivo. Bajo condiciones que obligan a las células de melanoma a depender más de las grasas como combustible, esta combinación resultó aún más letal. El trabajo sugiere que una estrategia de doble terapia usando estos fármacos ya aprobados podría tanto retrasar la resistencia a tratamientos dirigidos a BRAF como hacer que los tumores resistentes, incluidos aquellos que atenúan el ataque inmune, sean más vulnerables al forzarlos hacia la ferroptosis.
Qué podría significar esto para los pacientes
Esta investigación dibuja un panorama detallado de cómo las células de melanoma, acorraladas por la terapia dirigida, remodelan su metabolismo y señalización hormonal para esquivar una forma letal de muerte celular basada en hierro y lípidos. Al revelar que las vías de quema de grasas y el receptor de andrógenos cooperan para mantener la ferroptosis bajo control, apunta a una vía práctica para eliminar esa red de seguridad. Aunque serán necesarios ensayos clínicos, la idea de reutilizar fármacos cardíacos y prostáticos junto con tratamientos existentes para el melanoma ofrece una vía prometedora hacia respuestas más duraderas y potencialmente mejores resultados para pacientes cuyos tumores tienden a recaer.
Cita: Redondo-Muñoz, M., Caballe-Mestres, A., Reisz, J.A. et al. Androgen receptor and fatty acid oxidation cooperate in ferroptosis evasion in BRAFi resistant melanoma. Cell Death Dis 17, 338 (2026). https://doi.org/10.1038/s41419-026-08578-4
Palabras clave: melanoma, ferroptosis, oxidación de ácidos grasos, receptor de andrógenos, resistencia a fármacos