Clear Sky Science · it
Recettore degli androgeni e ossidazione degli acidi grassi cooperano nell’evasione dalla ferroptosi nel melanoma resistente a BRAFi
Perché questo è importante per il trattamento dei tumori cutanei ostinati
I farmaci che bloccano il BRAF mutato, un interruttore chiave della crescita nel melanoma, hanno trasformato la cura delle persone con carcinoma cutaneo avanzato. Tuttavia molti tumori si riducono inizialmente solo per riemergere con forza mesi dopo. Questo studio indaga cosa permette a quei tumori di ricomparire restando vivi ed esplora un nuovo modo per spingerli verso una modalità di autodistruzione chiamata ferroptosi, usando in combinazione due farmaci già impiegati per cuore e prostata.
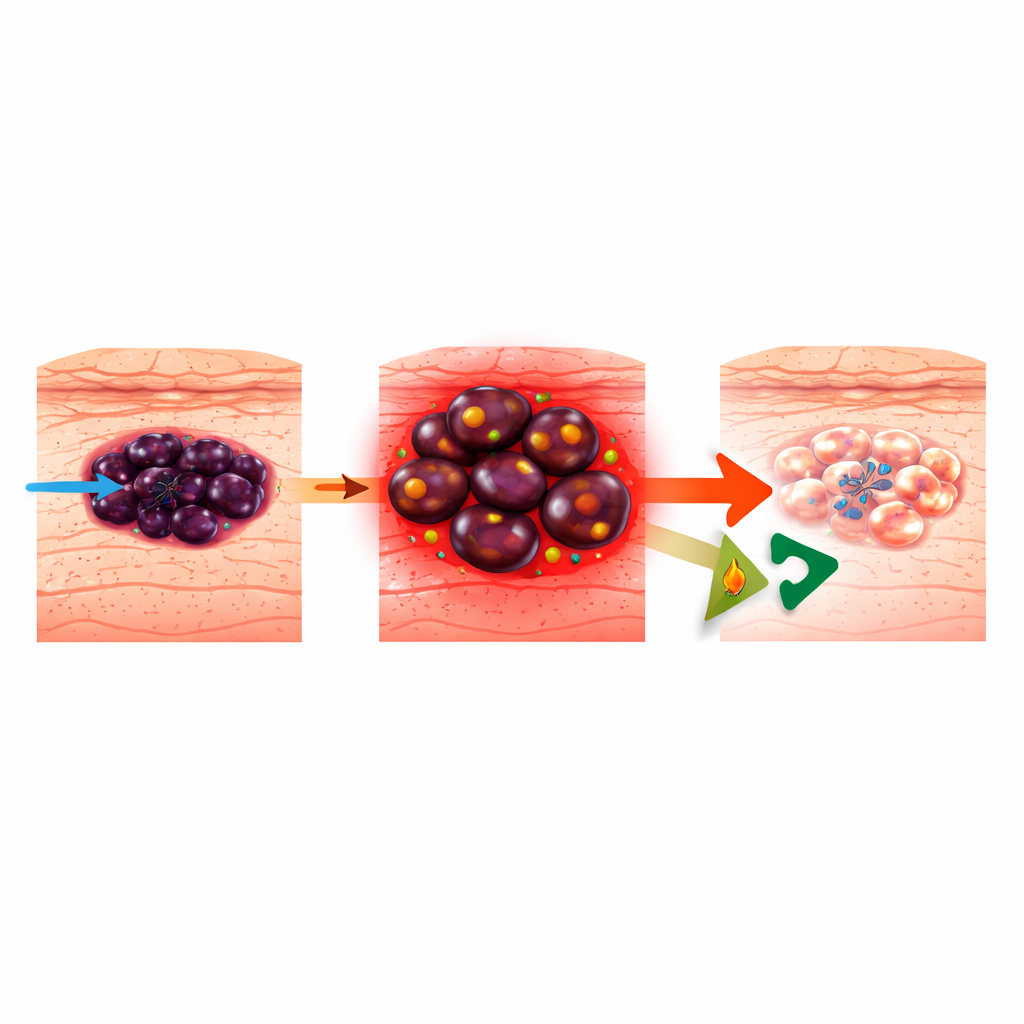
Come il melanoma impara a eludere i farmaci mirati
Il melanoma deriva dalle cellule che producono pigmento nella pelle ed è responsabile della maggior parte dei decessi per cancro cutaneo. Le terapie mirate moderne colpiscono la via BRAF–MEK iperattiva che guida molti melanomi, ma i tumori sono straordinariamente adattabili. Possono cambiare “stato cellulare”, passando da un’identità più matura e produttrice di pigmento a uno stato più primitivo, simile alla cresta neurale o indifferenziato, che è aggressivo e resistente ai farmaci. Lavori precedenti hanno mostrato che man mano che i melanomi diventano resistenti agli inibitori di BRAF (BRAFi), sempre più si alimentano bruciando grassi nei loro mitocondri, un processo chiamato ossidazione degli acidi grassi (FAO). Bloccare la FAO con il farmaco cardiaco ranolazina era noto rallentare l’ascesa delle cellule resistenti, ma non era chiaro come ciò uccidesse effettivamente le cellule di melanoma.
Una vulnerabilità nascosta: danno lipidico guidato dal ferro
I ricercatori si sono concentrati sulla ferroptosi, una forma di morte cellulare scatenata quando il ferro favorisce reazioni chimiche distruttive in certi grassi presenti nelle membrane cellulari. Hanno trovato che le cellule di melanoma resistenti a BRAFi presentano molte caratteristiche che le lasciano sul punto della ferroptosi: hanno livelli più bassi dell’antiossidante glutatione, arricchiscono le loro membrane con grassi polinsaturi lunghi e suscettibili al danno e mostrano lipidi di membrana più ossidati rispetto ai loro omologhi sensibili al farmaco. Campioni tumorali di pazienti progrediti durante l’uso di inibitori di BRAF mostravano lo stesso schema, con marcatori sia della ferroptosi sia delle vie di ossidazione dei grassi che aumentavano insieme. Questo suggerisce che le cellule resistenti camminano su una corda tesa — altamente vulnerabili al danno lipidico guidato dal ferro, ma allo stesso tempo cablate per sopprimerlo.
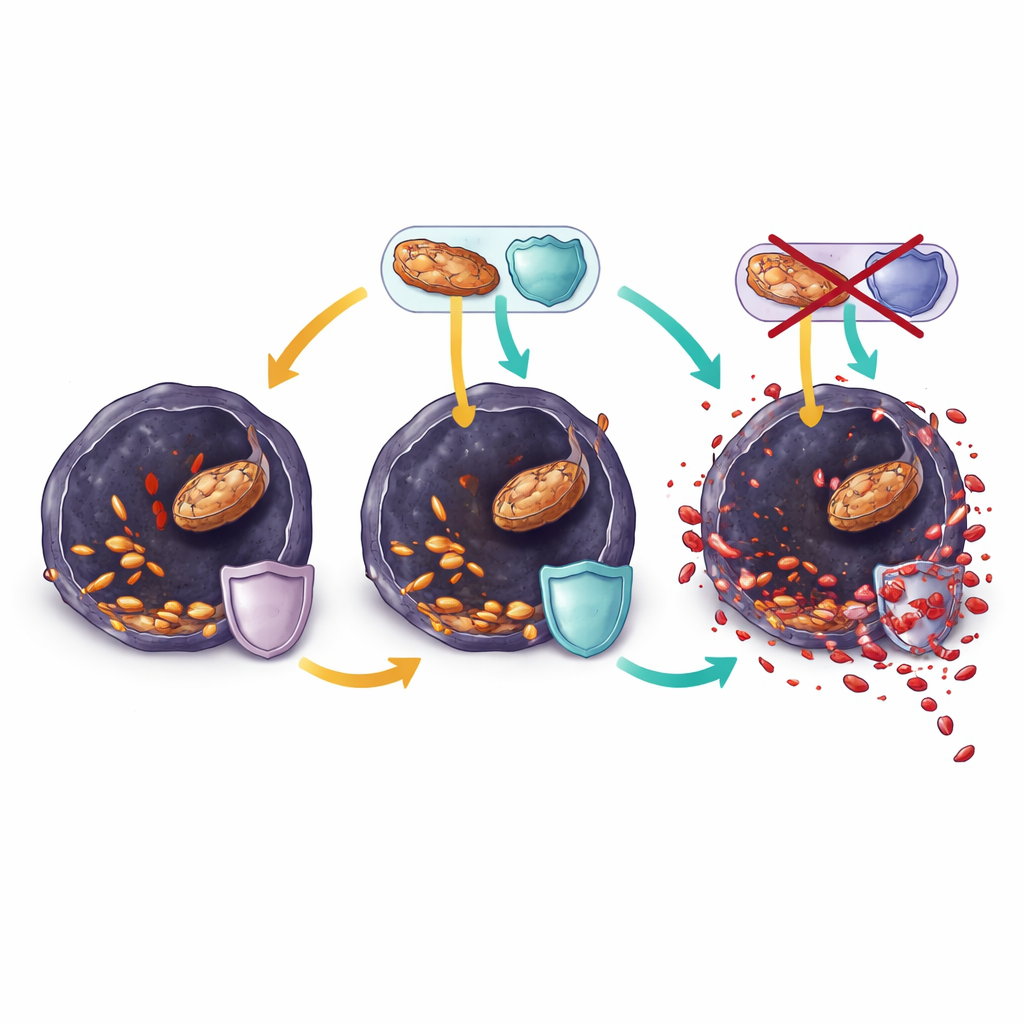
La ranolazina sposta l’equilibrio verso la morte cellulare
In cellule di melanoma resistenti coltivate in laboratorio, la ranolazina ha rapidamente ridotto l’attività di ossidazione dei grassi, esaurito molecole energetiche chiave e abbassato ulteriormente il glutatione. Contemporaneamente, più grassi polinsaturi venivano incorporati nei lipidi di membrana e i segni di stress ossidativo e danno lipidico sono aumentati. Questi cambiamenti hanno rallentato la crescita cellulare in poche ore e potevano essere invertiti dai classici bloccanti della ferroptosi, dimostrando che la ranolazina uccideva le cellule principalmente spingendole oltre il limite verso la ferroptosi. Tuttavia, quando i tumori nei topi alla fine eludevano il trattamento combinato con BRAF e ranolazina, le loro cellule si erano nuovamente riorganizzate. Mantenevano alti livelli di enzimi che riparano i lipidi ossidati e riforniscono molecole protettive, e ristrutturavano le membrane per contenere più grassi monoinsaturi resistenti invece di quelli polinsaturi vulnerabili.
I segnali ormonali aiutano a ricostruire le difese del tumore
Il gruppo ha ricondotto questa ristrutturazione delle membrane ad enzimi chiamati MBOAT1 e MBOAT2, che sostituiscono i grassi con altri più sicuri durante il rinnovamento dei fosfolipidi. Questi enzimi erano fortemente aumentati nelle cellule resistenti alla ranolazina e in molti tumori di pazienti ricaduti durante gli inibitori di BRAF. La loro attività dipendeva dal recettore degli androgeni (AR), un sensore ormonale più noto nel cancro della prostata. L’AR si legava a regioni di controllo dei geni MBOAT1 e MBOAT2 e ne aumentava l’attività. Quando i ricercatori bloccarono l’AR con il farmaco per il cancro della prostata enzalutamide, i livelli di MBOAT1/2 diminuirono e le cellule di melanoma divennero molto più sensibili agli agenti che inducono la ferroptosi. Questo effetto si osservava in diversi stati del melanoma, inclusi sia le cellule primitive altamente resistenti ai farmaci sia le cellule più differenziate simili a quelle produttrici di pigmento.
Accoppiare due vecchi farmaci per superare i tumori resistenti
Poiché la FAO e il rimodellamento lipidico controllato dall’AR aiutano ciascuno le cellule di melanoma a sfuggire alla ferroptosi, gli autori hanno testato se colpire entrambi contemporaneamente sarebbe particolarmente efficace. in coltura cellulare, la combinazione di ranolazina (che blocca la combustione dei grassi e aumenta il danno lipidico) con enzalutamide (che disarma l’AR e i suoi enzimi protettivi di membrana) ha causato una diffusa morte cellulare per ferroptosi, specialmente nelle celle che dipendevano fortemente dalla FAO e che si erano spostate nello stato indifferenziato aggressivo. In condizioni che costringono le cellule di melanoma a dipendere maggiormente dai grassi come carburante, questa combinazione è diventata ancora più letale. Il lavoro suggerisce che una strategia a doppia terapia con questi farmaci già approvati potrebbe sia ritardare la comparsa di resistenza ai trattamenti mirati al BRAF sia rendere i tumori resistenti, inclusi quelli che attenuano l’attacco immunitario, più vulnerabili forzandoli verso la ferroptosi.
Cosa potrebbe significare per i pazienti
Questa ricerca dipinge un quadro dettagliato di come le cellule di melanoma, spinte all’angolo dalla terapia mirata, rimodellino il loro metabolismo e la segnalazione ormonale per evitare una forma letale di morte cellulare basata su ferro e grassi. Svelando che le vie di ossidazione dei grassi e il recettore degli androgeni cooperano per tenere la ferroptosi sotto controllo, indica un modo praticabile per rimuovere quella rete di salvataggio. Pur richiedendo test clinici, l’idea di riproporre farmaci per cuore e prostata insieme ai trattamenti esistenti per il melanoma offre una strada promettente verso risposte più durature e potenzialmente migliori esiti per i pazienti i cui tumori sono soggetti a recidiva.
Citazione: Redondo-Muñoz, M., Caballe-Mestres, A., Reisz, J.A. et al. Androgen receptor and fatty acid oxidation cooperate in ferroptosis evasion in BRAFi resistant melanoma. Cell Death Dis 17, 338 (2026). https://doi.org/10.1038/s41419-026-08578-4
Parole chiave: melanoma, ferroptosi, ossidazione degli acidi grassi, recettore degli androgeni, resistenza ai farmaci