Clear Sky Science · ru
Сравнительный анализ архитектур множественного обучения на примерах от фрагментов до патологии для выявления и градации рака простаты с помощью внимания и слабо контролируемого обучения
Почему это важно для пациентов и врачей
Рак простаты — одно из наиболее распространённых онкологических заболеваний у мужчин; оценка его тяжести по слайсам под микроскопом напрямую влияет на выбор лечения. Сегодня эта градация занимает много времени, может варьировать между патологами и трудно масштабируется по мере старения населения. В исследовании показано, что современные методы искусственного интеллекта способны определять степень тяжести по цифровым слайзам, требуя значительно меньше ручных разметок, чем ранее, при этом оставаясь понятными для врачей. Это делает подход реалистичным кандидатом для поддержки повседневной диагностики в обычных больницах, а не только в исследовательских лабораториях.
От гигантских слайдов к крошечным фрагментам изображения
Современные сканеры превращают тонкий срез ткани предстательной железы в огромную цифровую картинку, часто размером 20 000 на 20 000 пикселей. Большая часть такого изображения — фон, а даже полезная ткань слишком велика, чтобы подать её в типичную модель целиком. Авторы решили эту проблему, разрезав каждый слайд на множество небольших квадратных «патчей» ткани, словно превратив плакат в пазл. Они тщательно определили только настоящие области ткани, отфильтровали пустые участки и артефакты и сгенерировали координатные карты, указывающие компьютеру, где именно брать образцы. Исследователи опробовали четыре стратегии разреза — с большими и малыми квадратами, с перекрытием и без — и в итоге получили более 31 миллиона патчей из более чем 10 600 слайдов в крупном публичном наборе данных по раку простаты PANDA. 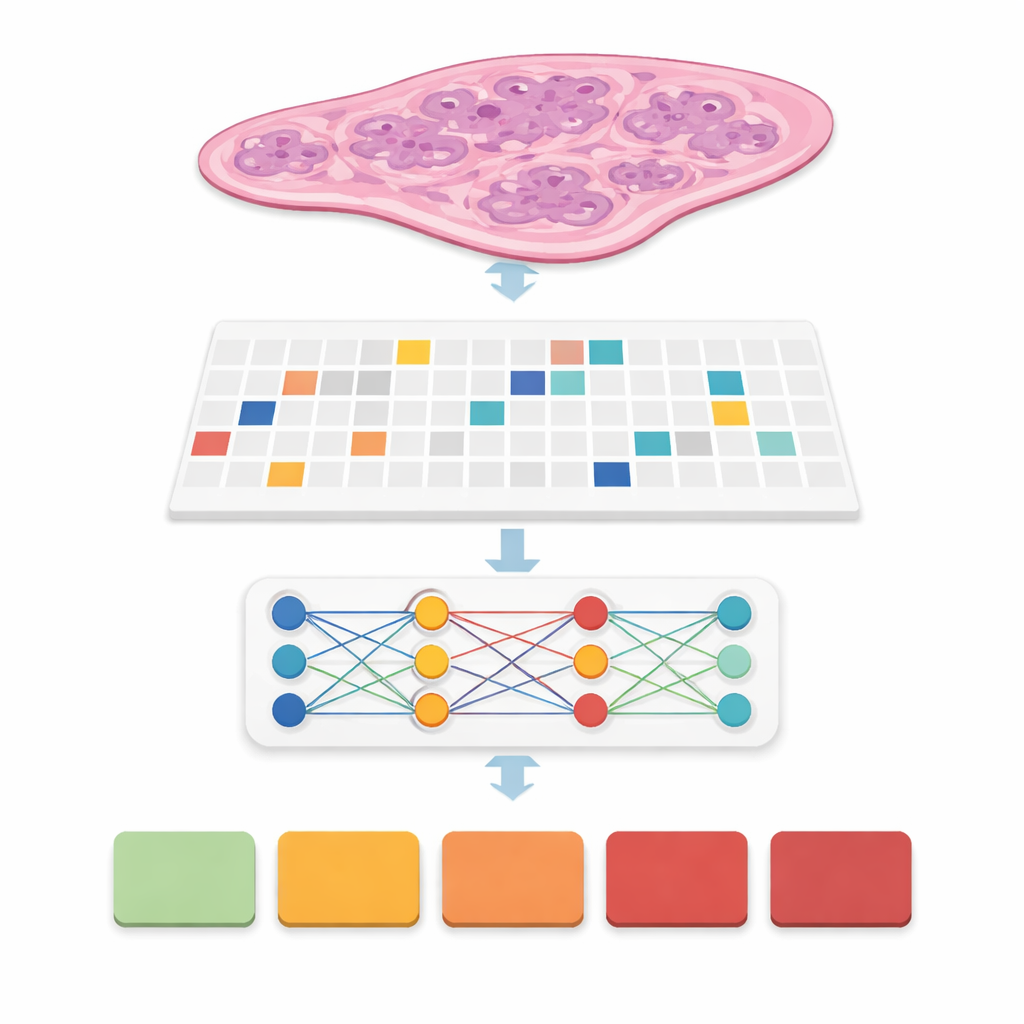
Обучение компьютеров распознавать рак без покадровых меток
Во многих предыдущих системах экспертам приходилось вручную обводить каждое очаговое поражение — трудоёмкая операция, затрудняющая применение в реальной практике. В этой работе команда использовала подход, называемый слабой супервизией: компьютеру доступна лишь метка на уровне слайда, например итоговая группа градации от 0 (доброкачественно) до 5 (наиболее агрессивно), без подробных внутренних разметок. Каждый слайд становится «мешком» патчей, и специальные модели учатся выделять те патчи, которые важны для предсказания общей градации. Эта группа методов, известная как множественное обучение экземпляров, позволяет модели самостоятельно обнаруживать паттерны желез и клеток, отличающие лёгкое от агрессивного заболевания, значительно снижая рабочую нагрузку патологов при обучении.
Сравнение множества блоков ИИ лицом к лицу
Вместо того чтобы предлагать одну новую модель, авторы сформировали детальный бенчмарк. Они сочетали шесть ведущих архитектур множественного обучения экземпляров с тремя разными извлекателями признаков, или «кодировщиками», которые превращают каждый патч в насыщенный числовой отпечаток. Один кодировщик был классической моделью компьютерного зрения, обученной на повседневных фотографиях, а остальные — крупными «фундаментальными» моделями, тренированными специально на сотнях тысяч слайдов патологии. Все комбинации прогоняли в четырёх настройках патчей и при пяти фолдах кросс‑валидации, что дало 360 запусков обучения и 72 основных конфигурации. Производительность оценивали по точности, нескольким типам F‑мер и квадратичной взвешенной каппа — статистике, которая вознаграждает прогнозы, близкие к решению эксперта, даже если они не идеально точны.
Оптимум найден: небольшие перекрывающиеся патчи и фундаментальная модель патологии
Чёткое преимущество показала комбинация относительно небольших патчей ткани (256 на 256 пикселей) с перекрытием 50%, кодированных моделью‑фундаментом UNI2 и агрегированных методом внимания с низким рангом ILRA‑MIL. Такое сочетание достигало примерно 79% точности и очень высокой квадратичной взвешенной каппа чуть выше 0,90, что приближалось к уровню согласия между экспертами в оригинальном конкурсе PANDA. Меньшие перекрывающиеся патчи давали модели и тонкие клеточные детали, и достаточный контекст, а кодировщик, обученный на патологии, явно превосходил универсальную сеть, натренированную на фотографиях, на 15–20 процентных пунктов по точности. Важно, что авторы показали достижимость этих улучшений с доступными облачными ресурсами, используя распределённые вычисления на публичных платформах вместо дорогих специализированных кластеров. 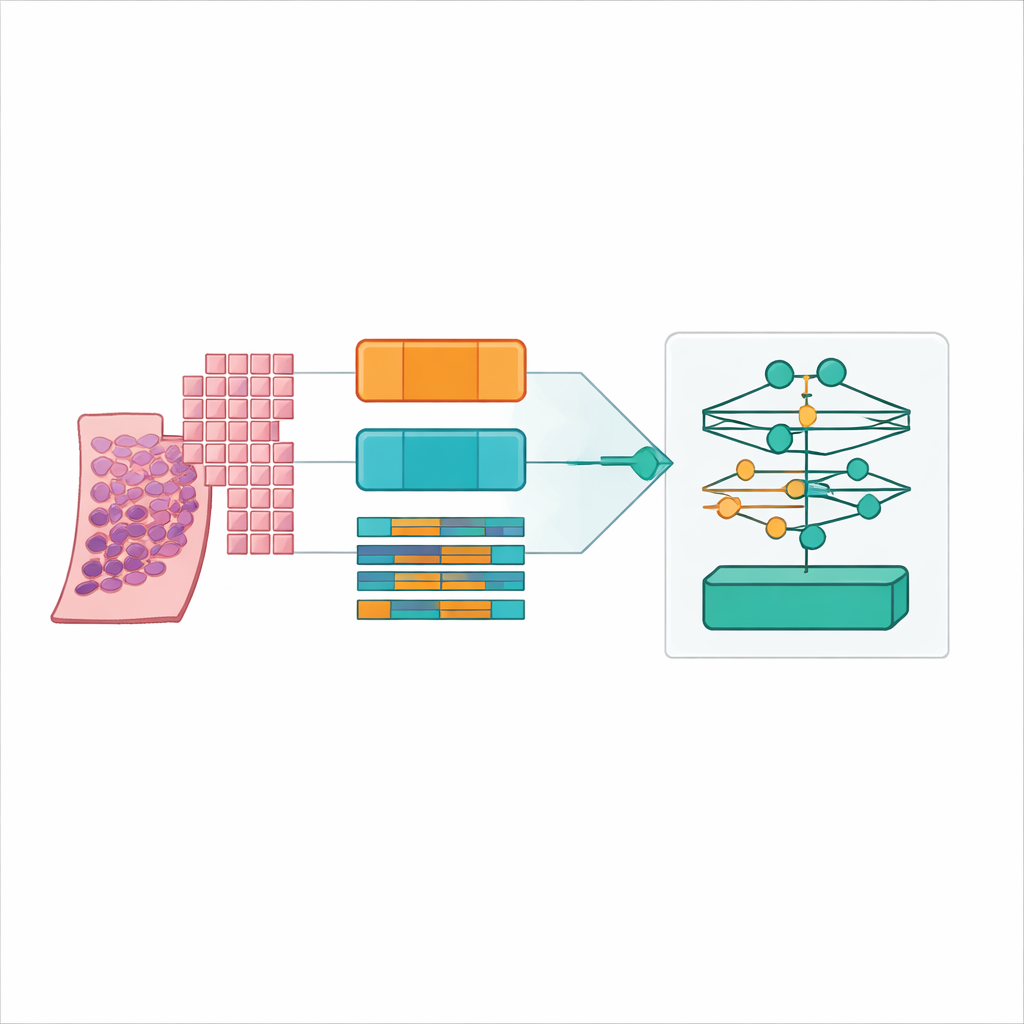
Делать решения ИИ видимыми для патологоанатомов
Для любого инструмента, который может повлиять на лечение, точности недостаточно; врачам важно понимать, почему он принимает то или иное решение. Исследователи встроили карты внимания и тепловые карты Grad‑CAM, которые подчёркивают области слайда, повлиявшие на предсказание. Эти визуальные объяснения можно накладывать на изображение ткани, чтобы патологоанатом убедился, что модель действительно фокусируется на раковых железах или агрессивных паттернах, а не на шуме или доброкачественных структурах. Такой акцент на интерпретируемости в сочетании с веб‑интерфейсом и детально описанным рабочим процессом от сырого слайда до предсказания призван облегчить внедрение и независимую валидацию в клинических лабораториях.
Что это значит для будущего ухода при раке простаты
Проще говоря, исследование демонстрирует, что тщательно спроектированная система ИИ может градуировать рак простаты по цифровым слайдам с производительностью, близкой к специалистам‑патологам, без необходимости исчерпывающей ручной обводки каждого обучающего слайда. Наиболее эффективный рецепт — множество маленьких перекрывающихся плиток изображения и крупный кодировщик, обученный на патологии, подающий признаки в основанную на внимании модель, которая может указывать обратно на ткань, на которую опиралась. Хотя работа по‑прежнему опирается на один крупный набор данных и требует более широкого тестирования между больницами, она открывает реалистичный путь к более быстрой, более последовательной и более доступной диагностике рака простаты, особенно в регионах с дефицитом опытных патологоанатомов.
Цитирование: Butt, N.A., Sarwat, D., Noya, I.D. et al. Benchmarking multiple instance learning architectures from patches to pathology for prostate cancer detection and grading using attention-based weak supervision. Sci Rep 16, 11535 (2026). https://doi.org/10.1038/s41598-026-39196-x
Ключевые слова: рак простаты, цифровая патология, слабо контролируемое обучение, множественное обучение экземпляров, вычислительная патология