Clear Sky Science · he
השוואת ארכיטקטורות למידת מקרים מרובים מתמונות חתוכות לפתולוגיה לזיהוי וסיווג סרטן הערמונית באמצעות השגחה חלשה מבוססת תשומת לב
מדוע זה חשוב למטופלים ולרופאים
סרטן הערמונית הוא אחד הסוגים השכיחים ביותר של סרטן בקרב גברים, והחלטה לגבי חומרת הממצאים משקפת ישירות את בחירות הטיפול. היום תהליך הדירוג הזה איטי, עשוי להשתנות בין פתולוגים, וקשה להרחבה ככל שאוכלוסיות מזדקנות. המחקר מראה כיצד בינה מלאכותית מודרנית יכולה ללמוד להעריך חומרת סרטן משקפים דיגיטליים תוך שימוש בהרבה פחות סימונים אנושיים מאשר בעבר, ובמקביל להישאר מובן לרופאים. זה הופך את הגישה למועמד ריאלי לתמיכה באבחון יומי בבתי חולים אמיתיים ולא רק במעבדות מחקר.
משקפים ענקיים ליחידות תמונה זעירות
סריקות מודרניות ממירות פרוסת רקמה דקה של הערמונית לתמונה דיגיטלית ענקית, לעתים בגודל של 20,000 על 20,000 פיקסלים. רוב התמונה הוא רקע, ואף רקמה מועילה גדולה מדי כדי להזין אותה למודל מחשב טיפוסי בבת אחת. החוקרים פתרו זאת על ידי חיתוך כל משטח שלם להרבה "תבניות" מרובעות קטנות של רקמה, כמו להפוך פוסטר לפאזל. הם זיהו בקפידה רק את אזורי הרקמה האמיתיים, סיננו אזורים ריקים ואומללים, ויצרו מפות קואורדינטות שהודיעו למחשב היכן לדגום בדיוק. הם בדקו ארבע אסטרטגיות חיתוך שונות, בשילוב ריבועים גדולים וקטנים ובאופן חופף או לא חופף, ולבסוף הפיקו יותר מ‑31 מיליון תבניות מיותר מ‑10,600 משטחים בערכה ציבורית גדולה של סרטן הערמונית המכונה PANDA. 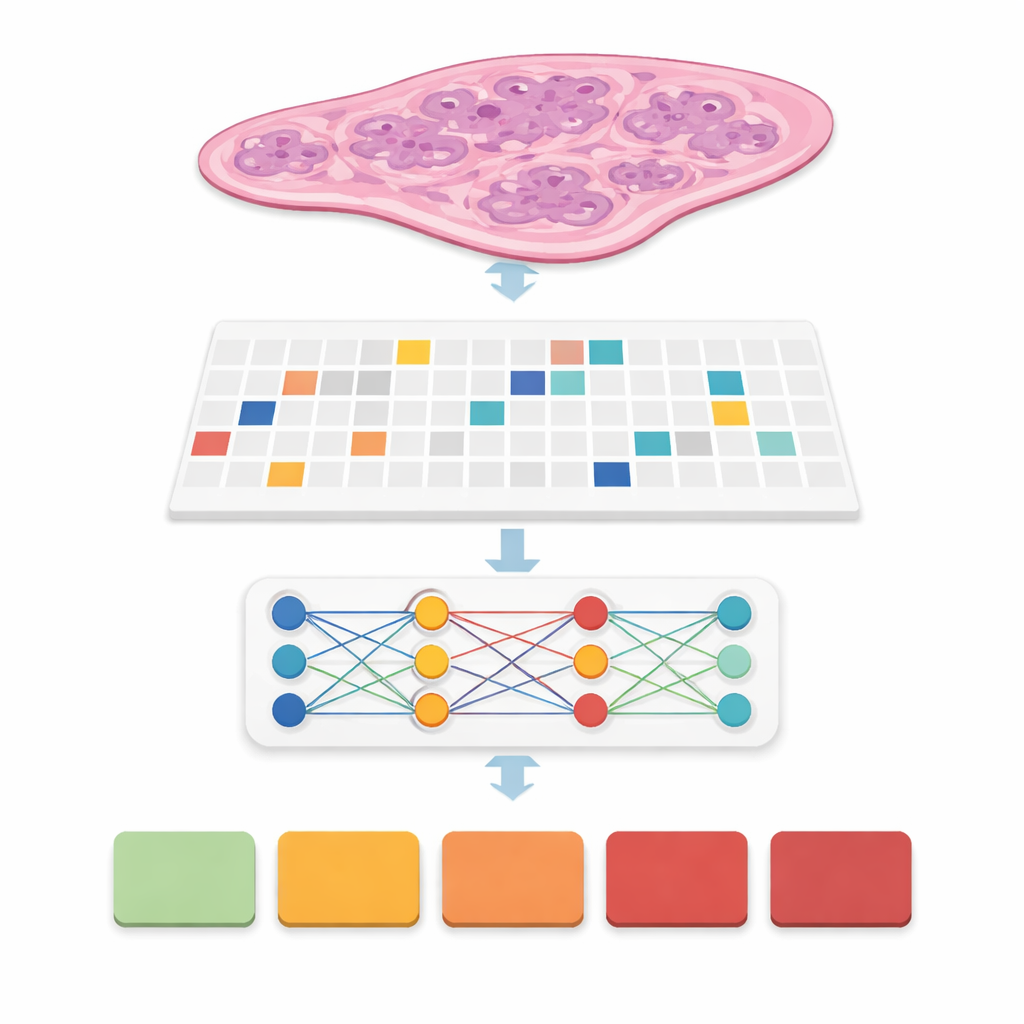
ללמד מחשבים לראות סרטן ללא תיוג פיקסל-אחר-פיקסל
ברבים מהמערכות הקודמות נדרשו מומחים לצייר מתארים מדויקים סביב כל מוקד סרטן, שלב הצורך בזמן שהופך פריסה בעולם האמיתי למסורבלת. כאן הצוות השתמש בגישת השגחה חלשה: המחשב רואה רק תווית ברמת המשטח, כמו דרוג גידול סופי מקבוצה 0 (שפיר) עד 5 (האגרסיבי ביותר), ללא סימונים מפורטים בפנים. כל משטח הופך ל"שק" של תבניות, ומודלים מיוחדים לומדים אילו תבניות חשובות לחיזוי הדירוג הכולל. משפחת השיטות הזו, המכונה למידת מקרים מרובים, מאפשרת למחשב לגלות דפוסים של בלוטות ותאים שמבדילים בין מחלה מתונה לאגרסיבית תוך קיצוץ ניכר בעומס העבודה של הפתולוגים בזמן האימון.
השוואה ישירה בין רבות מרכיבי ה‑AI
במקום להציע מודל חדש יחיד, המחברים בנו קריטריון השוואה מדוקדק. הם שילבו שישה עיצובים מובילים של למידת מקרים מרובים עם שלושה חלוצי חילוץ תכונות, או "מקודדים", שהופכים כל תבנית לטביעת אצבע מספרית עשירה. מקודד אחד היה מודל ראייה קלאסי שאומן על תמונות יום‑יומיות, בעוד האחרים היו מודלי יסוד גדולים שאומנו במיוחד על מאות אלפי משטחים פתולוגיים. הם הריצו את כל השילובים תחת ארבעה מצבי חיתוך וחמישה קיפולי חצייה (cross‑validation), מה שהניב 360 הרצות אימון ו‑72 תצורות מרכזיות. הביצועים נמדדו באמצעות דיוק, מספר סוגי מדדי F, וקאפה משוקללת ריבועית (quadratic weighted kappa), סטטיסטיקה שמעניקה פרס לקרבה בין דירוג המודל להחלטת המומחה גם כאשר היא אינה מדויקת לחלוטין.
מוצאים את הנקודה המתאימה: תבניות קטנות חופפות ומודל יסוד לפתולוגיה
המנצח הברור צץ כאשר הצוות השתמש בתבניות רקמה יחסית קטנות (256 על 256 פיקסלים) עם חפיפה של 50 אחוז, מקודדות על‑ידי מודל היסוד UNI2 ומאוגדות בשיטה מבוססת תשומת לב בדרגה נמוכה הנקראת ILRA‑MIL. שילוב זה הגיע לדיוק של כ‑79 אחוז וקאפה משוקללת ריבועית גבוהה מאוד של קצת מעל 0.90, מתקרב לרמות ההסכמה שנצפו בין מומחים בבאתגר PANDA המקורי. תבניות קטנות וחופפות סיפקו למודל גם פירוט תאי עדין וגם מספיק הקשר, בעוד שהמקודד המותאם לפתולוגיה הציג ביצועים טובים משמעותית מהרשת המאומנת על תמונות יומיומיות — הבדל של כ‑15–20 נקודות באחוזי הדיוק. חשוב לציין שהמחברים הראו שניצחונות אלה ניתנים להשגה באמצעות משאבי ענן נגישים, באמצעות חישוב מבוזר בפלטפורמות ציבוריות במקום אשכולות יקרות מיוחדות. 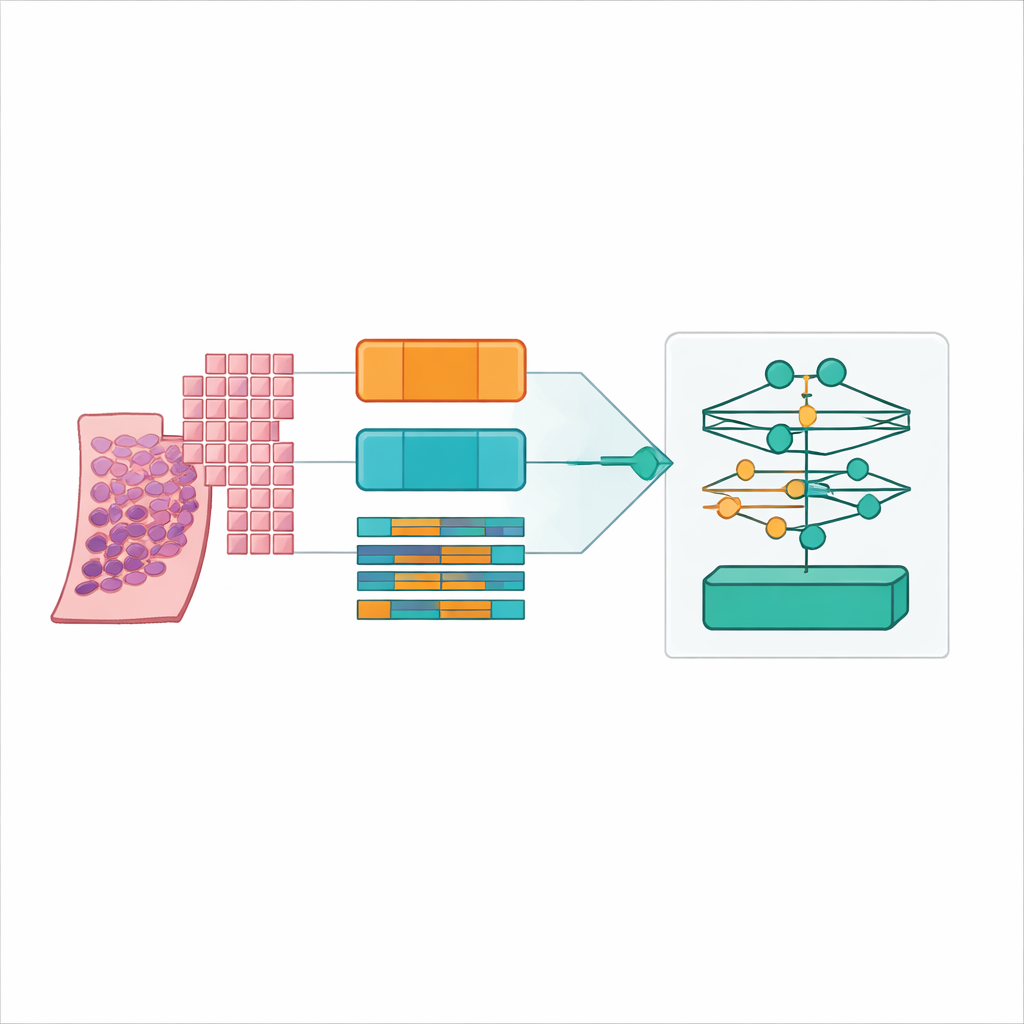
להפוך את החלטות ה‑AI לגלויות לפתולוגים
לכל כלי העלול להשפיע על טיפול, דיוק אינו מספיק; הרופאים זקוקים להבנה מדוע הוא נותן חיזוי מסוים. החוקרים שילבו מפות תשומת לב ומפות חום Grad‑CAM המדגישות אילו אזורים במשקף הובילו לחיזוי. הסברים חזותיים אלה ניתנים להטלה על תמונת הרקמה כך שפתחולוג יוכל לאמת שהמודל באמת מתמקד בבלוטות סרטניות או בדפוסים אגרסיביים ולא ברעש או במבנים שפירים. תשומת לב זו לפרשנות, בצירוף ממשק אינטרנטי וזרימת עבודה מתוארת במלואה מהמשטח הגולמי עד לחיזוי, נועדה להקל על אימוץ ובדיקה עצמאית במעבדות קליניות.
מה זה אומר לטיפול עתידי בסרטן הערמונית
במונחים פשוטים, המחקר מראה שמערכת בינה מלאכותית שעוצבה בקפידה יכולה לדרג סרטן הערמונית במשקפים דיגיטליים בביצועים קרובים לאלו של פתולוגים מומחים, ללא צורך בציור ידני מקיף על כל משטח אימון. המתכון היעיל ביותר משתמש בהרבה חתיכות תמונה קטנות וחופפות ומקודד גדול המאומן על פתולוגיה שמזין מודל מבוסס תשומת לב שיכול להצביע חזרה אל הרקמה שעליה הסתמך. למרות שהעבודה עדיין מתבססת על מאגר נתונים מרכזי אחד וזקוקה לבדיקות רחבות יותר בין בתי חולים, היא מציעה מסלול מציאותי לאבחון מהיר, עקבי ונגיש יותר של סרטן הערמונית, במיוחד באזור שבהם פתולוגים מומחים נדירים.
ציטוט: Butt, N.A., Sarwat, D., Noya, I.D. et al. Benchmarking multiple instance learning architectures from patches to pathology for prostate cancer detection and grading using attention-based weak supervision. Sci Rep 16, 11535 (2026). https://doi.org/10.1038/s41598-026-39196-x
מילות מפתח: סרטן הערמונית, פתולוגיה דיגיטלית, למידה בהשגחה חלשה, למידת מקרים מרובים, פתולוגיה חישובית