Clear Sky Science · ar
مقارنة معمارية التعلم متعدد العينات من الرقع إلى علم الأمراض لاكتشاف وتدرّيج سرطان البروستاتا باستخدام الإشراف الضعيف المعتمد على الانتباه
لماذا هذا مهم للمرضى والأطباء
يُعد سرطان البروستاتا واحداً من أكثر أنواع السرطان شيوعاً لدى الرجال، وقرار تحديد مدى شدّته من شرائح المجهر يؤثر مباشرة على خيارات العلاج. اليوم، عملية التدرّيج هذه بطيئة، وقد تختلف بين الأطباء المختصين، ومن الصعب توسيع نطاقها مع شيخوخة السكان. تُظهر هذه الدراسة كيف يمكن للذكاء الاصطناعي الحديث أن يتعلّم تقييم شدة السرطان من الشرائح الرقمية مع حاجته إلى علامات بشرية أقل بكثير من السابق، مع الحفاظ على قابلية الفهم للأطباء. وهذا يجعل منه مرشحاً واقعياً لدعم التشخيص اليومي في مستشفيات حقيقية بدلاً من أن يقتصر على مختبرات الأبحاث.
من الشرائح العملاقة إلى مربعات الصورة الصغيرة
تحوّل الماسحات الحديثة شريحة رقيقة من نسيج البروستاتا إلى صورة رقمية ضخمة، غالباً بحجم 20,000 في 20,000 بكسل. معظم تلك الصورة هو خلفية، وحتى النسيج المفيد كبير جدّاً لإدخاله في نموذج حاسوبي نموذجي دفعة واحدة. حلّ الباحثون هذه المشكلة بتقسيم كل شريحة كاملة إلى العديد من «الرقع» المربعة الصغيرة من النسيج، مثل تحويل ملصق إلى قطع بلاطية. اكتشفوا بعناية مناطق النسيج الحقيقية فقط، وفلتروا المناطق الفارغة والشوائب، وأنشأوا خرائط إحداثيات تخبر الحاسوب أين يأخذ العينات بالضبط. اختبروا أربع استراتيجيات لقطع الرقع—مزيج من مربعات كبيرة وصغيرة ومع تداخل أو بدونه—وانتجوا في النهاية أكثر من 31 مليون رقعة من أكثر من 10,600 شريحة في مجموعة بيانات عامة كبيرة لسرطان البروستاتا تُسمى PANDA. 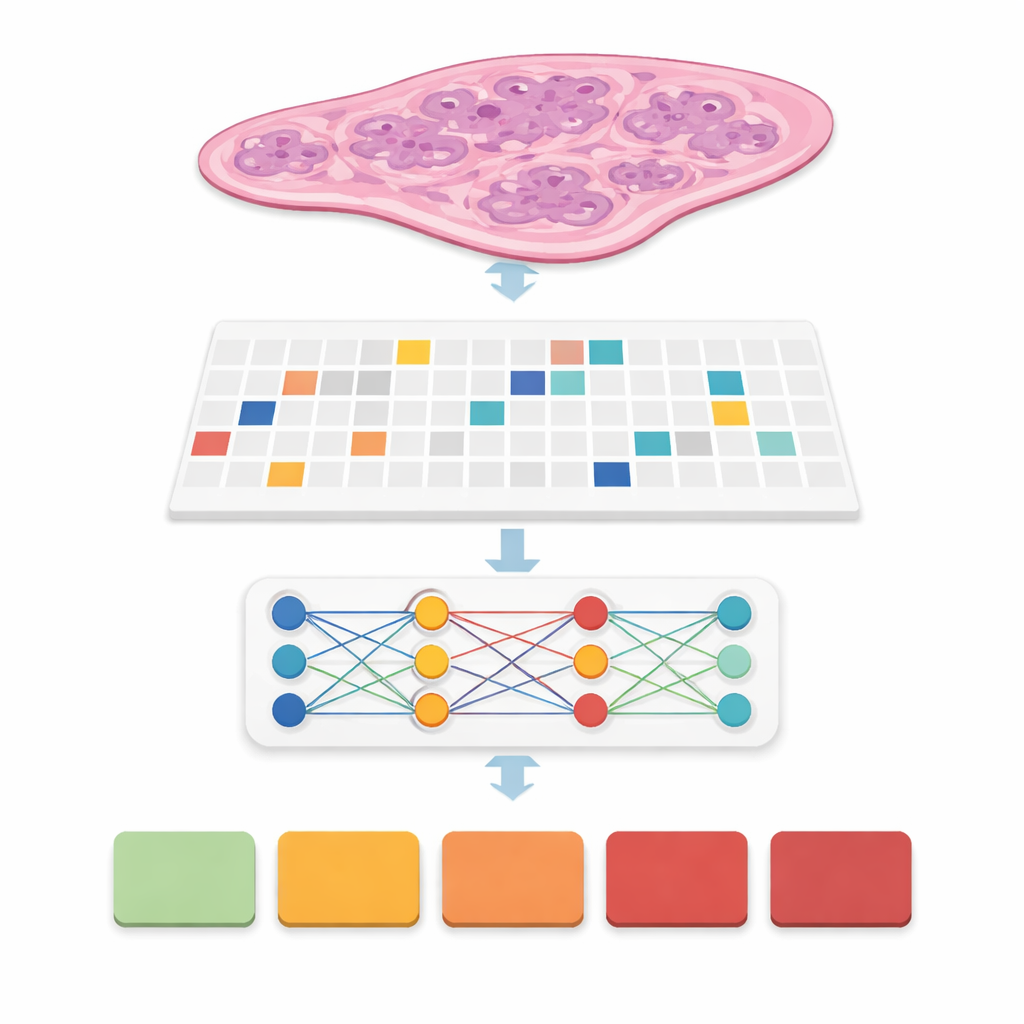
تعليم الحواسيب رؤية السرطان بدون تسميات بكسل‑ببكسل
في العديد من الأنظمة السابقة، كان على الخبراء رسم محيطات دقيقة حول كل بؤرة سرطانية، وهي خطوة تستغرق وقتاً كبيراً وتُصعّب النشر على نطاق عملي. هنا، استخدم الفريق منهجية تسمى الإشراف الضعيف: يرى الحاسوب فقط تسمية على مستوى الشريحة، مثل مجموعة الدرجة النهائية للسرطان من 0 (حميد) إلى 5 (الأكثر عدوانية)، دون أي علامات مفصّلة داخل الشريحة. تصبح كل شريحة «حقيبة» من الرقع، وتتعلم نماذج خاصة أي الرقع هي الأهم للتنبؤ بالدرجة الإجمالية. تتيح هذه العائلة من الطرق، المسماة التعلّم متعدد العينات، للحاسوب اكتشاف أنماط الغدد والخلايا التي تميّز المرض الخفيف عن العدواني مع تقليل عبء العمل على أطباء الأمراض أثناء التدريب.
مقارنة مكثّفة لمكوّنات الذكاء الاصطناعي
بدلاً من اقتراح نموذج جديد واحد، بنى المؤلفون معيار قياس دقيق. دمجوا ستة تصاميم رائدة للتعلّم متعدد العينات مع ثلاثة مُستخرجات ميزات مختلفة، أو «مشفرات»، التي تحوّل كل رقعة إلى بصمة رقمية غنية. كان أحد المشفرات نموذج رؤية تقليدي مدرّب على صور يومية، بينما درّبت المشفرات الأخرى نماذج «أساسية» كبيرة خصيصاً على مئات الآلاف من شرائح علم الأمراض. شغّلوا كل هذه التركيبات تحت أربع إعدادات للرقع وخمسة طيات من التحقق المتبادل، مما أسفر عن 360 تجربة تدريب و72 تهيئة أساسية. قيس الأداء بالدقة، وأنواع متعددة من درجات F، ومعامل كابا الموزون تربيعياً، وهو إحصاء يكافئ الحصول على درجة السرطان قريبة من قرار الخبير حتى لو لم تكن مطابقة تماماً.
إيجاد النقطة المثلى: رقع صغيرة متداخلة وموديل أساس لعلم الأمراض
ظهر الفائز الواضح عندما استخدم الفريق رقع نسيجية نسبياً صغيرة (256 في 256 بكسل) مع تداخل بنسبة 50٪، مشفّرة بواسطة نموذج الأساس UNI2 ومجمعة بواسطة طريقة انتباه منخفضة الرتبة تسمى ILRA‑MIL. وصلت هذه التركيبة إلى دقة تبلغ نحو 79٪ ومعامل كابا موزون تربيعياً عالٍ جداً يزيد قليلاً عن 0.90، مقتربة من مستويات الاتفاق بين الخبراء البشريين التي لوحظت في تحدي PANDA الأصلي. أعطت الرقع الصغيرة المتداخلة للنموذج تفاصيل خلوية دقيقة وسياقاً كافياً، بينما تفوق المشفر المخصّص لعلم الأمراض بوضوح على الشبكة العامة المدرّبة على الصور العادية بفارق 15–20 نقطة مئوية في الدقة. ومن المهم أن المؤلفين أظهروا أن هذه المكاسب قابلة للتحقيق بموارد سحابية متاحة، مستخدمين حوسبة موزّعة على منصات عامة بدلاً من عناقيد مكلفة مخصصة. 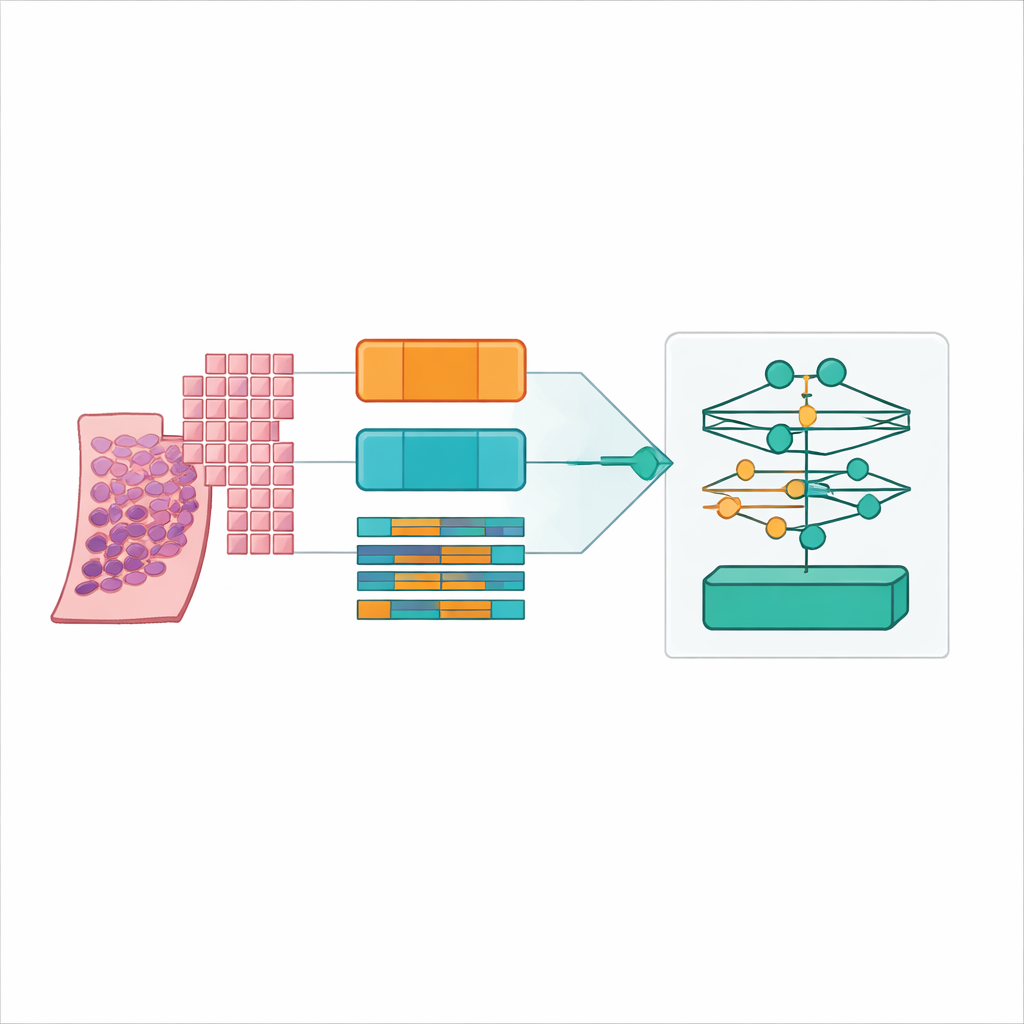
جعل قرارات الذكاء الاصطناعي مرئية لأطباء الأمراض
لأي أداة قد تؤثر على العلاج، لا يكفي أن تكون دقيقة فقط؛ يحتاج الأطباء إلى فهم سبب إصدارها قراراً معيناً. بنى الباحثون خرائط انتباه وخرائط حرارة Grad‑CAM تبرز المناطق من الشريحة التي دفعت التنبؤ. يمكن تراكب هذه التفسيرات البصرية على صورة النسيج حتى يتمكن اختصاصي الأمراض من التأكد من أن النموذج يركّز فعلاً على الغدد السرطانية أو الأنماط العدوانية بدلاً من الضوضاء أو التركيبات الحميدة. يُقصد من هذا الاهتمام بالتفسير، إلى جانب واجهة ويب معَرّفة بالكامل وسير عمل موصوف من الشريحة الخام حتى التنبؤ، تيسير الاعتماد والتحقق المستقل في مختبرات سريرية.
ما الذي يعنيه هذا لرعاية سرطان البروستاتا في المستقبل
بعبارات بسيطة، تظهر الدراسة أن نظام ذكاء اصطناعي مصمَّم بعناية يمكنه تدرّيج سرطان البروستاتا على الشرائح الرقمية بأداء يقترب من اختصاصيي الأمراض، دون الحاجة إلى رسم يدوي مستفيض على كل شريحة تدريب. الوصفة الأكثر فاعلية تستخدم العديد من مربعات الصورة الصغيرة المتداخلة ومشفر كبير مدرّب على علم الأمراض يغذّي نموذجاً معتمداً على الانتباه يمكنه الإشارة مرة أخرى إلى الأنسجة التي اعتمد عليها. ومع أن العمل لا يزال معتمداً على مجموعة بيانات رئيسية واحدة ويحتاج إلى اختبار أوسع بين المستشفيات، فإنه يوفر مساراً واقعياً نحو تشخيص أسرع وأكثر اتساقاً وأكثر توفراً لسرطان البروستاتا، خاصة في المناطق التي تعاني ندرة أخصائيي الأمراض.
الاستشهاد: Butt, N.A., Sarwat, D., Noya, I.D. et al. Benchmarking multiple instance learning architectures from patches to pathology for prostate cancer detection and grading using attention-based weak supervision. Sci Rep 16, 11535 (2026). https://doi.org/10.1038/s41598-026-39196-x
الكلمات المفتاحية: سرطان البروستاتا, علم الأمراض الرقمي, التعلّم تحت إشراف ضعيف, التعلّم متعدد العينات, الحوسبة في علم الأمراض