Clear Sky Science · ru
Последовательные транскрипционные волны и опосредованное NF-κB ремоделирование хроматина направляют лекарственно-индуцированную дедифференцировку в раке
Почему раковые клетки могут возвращаться после лечения
Современные противораковые препараты способны значительно уменьшать опухоли, но нередко болезнь возвращается. В этом исследовании изучается скрытый путь спасения, которым пользуются раковые клетки: вместо того чтобы быть безвозвратно уничтоженными или приобретать мутации, некоторые клетки временно «перематывают» себя в более примитивное, стволоподобное состояние, что помогает им пережить терапию. Отслеживая эти изменения во времени на уровне генов и хроматина (того, как упакована ДНК), авторы обнаружили поэтапную программу, управляемую путём распознавания стресса NF-κB/RelA, которая позволяет клеткам входить в лекарственно‑терпимую фазу и затем выходить из неё. Понимание этого обратимого процесса открывает новые подходы для продления эффективности лечения.
Клетки, выживающие за счёт упрощения специализации
Исследователи сосредоточились на меланомах с мутантным BRAF — частой мишени точечных препаратов. При обработке высокоадаптивных клеток меланомы ингибитором BRAF клетки не просто умирали или оставались прежними. Вместо этого они проходили через последовательность состояний: от пигментных меланоцитарных клеток к нейрально‑кремовым (neural‑crest‑like) клеткам, которые делятся медленно и переносят препараты, и, в конце концов, к ещё более примитивному мезенхимоподобному состоянию с высокой устойчивостью к множеству терапий. Примечательно, что после отмены препарата эти же клетки постепенно возвращались к исходной, чувствительной к лекарству идентичности, что свидетельствует о том, что резистентность обусловлена не постоянными изменениями ДНК, а гибким переходом состояний.
Кольцевая траектория вместо прямой линии
Чтобы упростить интерпретацию тысяч меняющихся генов, команда применила метод на основе теории информации и сжала данные до двух основных «волн» координированной активности генов. Первая, ранняя волна, включалась в течение нескольких дней после лечения и была связана с быстрыми изменениями хроматина и остановкой клеточного деления. Вторая, поздняя волна контролировала гены, определяющие клеточную идентичность и инвазивное поведение. Нанесение этих двух волн друг против друга показало, что путь в состояние лекарственной терпимости и путь возвращения не совпадают: клетки «помнили» историю лечения в конфигурации своего хроматина — явление, известное как гистерезис. Эта память означает, что даже при похожей активности генов упаковка ДНК может существенно различаться.
Как сигналы стресса перестраивают упаковку ДНК
Углубляясь, авторы обнаружили, что лечение нарушает антиоксидантную защиту клеток, что приводит к накоплению реактивных форм кислорода (ROS). Этот окислительный стресс активировал NF-κB/RelA, главный фактор ответа на стресс. После активации RelA перемещался в ядро и связывался со множеством участков генома вместе с двумя ремоделирующими хроматин ферментами — KDM5B и HDAC1. На сотнях целевых генов, включая ключевые гены идентичности меланомы, такие как SOX10 и MITF, это трио удаляло активирующие гистоновые метки и делало локальный хроматин менее доступным. Активность генов падала и оставалась низкой, пока присутствовал препарат, запирая клетки в медленно делящемся, лекарственно‑терпимом состоянии. Когда проникновение RelA в ядро блокировали, хроматинные метки восстанавливались, SOX10 возвращался, и клетки снова становились чувствительны к ингибированию BRAF.
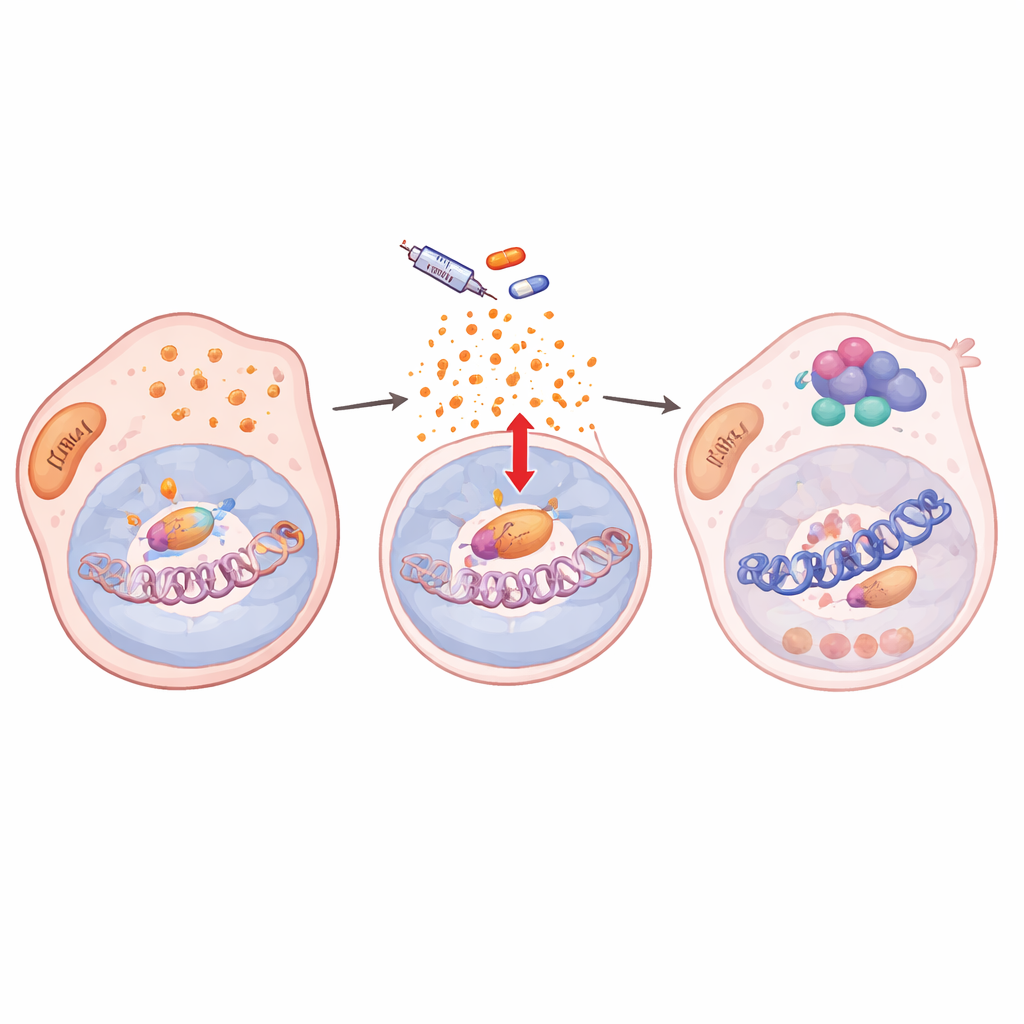
Пластичность, закодированная в хроматине, общая для разных опухолей
Далее команда спросила, почему одни опухоли более склонны к таким трансформациям, чем другие. В нескольких линиях клеток меланомы они обнаружили, что степень лекарственно‑индуцированных изменений коррелировала с тем, насколько открыт и активен был хроматин на целевых генах RelA до лечения. Линии с более «пермиссивным» хроматином демонстрировали более крупные переходы и сильную пользу от сочетания ингибиторов BRAF с препаратами, нацеленными на RelA или его хроматинные партнёры. Наконец, они показали, что похожий путь ROS–NF‑κB–хроматин управляет входом в состояния лекарственно‑терпимых упорников и в раках лёгкого и толстой кишки при терапии их драйверных онкогенов. Во всех случаях блокирование активации NF‑κB/RelA или подавление ROS ограничивало появление и повторный рост клеток‑упорников.
Что это значит для будущих лечений рака
Эта работа переосмысляет лекарственную устойчивость во многих раках как обратимую программу ответа на стресс, а не исключительно как генетическую проблему. Раковые клетки чувствуют индуцированный терапией окислительный стресс, активируют NF‑κB/RelA и с помощью сопряжённых ремоделеров хроматина временно выключают гены, поддерживающие их специализацию и чувствительность к препаратам. Поскольку этот процесс зависит от упаковки ДНК, а не от постоянных мутаций, его можно потенциально прервать. Результаты поддерживают стратегии лечения, объединяющие таргетные препараты с агентами, блокирующими сигнализацию NF‑κB/RelA или его хроматинные партнёрские белки, особенно в опухолях, чей хроматин настроен на такую пластичность. Предотвращая вход клеток в состояние упорников, такие комбинации могут сделать ремиссии глубже и долговечнее.
Цитирование: Su, Y., Liu, C., Lu, X. et al. Sequential transcriptional waves and NF-κB-driven chromatin remodeling direct drug-induced dedifferentiation in cancer. Nat Commun 17, 3228 (2026). https://doi.org/10.1038/s41467-026-71349-4
Ключевые слова: клетки-упорники, терпимые к лекарствам, сигнальная система NF-kB RelA, ремоделирование хроматина, пластичность раковых клеток, устойчивость к таргетной терапии