Clear Sky Science · ar
موجات نسخية متتابعة وإعادة تشكيل الكروماتين المدفوعة بـ NF-κB توجه إعادة التمايز المحفزة بالعقار في السرطان
لماذا يمكن لخلايا السرطان أن تعود بعد العلاج
يمكن للعلاجات السرطانية الحديثة أن تقلص الأورام بشكل كبير، لكن المرض غالبًا ما يعود. تستكشف هذه الدراسة مخرجًا خفيًا تهرب منه خلايا السرطان: فبدل أن تُقتل نهائيًا أو تتحور، تعود بعض الخلايا مؤقتًا إلى حالة أكثر بدائية تشبه الخلايا الجذعية تساعدها على النجاة من العلاج. من خلال تتبع هذه التغيرات مع الزمن على مستوى الجينات والكروماتين (طريقة تغليف الحمض النووي)، يكشف الباحثون عن برنامج خطوة بخطوة، يتحكم فيه مسار استشعار الإجهاد المسمى NF‑κB/RelA، يسمح للخلايا بالانتقال إلى حالة متسامحة مع الدواء ثم الخروج منها لاحقًا. فهم هذه العملية القابلة للعكس يقترح طرقًا جديدة للحفاظ على فعالية العلاج لفترة أطول.
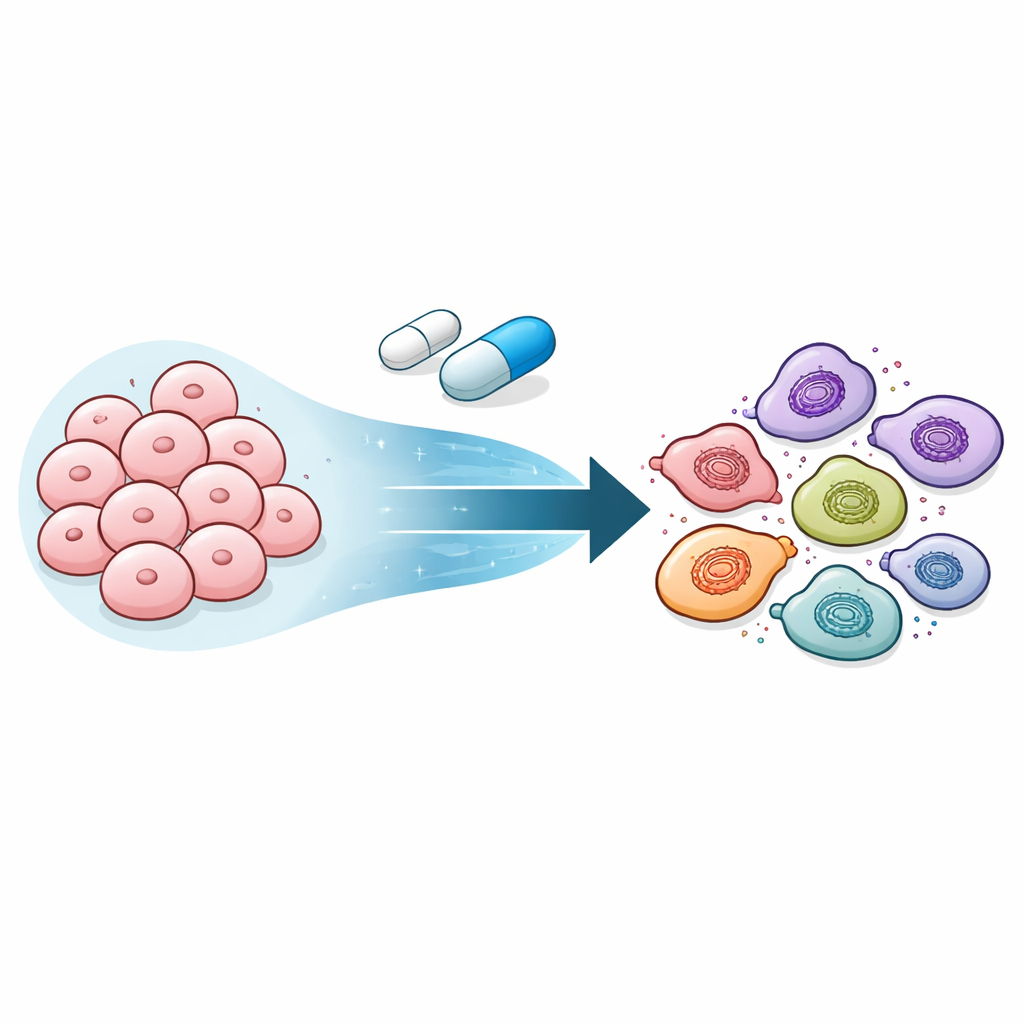
الخلايا التي تبقى على قيد الحياة عبر أن تصبح أقل تخصصًا
ركز الباحثون على الأورام الميلانينية المدفوعة بطفرات BRAF، وهو هدف شائع للأدوية الموجهة. عندما عالجوا خلايا ميلانين شديدة التكيف بمثبط BRAF، لم تمُت الخلايا ببساطة أو تبقَ كما هي. بل انتقلت عبر سلسلة من الهويات: من خلايا منتجة للأصباغ، إلى حالة شبيهة بالقشرة العصبية تنقسم ببطء وتتحمل الأدوية، وأخيرًا إلى حالة أكثر بدائية تشبه الحالة الميزنكيمية المقاومة بشدة للعديد من العلاجات. واللافت أنه عند إزالة الدواء، عادت هذه الخلايا تدريجيًا إلى هويتها الأصلية الحساسة للعقار، مما يدل على أن المقاومة لم تكن ناجمة عن طفرات دائمة في الحمض النووي بل عن تغير مرن في الحالة.
مسار دائري بدلاً من خط مستقيم
لفهم آلاف الجينات المتغيرة، استخدم الفريق طريقة مبنية على نظرية المعلومات لضغط البيانات إلى موجتين رئيسيتين من النشاط الجيني المنسق. الأولى، موجة مبكرة، ظهرت خلال أيام من العلاج وكانت مرتبطة بتغيرات سريعة في الكروماتين وتوقف انقسام الخلايا. الثانية، موجة لاحقة، سيطرت على جينات تحدد هوية الخلية وسلوكها الغازي. رسم هاتين الموجتين مقابل بعضهما كشف أن المسار نحو التحمل الدوائي والمسار العودة للخارج لم يتطابقا: كانت للخلايا ذاكرة عن تاريخ علاجها ضمن تركيب الكروماتين، سلوك معروف باسم التهيُّؤ (hysteresis). تعني هذه الذاكرة أنه حتى عندما يبدو النشاط الجيني مشابهًا، يمكن أن يكون تغليف الحمض النووي مختلفًا جدًا.
كيف تُعيد إشارات الإجهاد توصيل الكروماتين
بالتعمق أكثر، وجد المؤلفون أن العلاج الدوائي أعطاب دفاعات الخلايا المضادة للأكسدة، ما أدى إلى تراكم أنواع الأكسجين التفاعلية (ROS). هذا الإجهاد التأكسدي فعَّل NF‑κB/RelA، العامل الرئيسي في استجابة الإجهاد. بعد تفعيله، انتقل RelA إلى النواة وارتبط بالعديد من المواقع في الجينوم مع إنزيمين معدِّلين للكروماتين، KDM5B وHDAC1. في مئات الجينات المستهدفة، بما في ذلك جينات هوية الميلانين الأساسية مثل SOX10 وMITF، أزال هذا الثالوث علامات هستون النشطة وجعل الكروماتين المحلي أقل نفاذية. انخفض النشاط الجيني وبقي منخفضًا طالما استمر وجود الدواء، ما قفل الخلايا في حالة دورة بطيئة وتحمل دوائي. عندما تم منع دخول RelA إلى النواة، استعادت علامات الكروماتين ووَجهَت SOX10 انتعاشًا، وأصبحت الخلايا حساسة لمثبط BRAF مرة أخرى.
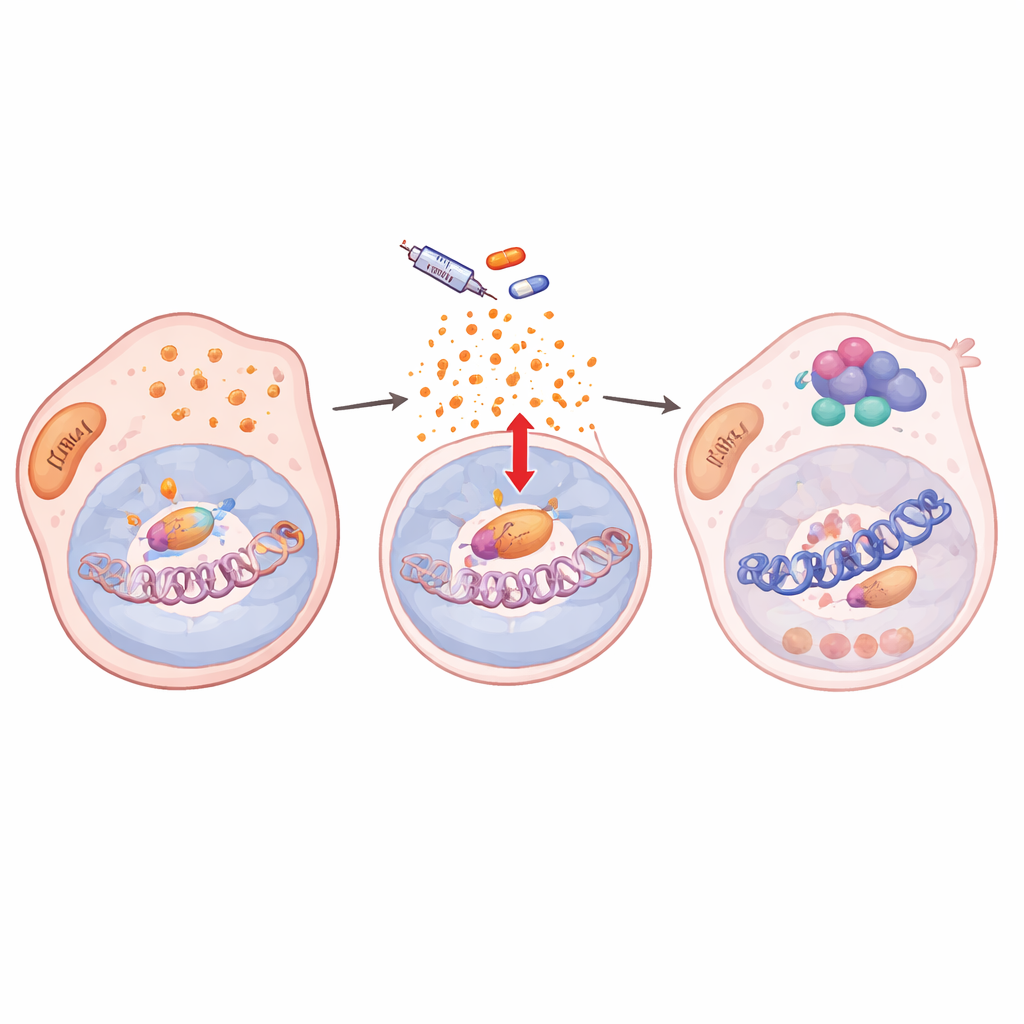
الليونة المشفرة في الكروماتين، والمشتركة عبر سرطانات متعددة
سأل الفريق بعد ذلك لماذا بعض الأورام أكثر ميلاً لهذا السلوك المتحول من غيرها. عبر عدة خطوط خلايا ميلانينية، وجدوا أن درجة التغير المحفز بالعقار تتبع إلى أي مدى كان الكروماتين عند جينات أهداف RelA منفتحًا ونشطًا قبل العلاج. الخطوط ذات الكروماتين الأكثر «تسامحًا» أظهرت انتقالات أكبر وفائدة أقوى من دمج مثبطات BRAF مع أدوية تستهدف RelA أو شركائه في تعديل الكروماتين. أخيرًا، أظهروا أن مسار ROS–NF‑κB–الكروماتين المماثل يدفع الدخول إلى حالات المستمرين المقاومة للعقاقير في سرطانات الرئة والقولون عند معالجتها ضد أورامها المحركة. في كل الحالات، أدى حجب تنشيط NF‑κB/RelA أو تخفيف ROS إلى تقليل ظهور وخِطاب (regrowth) خلايا المستمرين.
ما معنى ذلك لعلاجات السرطان المستقبلية
تعيد هذه العمل تصوير مقاومة الأدوية في许多 سرطانات على أنها برنامج استجابة للإجهاد قابل للعكس بدلاً من مشكلة جينية بحتة. تستشعر خلايا السرطان الإجهاد التأكسدي الناتج عن العلاج، تفعّل NF‑κB/RelA، وتستخدم معادلات إعادة تشكيل الكروماتين المرتبطة لإيقاف مؤقت لجينات تُبقيها متخصصة وحساسة للعقاقير. وبما أن هذه العملية تعتمد على كيفية تغليف الحمض النووي وليس على طفرات دائمة، فيمكن في المبدأ مقاطعتها. تدعم النتائج استراتيجيات علاجية تزاوج الأدوية الموجهة مع عوامل تحجب إشارة NF‑κB/RelA أو شركاءها المعدلين للكروماتين، خصوصًا في الأورام التي يكون كروماتينها مهيأً لهذه الليونة. عبر منع الخلايا من الدخول إلى حالة المستمرين من البداية، قد تجعل مثل هذه التركيبات فترات الهدوء أعمق وأكثر دوامًا.
الاستشهاد: Su, Y., Liu, C., Lu, X. et al. Sequential transcriptional waves and NF-κB-driven chromatin remodeling direct drug-induced dedifferentiation in cancer. Nat Commun 17, 3228 (2026). https://doi.org/10.1038/s41467-026-71349-4
الكلمات المفتاحية: خلايا المستمرين المقاومة للعقاقير, إشارة NF-kB RelA, إعادة تشكيل الكروماتين, ليونة خلايا السرطان, مقاومة العلاجات الموجهة