Clear Sky Science · ja
薬剤誘導性の脱分化を導く連続的な転写波およびNF-κB駆動のクロマチン再編成
治療後にがん細胞が回復する理由
現代のがん薬は腫瘍を劇的に縮小させることがありますが、しばしば疾患は再発します。本研究は、がん細胞が利用する隠れた逃避経路を探ります。つまり、多くの細胞が永久に死ぬか突然変異を起こすのではなく、治療を生き延びるために一時的により原始的な幹様状態へ「巻き戻す」ことがあるのです。遺伝子とクロマチン(DNAの包装様式)の変化を時間経過で追跡することで、著者らはストレス感知経路であるNF-κB/RelAにより制御される段階的プログラムを明らかにしました。これによりがん細胞は薬剤耐性状態へ入り、後にそこから出ることができます。この可逆的プロセスを理解することは、治療効果を長持ちさせる新たな方法を示唆します。
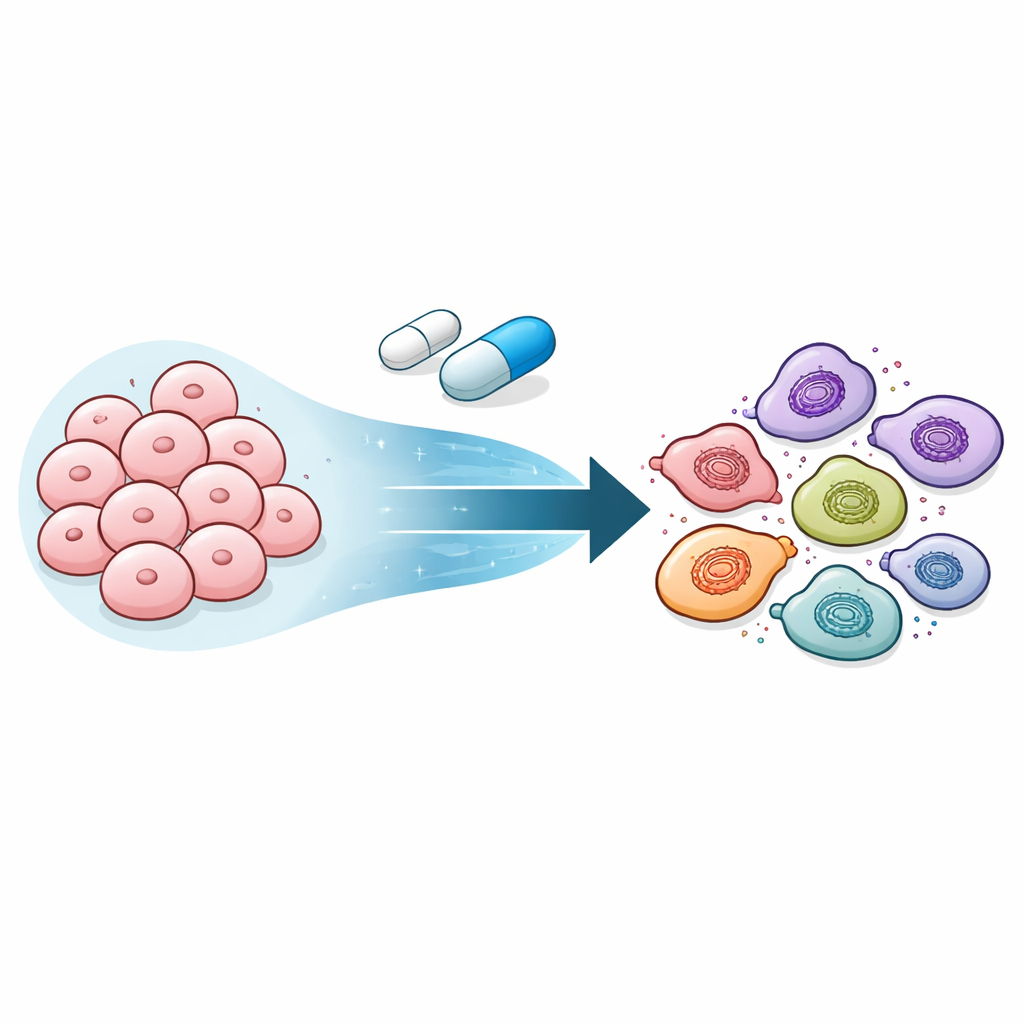
分化度を下げて生き残る細胞
研究者らは、精密医療薬の標的として一般的な変異BRAFで駆動されるメラノーマに注目しました。適応性の高いメラノーマ細胞にBRAF阻害薬を投与すると、細胞は単に死ぬか変わらずにいるのではありませんでした。むしろ、色素産生を行うメラノーマ細胞から、分裂が遅く薬剤を許容する神経堤様状態、さらに多くの治療に強く抵抗するより原始的な間葉様状態へと連続的に移行しました。驚くべきことに、薬剤を除去するとこれらの細胞は徐々に元の薬剤感受性のアイデンティティに戻り、抵抗性が恒久的なDNA変異によるものではなく状態の柔軟な変化によることを示しました。
直線ではなくループする経路
数千の変化する遺伝子を理解するため、チームは情報理論に基づく手法を用いてデータを2つの主要な協調遺伝子活動の「波」に圧縮しました。最初の早期波は治療から数日でオンになり、クロマチンの急速な変化と細胞分裂の停止に関連していました。後の二次波は細胞のアイデンティティや侵襲的挙動を定義する遺伝子を制御しました。この2つの波をプロットすると、薬剤耐性へ向かう経路とそこから戻る経路は重なっておらず、細胞はクロマチンの構成に治療履歴を記憶していること(ヒステリシス)を示しました。この記憶は、遺伝子発現が類似して見えても、基礎となるDNAのパッケージングが大きく異なり得ることを意味します。
ストレス信号がDNAの包装を書き換える仕組み
さらに掘り下げると、薬剤処理が細胞の抗酸化防御を乱し、活性酸素種(ROS)が蓄積することがわかりました。この酸化ストレスがNF-κB/RelAを活性化させるのです。RelAが活性化されると核内へ移行し、クロマチン修飾酵素のKDM5BおよびHDAC1とともにゲノムの多数の部位に結合しました。SOX10やMITFなどの主要なメラノーマ同一性遺伝子を含む数百の標的遺伝子で、この三者は活性化ヒストンマークを除去し局所的なクロマチンを不活性化しました。薬剤が存在する限り遺伝子活性は低下したままとなり、細胞は低増殖で薬剤耐性の状態に固定されました。RelAの核内移行を阻害するとクロマチンマークは回復し、SOX10は復活し、細胞は再びBRAF阻害薬に感受性を示しました。
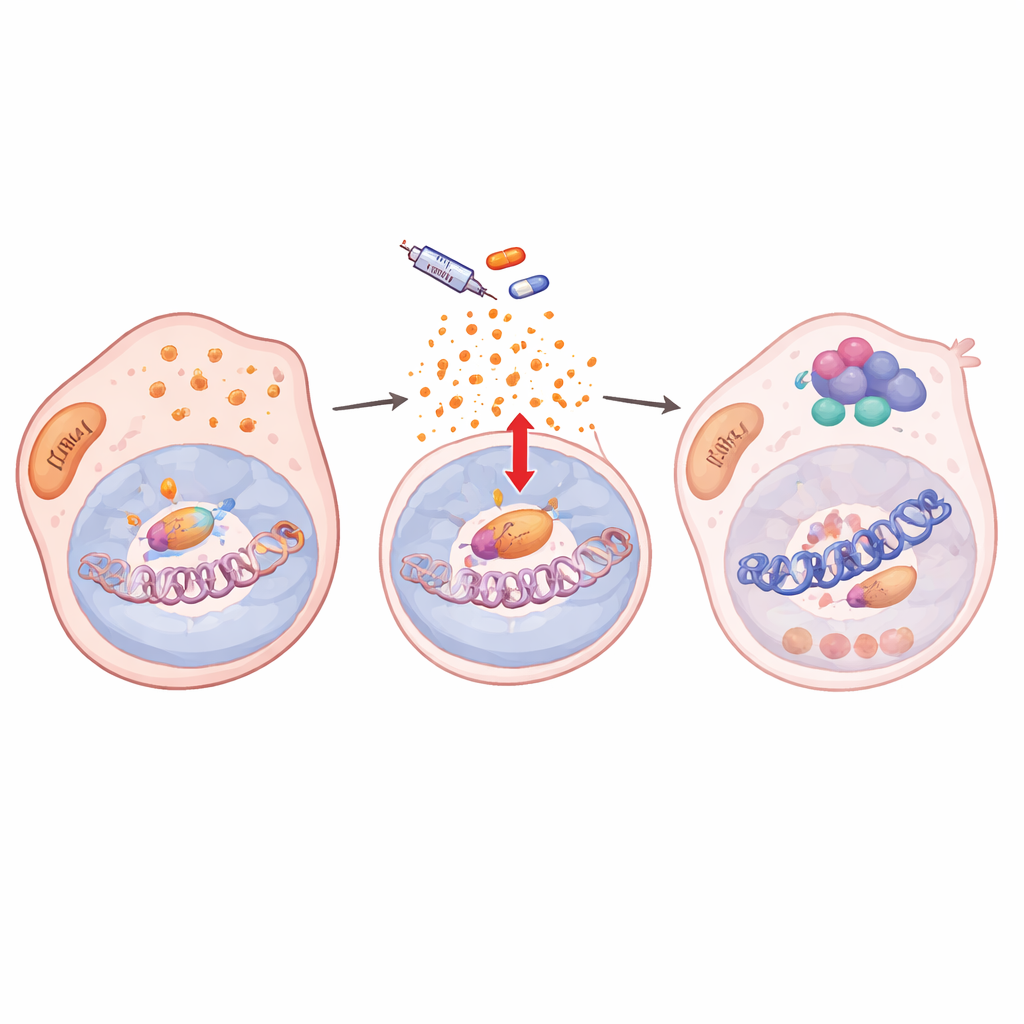
クロマチンに符号化された可塑性はがん種を超えて共有される
チームは、なぜ一部の腫瘍がこの形の変化を起こしやすいのかを問い直しました。複数のメラノーマ細胞株にわたり、薬剤誘導性の変化の程度は治療前のRelA標的遺伝子におけるクロマチンの開放性と活性性に相関していました。「許容的」なクロマチンを持つ株はより大きな移行を示し、BRAF阻害薬とRelAやそのクロマチンパートナーを標的とする薬剤の併用でより大きな利益を得ました。最後に、同様のROS–NF-κB–クロマチン経路が、各々のドライバーオンコジーンに対する治療を受ける肺がんや結腸がんでも薬剤耐性持続細胞への移行を駆動することを示しました。いずれの場合も、NF-κB/RelAの活性化を遮断するかROSを抑えることで、持続細胞の出現と再増殖が抑制されました。
将来のがん治療への示唆
この研究は、多くのがんにおける薬剤耐性を単なる遺伝学的問題ではなく可逆的なストレス応答プログラムとして再定義します。がん細胞は治療誘導性の酸化ストレスを感知し、NF-κB/RelAを活性化し、関連するクロマチンリモデラーを使って専門化と薬剤感受性を維持する遺伝子を一時的にオフにします。この過程は恒久的な変異ではなくDNAの包装様式に依存するため、妨げることが可能です。これらの知見は、標的薬とNF-κB/RelAシグナルやそのクロマチン修飾パートナーを阻害する薬剤を組み合わせる治療戦略を支持します。特にクロマチンがそのような可塑性に適した腫瘍では、持続状態への移行を未然に防ぐことで寛解をより深く、より長期化させる可能性があります。
引用: Su, Y., Liu, C., Lu, X. et al. Sequential transcriptional waves and NF-κB-driven chromatin remodeling direct drug-induced dedifferentiation in cancer. Nat Commun 17, 3228 (2026). https://doi.org/10.1038/s41467-026-71349-4
キーワード: 薬剤耐性持続細胞, NF-kB RelA シグナル伝達, クロマチン再編成, がん細胞の可塑性, 標的療法抵抗性