Clear Sky Science · he
גלי שעתוק סדרתיים ושינוי כרומטין מונע על‑ידי NF-κB מכוונים דעיכה מוכוונת‑תרופה בסרטן
למה תאי סרטן יכולים להתאושש אחרי טיפול
תרופות מודרניות יכולות לצמצם גידולים משמעותית, אך לעתים קרובות המחלה חוזרת. המחקר הזה חוקר מסלול בריחה חבוי שתאי הסרטן משתמשים בו: במקום להיהרס לצמיתות או לעבור מוטציה, חלק מהתאים "מגבירים" זמנית חזרה למצב פרימיטיבי יותר, דמוי‑הגזע, שמסייע להם לשרוד טיפול. במעקב אחרי השינויים לאורך זמן ברמות הגנים והכרומטין (אופן אריזת ה‑DNA), המחברים חושפים תוכנית שלב אחר שלב, הנשלטת על‑ידי מסלול חישה של מתח שנקרא NF‑κB/RelA, שמאפשרת לתאי הסרטן להיכנס ולצאת ממדינת סבילות לתרופה. הבנת התהליך ההפיך הזה מציעה דרכים חדשות לשמר את יעילות הטיפולים לאורך זמן רב יותר.
תאים ששרדו על ידי הפחתת ההתמחות
החוקרים התמקדים במלנומות מונעות על‑ידי BRAF מוטנטי, מטרה שכיחה של תרופות מדויקות. כאשר טיפלו בתאים מלנומה בעלי יכולת הסתגלות גבוהה באמצעות מעכבי BRAF, התאים לא פשוט מתו או נשארו ללא שינוי. במקום זאת הם עברו רצף זהויות: מתאי מלנומה מייצרי פיגמנט, למצב הדומה לנאורל‑קרסט שמתחלק לאט וסובלני לתרופות, ולבסוף למצב פרימיטיבי יותר, דמוי מזנכימלי, העמיד מאוד למספר טיפולים. באופן מרשים, כאשר ההוראה הוסרה, אותם תאים חזרו בהדרגה לזהותם המקורית הרגישה לתרופה, מה שמראה שהעמידות לא נבעה ממוטציות DNA קבועות אלא משינוי מצב גמיש.
מסלול מעגלי יותר מאשר קו ישר
כדי לפענח אלפי גנים שמשתנים, הצוות השתמש בשיטה מבוססת תורת המידע כדי לדחוס את הנתונים לשתי "גלים" עיקריים של פעילות גנים מתואמת. הראשון, גל מוקדם, הופעל בתוך ימים מטיפול וקושר לשינויים מהירים בכרומטין ולעצירת חלוקת התאים. הגל השני, מאוחר יותר, שלט בגנים שמגדירים זהות תא והתנהגות פולשנית. ציור שני הגלים זה מול זה חשף שהדרך לכיוון סבילות לתרופה והדרך חזרה לא חופפות: תאים זכרו את היסטוריית הטיפול שלהם בתצורת הכרומטין שלהם, התנהגות הידועה כהיסטירזיס. זיכרון זה משמעותו שגם כאשר פעילות הגנים נראית דומה, אריזת ה‑DNA הבסיסית יכולה להיות שונה מאוד.
איך אותות מתח משנים את אריזת ה‑DNA
בהעמקה, המחברים גילו שטיפול בתרופה הפר את מנגנוני ההגנה האנטי‑חמצוניים של התאים, מה שהוביל להצטברות של ריאקטיביות חמצונית (ROS). מתח חמצוני זה הפעיל את NF‑κB/RelA, פקטור מרכזי בתגובה למתח. לאחר שהופעל, RelA עבר לגרעין וקושר אתרים רבים בגנום יחד עם שתי אנזימי שינוי כרומטין, KDM5B ו‑HDAC1. במאות גנים‑מטרה, כולל גנים מרכזיים לזיהוי מלנומה כמו SOX10 ו‑MITF, הטריאד הזה הסיר סימני היסטון מאקטבים וגרם לכרומטין מקומי להיות פחות נגיש. פעילות הגנים ירדה ונשארה נמוכה כל עוד התרופה נוכחה, ונעילת התאים במצב חלוקה איטית וסובלנות לתרופה. כאשר נחסמה כניסת RelA לגרעין, סימני הכרומטין שוחזרו, SOX10 חזר לרמות קודמות, והתאים חזרו להיות רגישים לעיכוב BRAF.
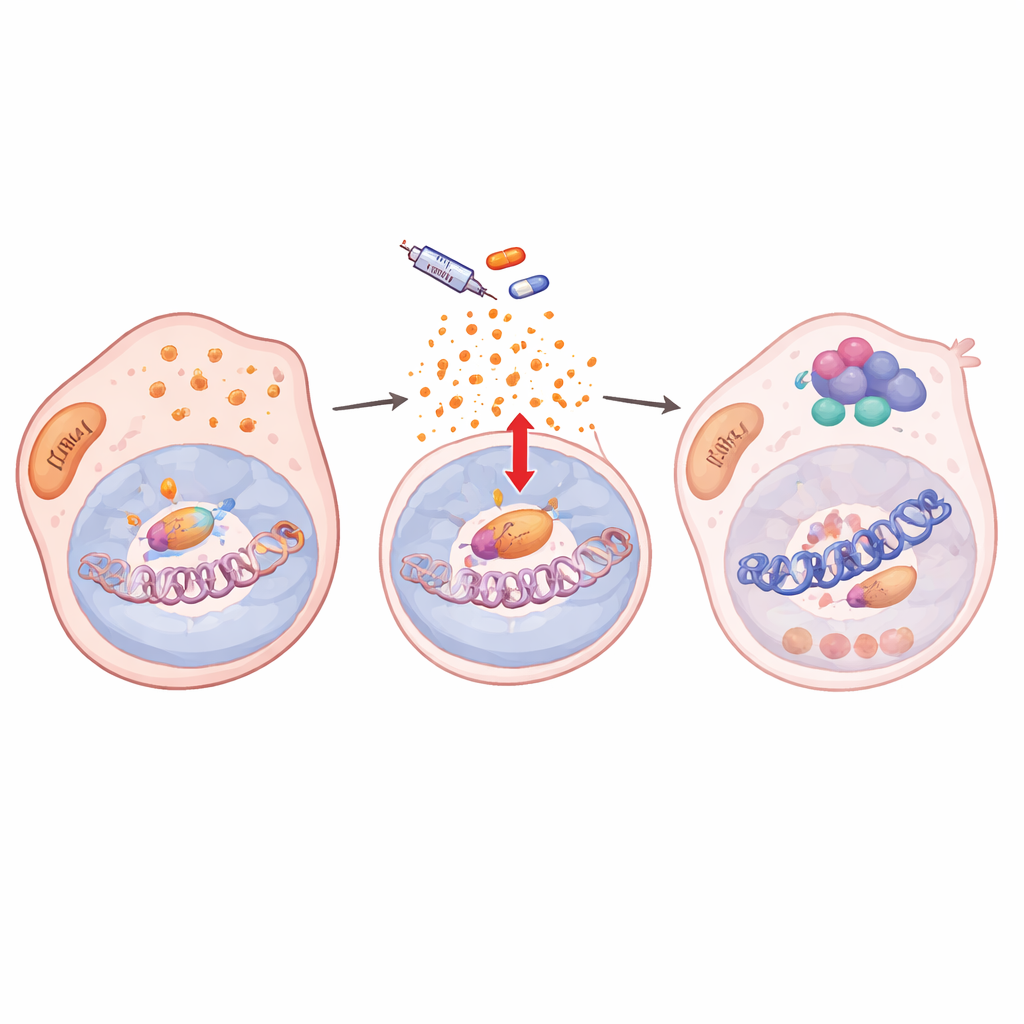
פלסטיות מקודדת בכרומטין, משותפת בין סוגי סרטן
הצוות שאל מדוע חלק מהגידולים נוטים יותר להתנהגות שינוי‑צורה זו מאחרים. במספר קווי תאי מלנומה הם מצאו שמידת השינוי המועלת על‑ידי תרופה התכתבה עם מידת הפתיחות והפעילות של הכרומטין בגני מטרה של RelA לפני הטיפול. קווים עם כרומטין "מקל" יותר הראו מעבר גדול יותר ותועלת חזקה יותר משילוב מעכבי BRAF עם תרופות המ targeting את RelA או שותפיו בכרומטין. בסופו של דבר, הם הראו שמסלול דומה של ROS–NF‑κB–כרומטין מניע כניסה למצבי תאי עמידים גם בסרטן ריאות וסרטן מעי כשהם מטופלים כנגד אונקוגנים מניעים בייחודם. בכל המקרים, חסימה של הפעלת NF‑κB/RelA או הפחתת ROS הגבילה את הופעתם והתייקרותם של תאי העמידות.
מה משמעות הדבר לטיפולים בסרטן בעתיד
המחקר הזה מציג מחדש את עמידות התרופות בהרבה סוגי סרטן כתוכנית תגובת מתח הפיכה ולא רק כבעיה גנטית. תאי הסרטן חשים מתח חמצוני שנגרם על‑ידי הטיפול, מפעילים NF‑κB/RelA ומשתמשים במעבדי כרומטין נלווים כדי לכבות זמנית גנים ששומרים על התמחותם ורגישותם לתרופות. מאחר שהתהליך תלוי באריזת ה‑DNA ולא במוטציות קבועות, הוא ניתן לתקיפה. הממצאים תומכים באסטרטגיות טיפול שמשלבות תרופות ממוקדות עם סוכנים החוסמים איתות NF‑κB/RelA או את שותפיו המעבדי‑כרומטין, במיוחד בגידולים שבהם הכרומטין מוכן לפלסטיות כזו. על‑ידי מניעת כניסת התאים למצב ה"מתמיד" מלכתחילה, קומבינציות כאלה עשויות להעמיק ולהאריך הפוגות בטיפול.
ציטוט: Su, Y., Liu, C., Lu, X. et al. Sequential transcriptional waves and NF-κB-driven chromatin remodeling direct drug-induced dedifferentiation in cancer. Nat Commun 17, 3228 (2026). https://doi.org/10.1038/s41467-026-71349-4
מילות מפתח: תאי עמידות עיקבית לתרופות, אותות NF-kB RelA, שכתוב כרומטין, פלסטיות של תאי סרטן, עמידות לטיפול ממוקד