Clear Sky Science · pl
Zastosowanie adaptacyjnego quasi-liniowego modelu lepkosprężystego do przewidywania obciążeń-odciążenia, relaksacji naprężenia i obciążeń sinusoidalnych w wątrobie świni
Dlaczego miękkość wątroby ma znaczenie
Kiedy gwałtownie hamujesz w wypadku samochodowym albo chirurg naciąga narząd podczas operacji, wątroba nie zachowuje się jak zwykła gumka. Powoli się rozciąga, relaksuje i rozprasza energię w sposób trudny do przewidzenia. W tym badaniu sprawdzono, jak dobrze popularny model matematyczny potrafi odzwierciedlić to złożone zachowanie w wątrobie świni i zadano pozornie proste pytanie: czy parametry modelu są rzeczywistymi właściwościami materiału wątroby, czy też zmieniają się wraz z szybkością i sposobem obciążania tkanki?
Jak naukowcy obecnie modelują miękkie narządy
Miękkie narządy, takie jak wątroba, są lepkosprężyste: przeciwdziałają odkształceniu jak ciało sprężyste, ale jednocześnie płyną i relaksują się jak gęsta ciecz. Przez dekady badacze używali rodzin modeli zwanych quasi-liniowymi modelami lepkosprężystymi (QLV) do opisu tego zachowania. Ulepszona wersja, adaptacyjny quasi-liniowy model lepkosprężysty (AQLV), przedstawia tkankę jako kombinacje sprężyn i tłumików, których odpowiedź może zmieniać się wraz z odkształceniem. Model ten jest atrakcyjny, ponieważ ma analityczne wzory dla typowych rodzajów obciążeń i można go skalibrować na podstawie stosunkowo prostych testów. Jednak standardowy sposób kalibracji modelu AQLV wykorzystuje wolne rozciąganie i utrzymanie odkształcenia, pozostawiając otwarte pytanie, czy te same parametry są wiarygodne przy dużo szybszym obciążaniu wątroby, jak ma to miejsce przy uderzeniach czy szybkich manewrach chirurgicznych.
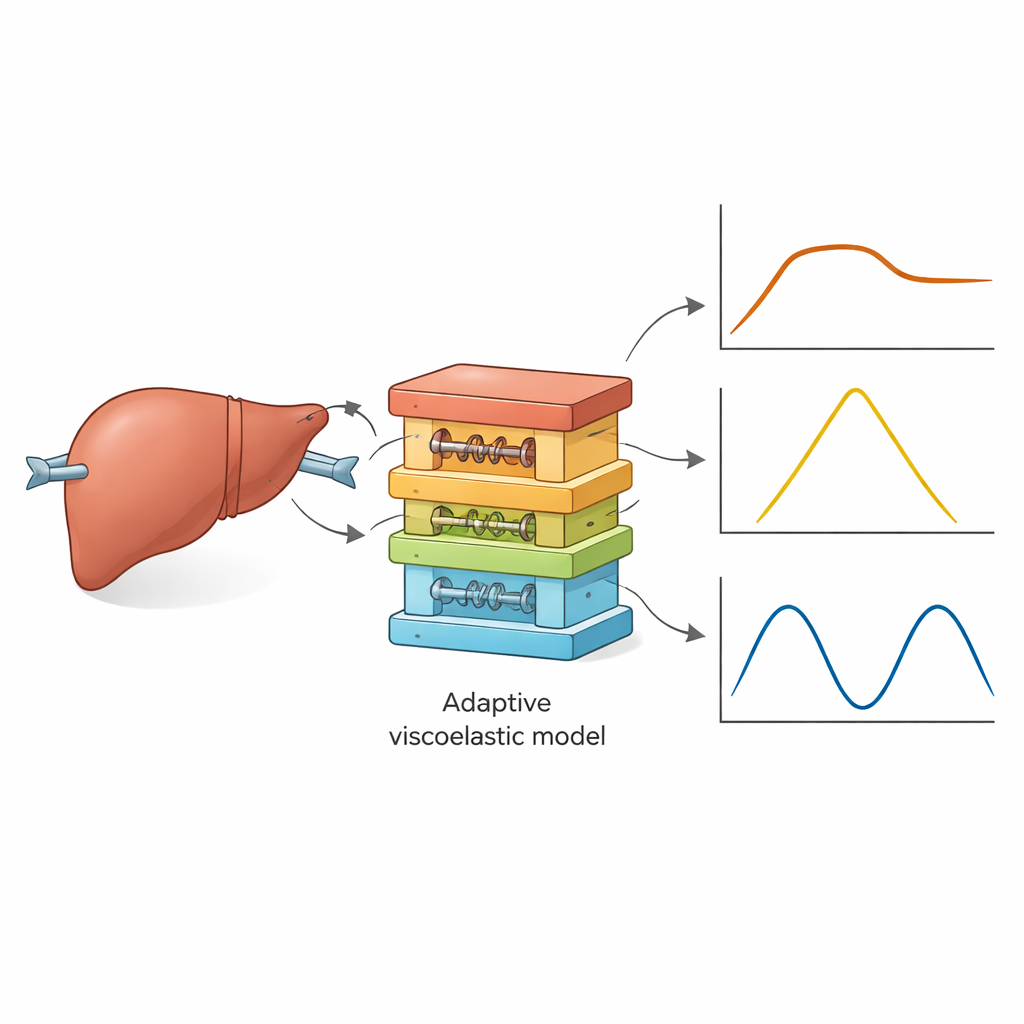
Wystawienie modelu wątroby na próbę
Autorzy użyli parametrów AQLV uzyskanych z wcześniejszych, wolnych testów na wątrobie świń i poprosili model o przewidzenie trzech bardzo różnych eksperymentów przeprowadzonych w odrębnym badaniu: szybkiego rozciągnięcia z następującym utrzymaniem (relaksacja naprężenia), trójkątnego cyklu obciąż-odciąż oraz obciążania sinusoidalnego w kilku częstotliwościach. W każdym przypadku zmierzone odkształcenie z eksperymentów zostało podane do modelu, aby wygenerować przewidywane naprężenie, które następnie porównano z rzeczywistymi pomiarami. Początkowo model radził sobie bardzo słabo: poziomy błędów były duże, niektóre przewidywania wykazywały niemożliwy ujemny napięcie podczas odciążania, a kluczowe miary energii różniły się znacząco od eksperymentu. Oznaczało to, że oryginalny zestaw parametrów, uzyskany przy jednej wolnej szybkości odkształcenia, nie mógł być po prostu ponownie użyty przy innych historiach obciążenia.
Dostrajanie modelu dla każdego rodzaju obciążenia
Aby zbadać to dalej, badacze ponownie skalibrowali parametry AQLV oddzielnie dla każdego przypadku obciążenia, używając optymalizacji najmniejszych kwadratów przy zachowaniu niezmienionej struktury modelu. Po ponownym dostrojeniu model bardzo dobrze odwzorował szybkie krzywe relaksacji naprężenia, z błędami zmniejszającymi się o rzędy wielkości; realistyczne były też przewidywania dla samego szybkiego narastania. Dla cykli obciąż-odciąż ponowna kalibracja usunęła artefakt ujemnego naprężenia i zbliżyła energie podczas obciążania i odciążania do wartości eksperymentalnych. Przy obciążeniu sinusoidalnym dostosowane parametry pozwoliły modelowi dopasować się do tego, jak sztywna wydaje się wątroba (moduł pamięci) i ile energii rozprasza (moduł strat i tangens strat) w funkcji częstotliwości, z niewielkimi rozbieżnościami tylko przy najwyższej badanej częstotliwości. Kluczowe było to, że wzorce zmian poszczególnych sztywności sprężyn i czasów relaksacji jasno pokazywały, iż wewnętrzne parametry systematycznie przesuwają się wraz z szybkością odkształcenia i częstotliwością.
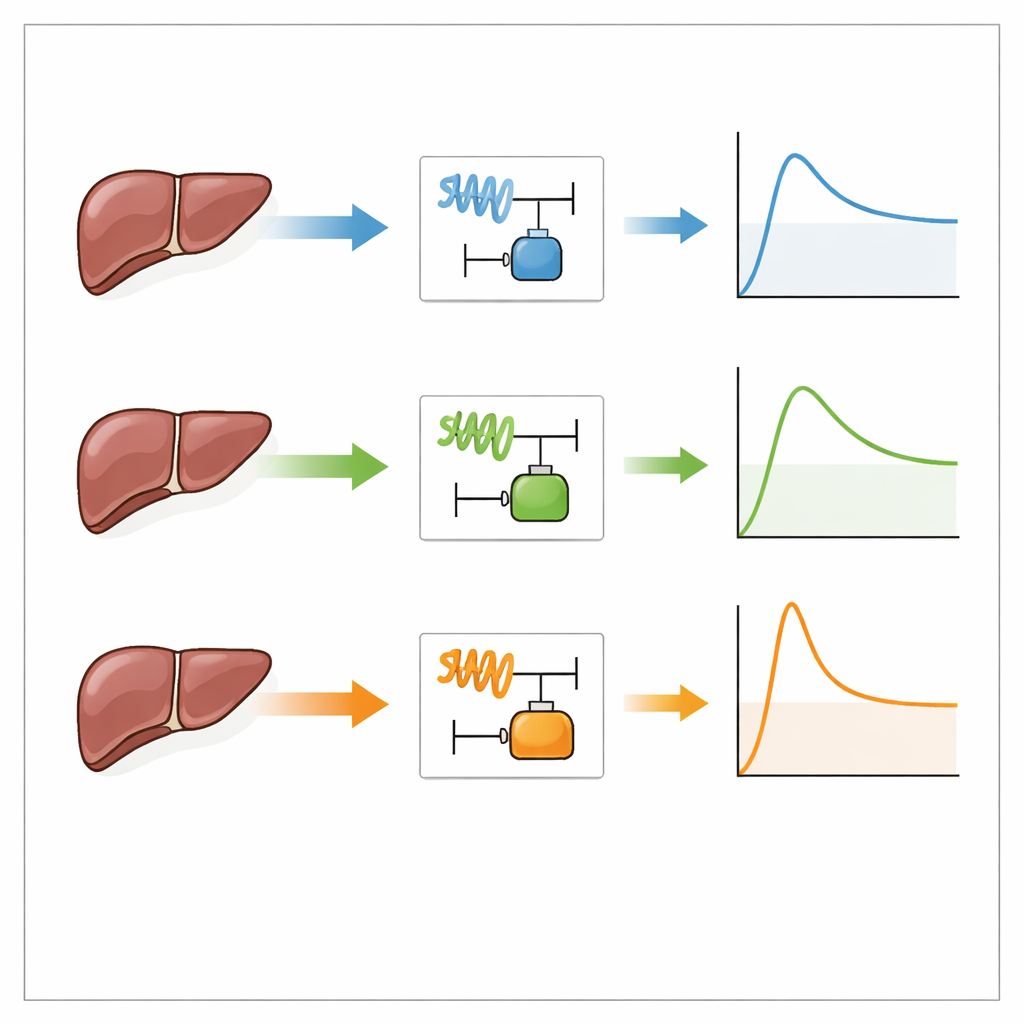
Czy jedna kalibracja wystarczy na wiele sytuacji?
Zespół zbadał następnie praktyczne uproszczenie: czy można skalibrować model raz w szybkim teście narastania-utrzymania i ponownie użyć tych parametrów do przewidywania innych, ale powiązanych obciążeń? Użycie parametrów z szybkiego testu narastania-utrzymania do przewidywania testów sinusoidalnych o podobnych średnich szybkościach odkształcenia działało stosunkowo dobrze dla części sprężystej odpowiedzi: moduł pamięci był bliski wartościom eksperymentalnym we wszystkich częstotliwościach. Jednak miary związane ze stratami energii, zwłaszcza tangens strat, nadal różniły się istotnie. Zastosowanie tego samego zestawu parametrów do cykli obciąż-odciąż powodowało większe błędy naprężeń i niedopasowanie energii obciążania i odciążania, mimo że ogólny kształt krzywych był uchwycony. Wyniki te sugerują, że samo dopasowanie szybkości odkształcenia nie wystarcza; istotny jest też dokładny przebieg czasowy obciążenia.
Co to oznacza dla modelowania prawdziwej tkanki
Z szerszej perspektywy badanie pokazuje, że parametry w modelu AQLV nie są stałymi, uniwersalnymi odciskami palca wątroby. Zamiast tego w dużym stopniu zależą od tego, jak tkanka jest testowana — jak szybko jest rozciągana, jak długo jest utrzymywana i czy obciążenie jest jednorazowym impulsem, cyklem czy ciągłą oscylacją. Model może bardzo dobrze opisać jednoosiowe zachowanie wątroby, jeśli jest dopasowany do konkretnego protokołu, ale nie dostarcza jednego, uniwersalnego zestawu stałych dla wątroby. Dla zastosowań takich jak symulacje wypadków samochodowych, planowanie zabiegów chirurgicznych czy projektowanie realistycznych fantomów treningowych oznacza to, że modelujący muszą albo dokonywać ponownej kalibracji dla każdego scenariusza obciążenia, albo przyjąć bardziej zaawansowane ułamkowe modele lepkosprężyste, które lepiej obejmują szeroki zakres skali czasowych jednym zestawem parametrów. Mówiąc prościej: wątroba nie ma jednej „sztywności”; jej pozorna sztywność zmienia się w zależności od tego, jak ją naciskasz, ciągniesz czy potrząsas, i nasze modele muszą to uwzględniać.
Cytowanie: Bittner-Frank, M., Aryeetey, O.J., Estermann, SJ. et al. Usage of the adaptive quasi-linear viscoelastic model to predict load-unload, stress-relaxation, and sine load of porcine liver. Sci Rep 16, 10675 (2026). https://doi.org/10.1038/s41598-026-45415-2
Słowa kluczowe: lepko-sprężysta wątroba, zależność od szybkości odkształcenia, modelowanie biomechaniczne, mechanika tkanek miękkich, adaptacyjna quasi-liniowa lepkosprężystość