Clear Sky Science · pl
Predykcja lokalizacji subkomórkowej circRNA przez łączenie sekwencji circRNA i informacji sieciowych
Dlaczego małe pętle RNA i ich adresy mają znaczenie
W każdej ludzkiej komórce ogromna liczba cząsteczek RNA krząta się, pomagając kontrolować, które geny są włączane, a które wyłączane. Wśród nich znajdują się RNA koliste, zwane circRNA — nietypowe, pętliste fragmenty RNA, które są zaskakująco stabilne i ściśle powiązane z wieloma chorobami, w tym z nowotworami. Aby zrozumieć rolę tych cząsteczek, naukowcy muszą znać jedną podstawową informację: gdzie w komórce się znajdują. Mapowanie „adresów” circRNA za pomocą tradycyjnych eksperymentów laboratoryjnych jest jednak powolne, kosztowne i niekompletne. W tym badaniu przedstawiono nową metodę komputerową, nazwaną CircLoc, która przewiduje, gdzie circRNA znajdują się wewnątrz komórek, łącząc informacje z ich sekwencji z informacjami złożonych sieci biologicznych, w których uczestniczą.
Małe pętle o dużych rolach biologicznych
Kiedyś uważane za bezpieczne pozostałości przetwarzania genów, circRNA są dziś znane z wpływu na szereg kluczowych procesów, od różnicowania komórek po regulację genów. Ich kolisty kształt sprawia, że są bardziej stabilne niż wiele innych RNA, co z kolei czyni je obiecującymi markerami diagnostycznymi. CircRNA mogą wiązać białka i wychwytywać mikroRNA — drobne regulatory, które zwykle tłumią aktywność genów — przez co przekształcają zachowanie komórki. Ponieważ wiele cząsteczek działa tylko w konkretnych częściach komórki, takich jak jądro, cytoplazma czy błony, znajomość lokalizacji subkomórkowej circRNA dostarcza ważnych wskazówek co do ich funkcji i potencjalnej roli w zdrowiu i chorobie.
Przekształcanie rozproszonych danych w „pole treningowe”
Autorzy rozpoczęli od zgromadzenia starannie skuratowanej kolekcji ludzkich circRNA z ustalonymi lokalizacjami z kilku publicznych baz danych. Po usunięciu rzadkich kategorii i skrajnie niezrównoważonych grup skupili się na siedmiu głównych rejonach komórkowych, w tym jądrze, nukleolusie, nukleoplazmie, cytoplazmie, cytozolu, chromatynie i błonach. W sumie zebrano 1 486 circRNA z wiarygodną sekwencją i co najmniej jedną znaną lokalizacją; wiele należało jednocześnie do kilku regionów, co czyniło zadanie typowym problemem predykcji wieloetykietowej. Dodatkowe zestawy danych z wcześniejszych wydań baz danych oraz duża kolekcja związana z nowotworami zostały odłożone jako niezależne testy, co pozwoliło autorom sprawdzić, jak dobrze ich model uogólnia się na nowo zgłoszone circRNA.
Łączenie wzorców sekwencji z mapami interakcji komórkowych
Główny pomysł CircLoc polega na tym, że „adres” circRNA kształtuje się nie tylko na podstawie jego własnej sekwencji, ale także na podstawie towarzystwa, w jakim się znajduje. Po stronie sekwencji model analizuje krótkie fragmenty sekwencji (k-mery i ich komplementy odwrotne) oraz bogatsze wzorce wyuczone przez duży model językowy skoncentrowany na RNA, nazwany RNAErnie, który został pierwotnie wytrenowany na masywnych zbiorach danych RNA, aby uchwycić subtelne regularności. Po stronie sieci autorzy zbudowali kilka map pokazujących, jak circRNA łączą się między sobą i z powiązanymi bytami biologicznymi: nakładające się sekwencje, związane choroby, odpowiedzi na leki, oddziałujące mikroRNA i białka wiążące. Narzędzie do osadzania sieci node2vec przekształca strukturę każdej mapy w cechy numeryczne, a autokoder grafowy z mechanizmem uwagi (GATE) następnie je udoskonala, podkreślając połączenia między circRNA o podobnym zachowaniu, efektywnie odszumiając i wzbogacając sygnały pochodzące z sieci.
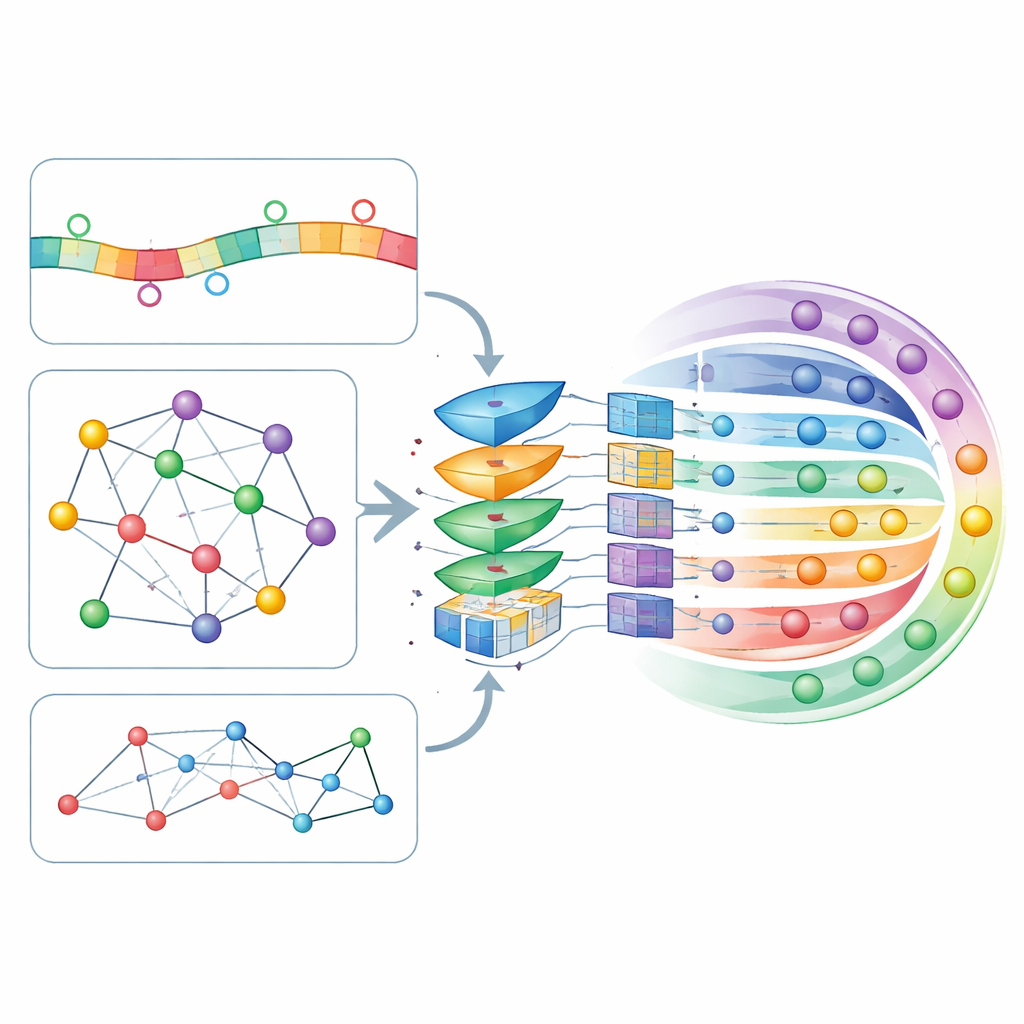
Pozwalając modelowi zdecydować, co jest najważniejsze
Wszystkie te cechy oparte na sekwencji i sieciach są zszywane w pojedynczy profil dla każdego circRNA i przekazywane przez warstwę samo-uwagi, mechanizm pozwalający modelowi nauczyć się, które kombinacje cech powinny najbardziej wpływać na jego decyzje. Udoskonalone profile trafiają następnie do głębokiej, w pełni połączonej sieci neuronowej, która zwraca prawdopodobieństwo dla każdego z siedmiu możliwych miejsc. Autorzy dostrajali wiele ustawień modelu za pomocą walidacji krzyżowej dziesięciokrotnej, rygorystycznej procedury, która wielokrotnie dzieli dane na części treningowe i testowe. CircLoc osiągnął średni wynik około 0,79 na standardowej miarze jakości (AUC), wyraźnie przewyższając wcześniejsze podejścia zaprojektowane dla mikroRNA oraz klasyczne metody wieloetykietowe trenowane na tych samych cechach. Eksperymenty polegające na usuwaniu konkretnych cech lub modułów wykazały, że informacje sieciowe i etap udoskonalenia przez GATE były szczególnie istotne, podczas gdy cechy sekwencyjne nadal wnosiły użyteczny, choć mniejszy, wkład.
Jak model radzi sobie z nowymi circRNA?
Aby sprawdzić użyteczność w rzeczywistych zastosowaniach, zespół trenował CircLoc na jednej wersji bazy lokalizacji, a testował go na circRNA, które pojawiły się tylko w późniejszym wydaniu, oraz na odrębnym zasobie skoncentrowanym na nowotworach. Wyniki spadły w porównaniu z oryginalnym zbiorem treningowym, co było spodziewane wobec naprawdę nowych danych z różnych źródeł, ale pozostały przyzwoite: średnie wyniki zmniejszyły się umiarkowanie, dalej wskazując na istotną moc predykcyjną. Testy te, wraz z porównaniami z innymi metodami, sugerują, że CircLoc może dostarczać rozsądne, wstępne przypuszczenia dotyczące lokalizacji nowo odkrytych circRNA, nawet gdy brak jest części informacji pomocniczych — takich jak szczegółowe powiązania z chorobami czy lekami.
Co to oznacza dla przyszłych badań nad RNA
Praca ta pokazuje, że łączenie bezpośrednich informacji o sekwencji z bogatymi sieciami interakcji może pomóc modelom obliczeniowym przewidzieć, gdzie circRNA prawdopodobnie się znajdują w komórce. Dla biologów eksperymentalnych CircLoc oferuje sposób priorytetyzacji, które circRNA warto badać w określonych przedziałach komórkowych, co potencjalnie pozwala zaoszczędzić czas i zasoby. Choć metoda nie może jeszcze zastąpić pomiarów laboratoryjnych, a jej twórcy zauważają ograniczenia, takie jak niekompletne dane i umiarkowana wydajność w niektórych zestawach testowych, stanowi ważny krok w kierunku wielkoskalowych, in silico „książek adresowych” dla cząsteczek RNA. W miarę jak bazy danych będą rosły, a techniki modelowania się poprawiały, takie narzędzia mogą stać się rutynowymi towarzyszami eksperymentów, kierując poszukiwania circRNA mających największe znaczenie w chorobach i terapii.
Cytowanie: Chen, L., Hu, J. & Zhou, B. Predicting circRNA subcellular localization by fusing circRNA sequence and network information. Sci Rep 16, 12775 (2026). https://doi.org/10.1038/s41598-026-43808-x
Słowa kluczowe: RNA koliste, lokalizacja subkomórkowa, biologia obliczeniowa, uczenie maszynowe, sieci RNA