Clear Sky Science · ja
説明可能な人工知能によるがん種・データ様式横断の教師なしリスク因子同定
隠れたリスクパターンを見つける重要性
がん専門医は、同じ診断であっても将来の経過が大きく異なる患者がいることをよく知っています。ある人は治療に良く反応して長く生存する一方で、病態が似て見えても別の人はそうでないことがあります。本稿は、日常的に得られる医療データや画像をコンピュータに探索させて、生存確率が似た患者群という隠れたクラスタを発見する新しい方法を示します。これを明確なリスク群に変換することで、複雑な追加検査を必要とせずに、より個別化された治療判断を支援することを目指しています。
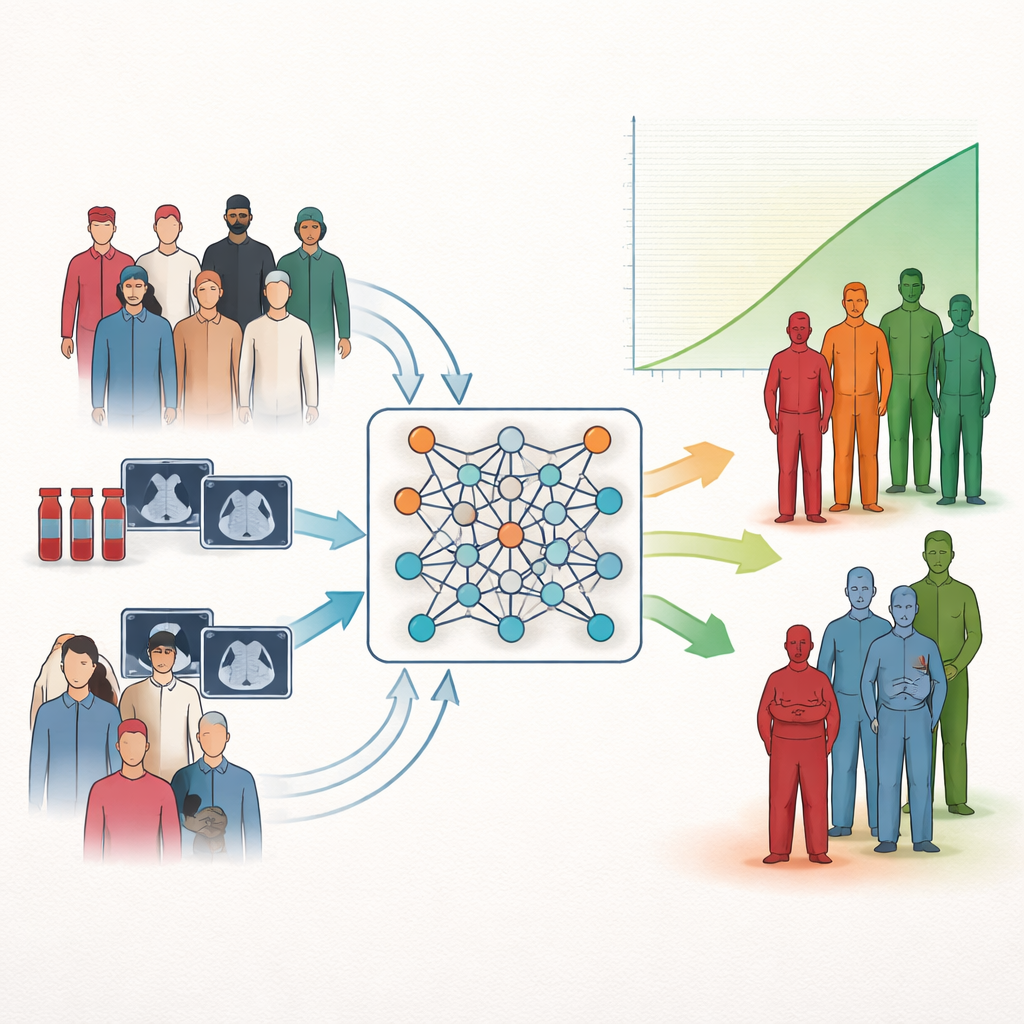
アウトカムで患者を分類する新手法
研究者らは医学でよくある課題、すなわちリスク層別化に注目しました。リスク層別化とは、予後が良い群と悪い群に患者を振り分けることです。従来の統計手法は個々の測定値が生存とどう関連するかを推定できますが、臨床で使える単純な低・中・高リスクのカテゴリにきれいに対応するとは限りません。多くの現代的なAI手法は性能を高めますが、それでも明確で解釈しやすい群分けを提供するのに苦労します。著者らは、生存時間をただ予測するのではなく、ニューラルネットワークに生存においてできるだけ異なる患者クラスタを直接形成させることで、このギャップに対処しています。
生存データを学習に取り込む
手法の中核は、標準的な生存統計であるログランク検定を、ニューラルネットワークが最適化できる滑らかな目的関数に作り替えたことです。訓練中に各患者を確定的に一つの群に割り当てる代わりに、モデルは群所属を確率として扱い、クラスタ間の生存差が鋭くなるようにこれらを調整します。すべての患者が同じカテゴリに落ち着いてしまう自明な解を避けるためのバランス項も導入されています。この訓練レシピは損失関数として作用するだけなので、内部設計を変えずにさまざまな種類のニューラルネットワークや入力データに組み込めます。
血液検査から学んだこと
臨床的価値を示すため、研究チームはまず多発性骨髄腫のほぼ1000人を対象に、診断時前後に測定された標準的な血液検査10項目だけを用いて手法を適用しました。ネットワークは自動的に生存曲線が明確に分かれた3つのリスク群を形成しました。最も予後不良な群の中央値生存期間は約4年で、最良群の約70%は9年後も生存していました。説明可能性ツールでどの検査値が群分けに寄与したかを調べると、β2-ミクログロブリンやクレアチニンといった既知の病勢指標や腎機能の負荷は高リスクへ、アルブミンやヘモグロビンの良好な値は低リスクへと患者を押しやっていることが分かりました。同じパターンは独立した臨床試験データセットでも再現され、発見された群が堅牢であることを示唆しています。
肺CTから見つかったこと
2つ目の検証例では、非小細胞肺がん患者数百名の胸部CTを用いました。ここでは腫瘍の手描き領域や事前計算された特徴は使わず、画像だけを入力としました。新しい損失関数で訓練した畳み込みニューラルネットワークは、労力のかかるラジオミクス法と同様に、生存時間が明確に異なる2群に患者を分けました。可視化された説明マップは、モデルが腫瘍を含む肺領域や、そこから伸びる浸潤性の広がり、さらには心臓近傍の血管などの構造に注目していることを示しました。高リスク患者ではこれらの構造がモデルの判断に強く寄与しており、浸潤性増殖や心血管疾患が予後不良と結びつくという臨床知見と一致します。
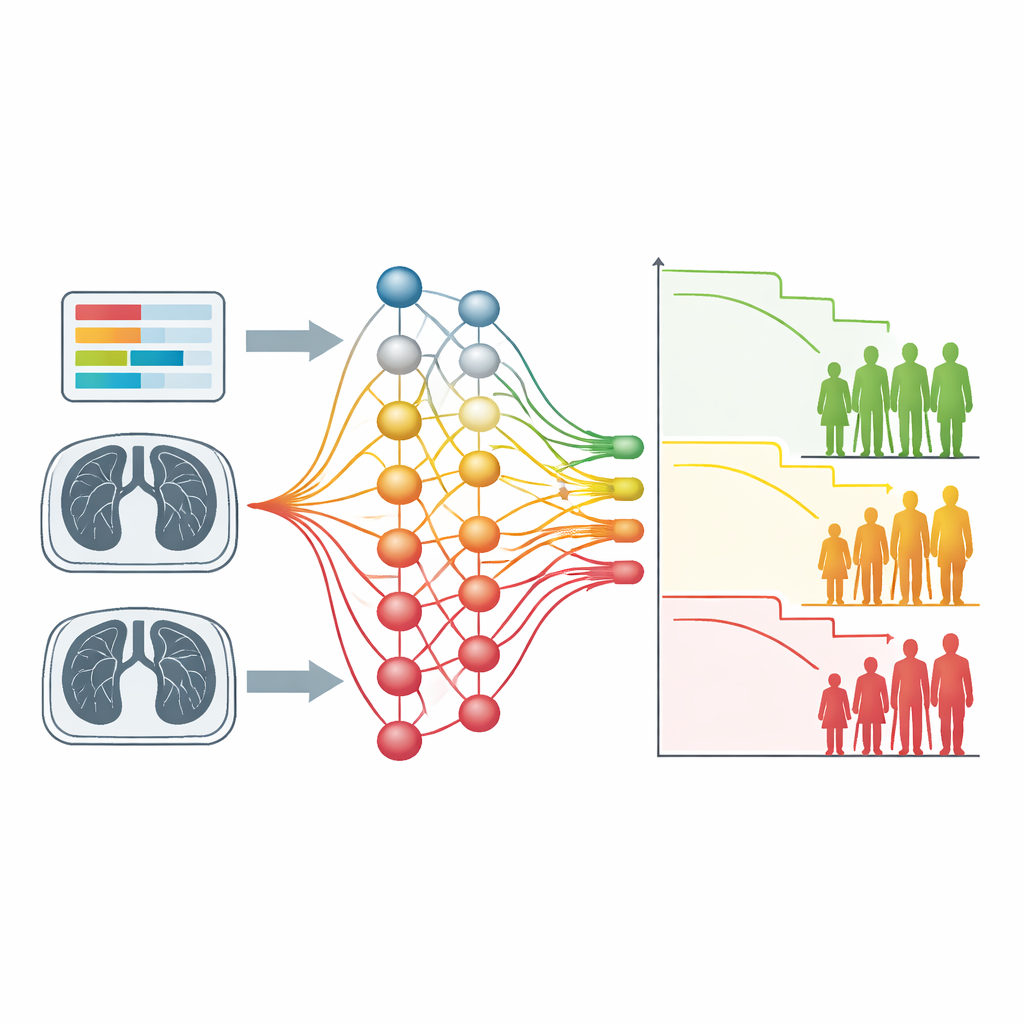
将来のがん医療への影響
総じて、この研究はサバイバル指向クラスタリングが、単純な血液検査から複雑な画像に至るまで既知のリスク因子を再発見でき、手作業のラベル付けや手作りのルールを必要としないことを示しています。同じ訓練レシピが複数のがん種やデータ型で機能するため、遺伝子発現プロファイルや時間変動する治療データのような領域を含め、新しい予後パターンの探索に柔軟な出発点を提供します。患者にとっての長期的な期待は、自身のデータから直接導かれるより明瞭なリスク区分が得られ、臨床医が治療の強度や方針をリスクレベルに合わせやすくなることです。一方で研究者は、転帰と結びつく新たなシグナルを発見するための道具を手に入れます。
引用: Ferle, M., Ader, J., Wiemers, T. et al. Unsupervised risk factor identification across cancer types and data modalities via explainable artificial intelligence. npj Digit. Med. 9, 363 (2026). https://doi.org/10.1038/s41746-026-02663-w
キーワード: がんリスク層別化, 生存解析, 医療画像AI, 多発性骨髄腫, 肺がん