Clear Sky Science · ar
تحديد عوامل الخطر غير الخاضعة للإشراف عبر أنواع السرطان وأنماط البيانات عبر ذكاء اصطناعي قابل للتفسير
لماذا يهم العثور على أنماط مخاطرة خفية
يعلم أطباء السرطان أن الأشخاص الذين لديهم نفس التشخيص قد يواجهون مسارات مستقبلية مختلفة تمامًا. بعضهم يستجيب جيدًا للعلاج ويعيش لسنوات عديدة، بينما قد لا يستفيد آخرون، حتى عندما تبدو أمراضهم متشابهة من الناحية الظاهرية. تعرض هذه المقالة طريقة جديدة لتمكين الحواسيب من البحث عبر البيانات الطبية الروتينية والصور لإبراز مجموعات مخفية من المرضى الذين يشتركون في احتمالات بقاء متقاربة. من خلال تحويل ذلك إلى فئات مخاطرة واضحة، تهدف الدراسة إلى دعم قرارات علاجية أكثر تخصيصًا دون الحاجة إلى اختبارات إضافية معقدة.
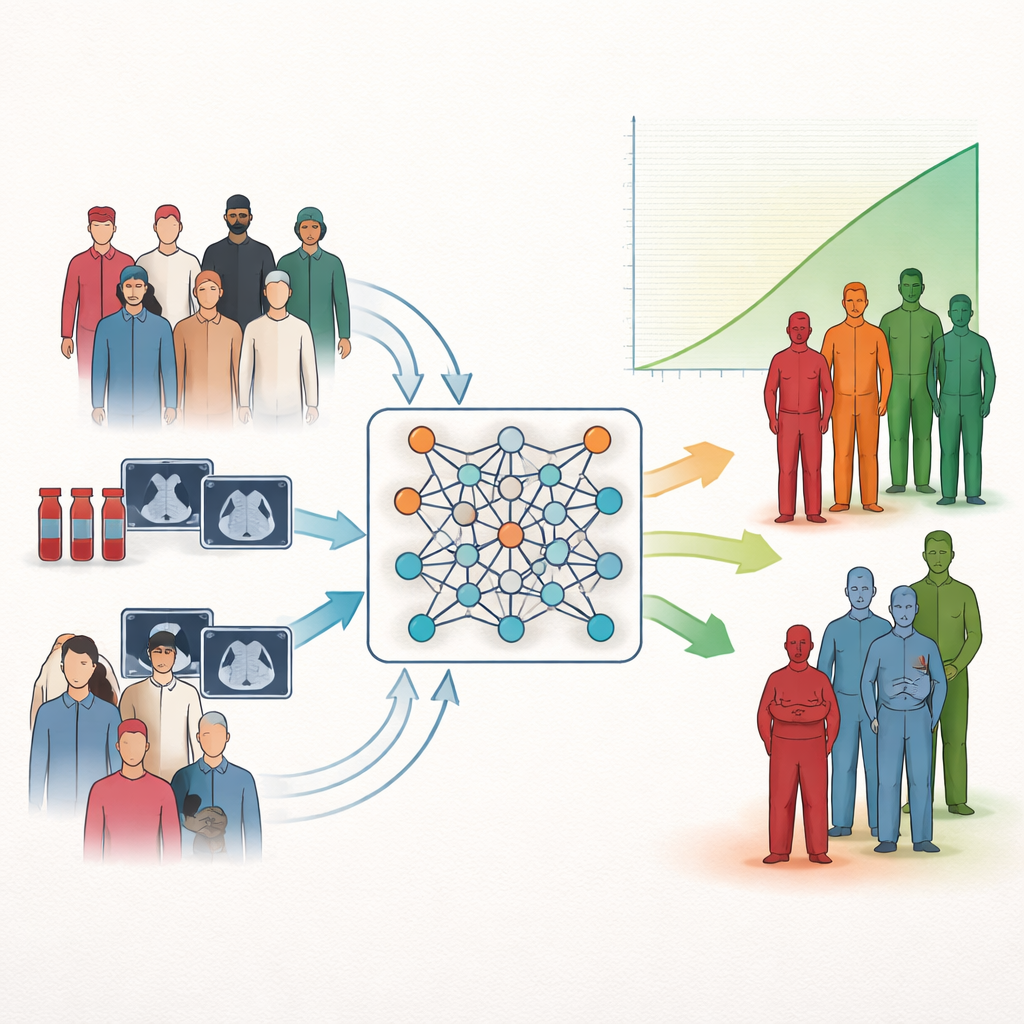
طريقة جديدة لتجميع المرضى حسب النتيجة
يركز الباحثون على مهمة شائعة في الطب: تصنيف المخاطر، أي فرز المرضى إلى مجموعات ذات توقعات أفضل أو أسوأ. يمكن للأدوات الإحصائية التقليدية تقدير كيف ترتبط القياسات الفردية بالبقاء، لكنها غالبًا لا تتوافق بسهولة مع فئات بسيطة مثل منخفضة أو متوسطة أو عالية المخاطر التي يمكن للأطباء استخدامها على نحو عملي. تضيف العديد من أنظمة الذكاء الاصطناعي الحديثة قدرة أكبر لكنها ما تزال تكافح لتقديم تجميعات واضحة وسهلة التفسير. يتصدى المؤلفون لهذه الفجوة بتعليم الشبكات العصبية مباشرة لتشكيل مجموعات مرضى تختلف في معدلات البقاء قدر الإمكان، بدلًا من محاولة التنبؤ بوقت البقاء فحسب أو تجميع المرضى استنادًا إلى التشابه السطحي فقط.
جعل بيانات البقاء توجه التعلم
في جوهر الطريقة إعادة صياغة لإحصائية بقاء كلاسيكية، تُعرف باختبار اللوغرنك، إلى هدف سلس يمكن للشبكة العصبية تحسينه. بدلاً من وضع كل مريض بحزم في مجموعة واحدة أثناء التدريب، يتعامل النموذج مع عضوية المجموعات كاحتمالات ويعدّلها لزيادة فروق البقاء بين التجمعات. يمنع حد موازن الحل التافه الذي يقضي على توزيع المرضى في فئة واحدة تقريبًا. وبما أن وصفة التدريب هذه تعمل فقط كدالة خسارة، فيمكن توصيلها بالعديد من أنواع الشبكات العصبية وأنماط البيانات دون تغيير تصميمها الداخلي.
ما الذي تعلمته الطريقة من اختبارات الدم
لإظهار القيمة السريرية، طبّق الفريق نهجه أولًا على ما يقرب من ألف شخص مصابين بالمايلوما المتعددة، وهو سرطان دموي، مستخدمين عشرة قياسات دموية معيارية مأخوذة حول وقت التشخيص. شكلت الشبكة تلقائيًا ثلاث مجموعات مخاطرة كانت منحنيات بقائها مفصولة بوضوح. كانت أسوأ مجموعة لها متوسط بقاء يقارب أربع سنوات، بينما بقي نحو سبعين بالمئة من أفضل مجموعة على قيد الحياة بعد تسع سنوات تقريبًا. عندما استخدم المؤلفون أدوات التفسير لرؤية أي قيم مخبرية دفعت هذه التجمعات، دفعت مؤشرات معروفة لحجم المرض وإجهاد الكلى، مثل بيتا-2-ميكروغلوبولين والكرياتينين، المرضى نحو مخاطر أعلى، في حين جذبتهم مستويات أفضل من الألبومين والهيموغلوبين نحو مخاطر أقل. حفظت نفس الأنماط على مجموعة بيانات تجريبية سريرية مستقلة، مما يدل على متانة التجمعات المكتشفة.
ما وجدته الطريقة في فحوصات الرئة
اختبار الحالة الثانية استخدم تصوير مقطعي للصدر لمئات الأشخاص المصابين بسرطان الرئة غير صغير الخلايا. هنا كان المدخل هو الصورة وحدها، دون أي حدود مرسومة يدويًا للأورام أو ميزات محسوبة مسبقًا. شبكة عصبية تلافيفية مدربة بدالة الفقد الجديدة قسمت المرضى إلى مجموعتين ذاتا فترات بقاء مختلفة بوضوح، شبيهة بنهج راديوميكس الأكثر استهلاكا للوقت. كشفت خرائط التفسير البصري أن النموذج تعلّم التركيز على مناطق الرئة التي تحتوي على أورام وتمديداتها المتفرعة والمتوغلة، بالإضافة إلى هياكل مجاورة مثل أوعية القلب. في المرضى ذوي المخاطر العالية، كانت هذه الهياكل تميل إلى المساهمة بقوة في قرارات النموذج، مما يعكس المعرفة السريرية أن النمو المتوغّل وأمراض القلب مرتبطان بنتائج أسوأ.
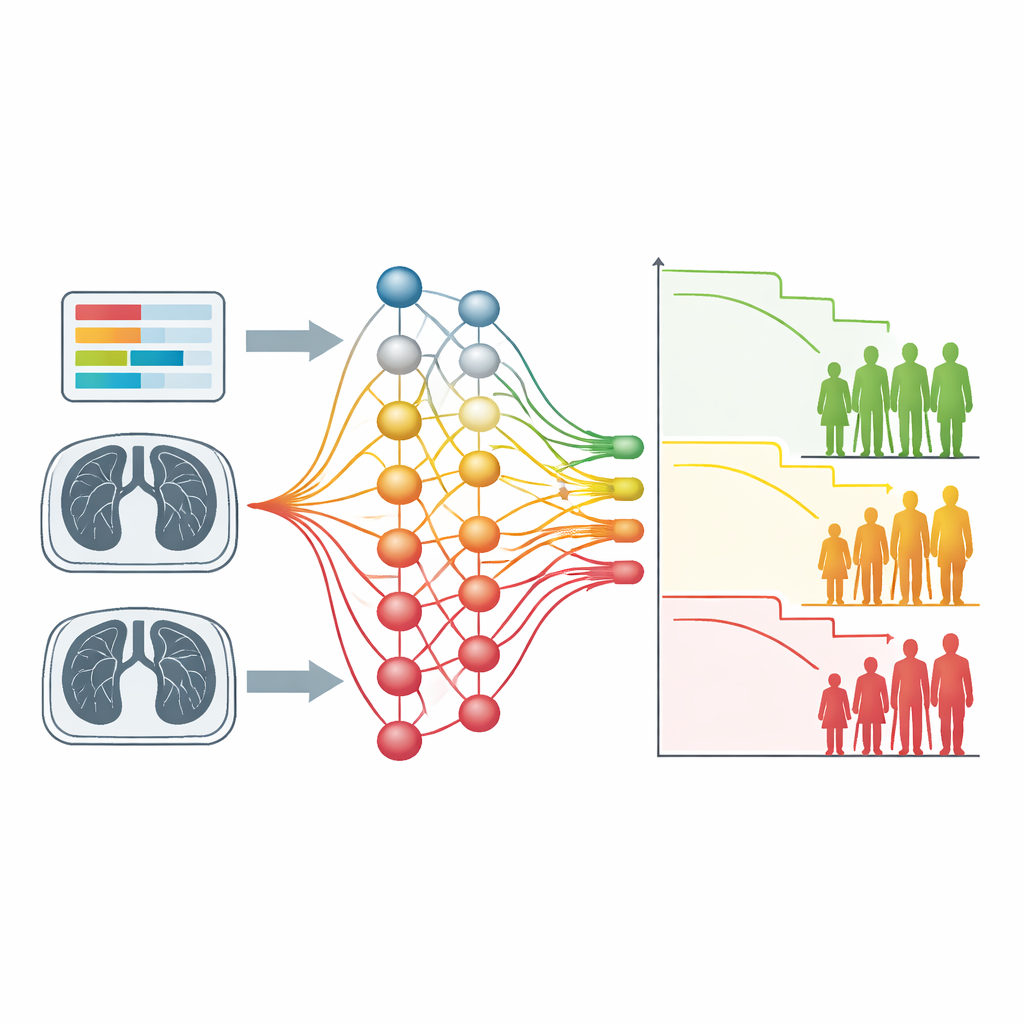
كيف يمكن أن يشكّل هذا رعاية السرطان المستقبلية
بشكل عام، تظهر الدراسة أن التجميع الموجه بالبقاء يمكنه إعادة اكتشاف عوامل خطر معروفة سواء من اختبارات دم بسيطة أو صور معقدة، وأنه يستطيع القيام بذلك دون وسم يدوي أو قواعد مصممة يدوياً. وبما أن وصفة التدريب نفسها تعمل عبر أنواع السرطان وأنماط البيانات، فإنها تقدم نقطة انطلاق مرنة لاستكشاف أنماط تنبؤية جديدة، بما في ذلك في مجالات مثل ملفات نشاط الجينات أو بيانات العلاج المتغيرة مع الزمن. بالنسبة للمرضى، الوعد طويل الأمد هو فئات مخاطرة أوضح تنشأ مباشرة من بياناتهم الخاصة وتساعد الأطباء على مطابقة شدة ونمط العلاج مع مستوى الخطر، بينما يحصل الباحثون على أداة لرصد إشارات جديدة مرتبطة بالنتيجة.
الاستشهاد: Ferle, M., Ader, J., Wiemers, T. et al. Unsupervised risk factor identification across cancer types and data modalities via explainable artificial intelligence. npj Digit. Med. 9, 363 (2026). https://doi.org/10.1038/s41746-026-02663-w
الكلمات المفتاحية: تصنيف مخاطر السرطان, تحليل البقاء, الذكاء الاصطناعي في التصوير الطبي, المايلوما المتعددة, سرطان الرئة