Clear Sky Science · de
mViSE: Eine visuelle Suchmaschine zur Analyse multipler IHC-Gehirngewebe-Bilder (räumliche Proteomik)
Mustern im Gehirn auf die Spur kommen
Moderne Mikroskope können inzwischen atemberaubend detaillierte Bilder ganzer Gehirnschnitte aufnehmen und dabei dutzende verschiedener Proteine gleichzeitig zeigen. Diese „multiplexen“ Bilder versprechen Hinweise darauf, wie Gehirnzellen organisiert sind, wie sie miteinander kommunizieren und wie Erkrankungen diese Muster stören. Die Bilder sind jedoch so riesig und komplex, dass selbst leistungsfähige Computer Schwierigkeiten haben, sie zu durchdringen. Dieses Paper stellt mViSE vor, eine visuelle Suchmaschine, mit der Forschende diese gewaltigen Gehirnbilder erkunden können, indem sie einfach auf Zellen und interessante Nachbarschaften klicken – statt eigenen Code zu schreiben.
Warum große Gehirnbilder schwer nutzbar sind
Jedes multiplexe Gehirnbild ist wie eine riesige Stadtkarte, auf der jedes Gebäude, jede Straße und jede Versorgungslinie gleichzeitig in vielen Farben beschriftet ist. Unterschiedliche Proteine markieren verschiedene Zelltypen, Zellzustände, Blutgefäße und Verschaltungsstrukturen. Traditionelle Analyse-Pipelines zerlegen diese Karte in eine lange Kette programmierter Schritte: Bild bereinigen, Zellen erkennen, segmentieren, Zelltypen zuordnen und Ergebnisse nach Regionen zusammenfassen. Diese Herangehensweise ist zwar mächtig, aber starr und schwer anzupassen, wenn neue Fragestellungen auftauchen – besonders beim Gehirn, dessen Mischung aus Neuronen, Gliazellen und Blutgefäßen enorme molekulare und räumliche Komplexität zeigt. Forschende brauchen zunehmend eine flexiblere, interaktive Möglichkeit, neue Fragen an diese Daten zu stellen, ohne zu Vollzeit-Programmierern werden zu müssen.
Eine Suchmaschine für Gehirnzellen
mViSE behandelt ein Gehirnbild eher wie eine Online-Fotobibliothek als wie ein statisches Datenset. Anstatt jeden Analyse-Schritt vorab zu definieren, klickt der Nutzer auf eine Zelle oder einen kleinen Gewebefleck, der interessant aussieht. Das System durchsucht dann das gesamte Gehirnbild nach Zellen oder Nachbarschaften, die über viele Proteinkanäle hinweg ähnlich aussehen und „sich ähnlich verhalten“. Die Treffer werden direkt in der Gesamtansicht des Gehirns hervorgehoben und können als Proteinexpressionsprofile zusammengefasst werden. So können Forschende schnell aufdecken, wo ähnliche Zellen oder Mikro‑Umgebungen auftreten, Gehirnregionen und kortikale Schichten abgrenzen und Muster in verschiedenen Bereichen vergleichen – alles gesteuert durch visuelle Abfragen statt durch Code. 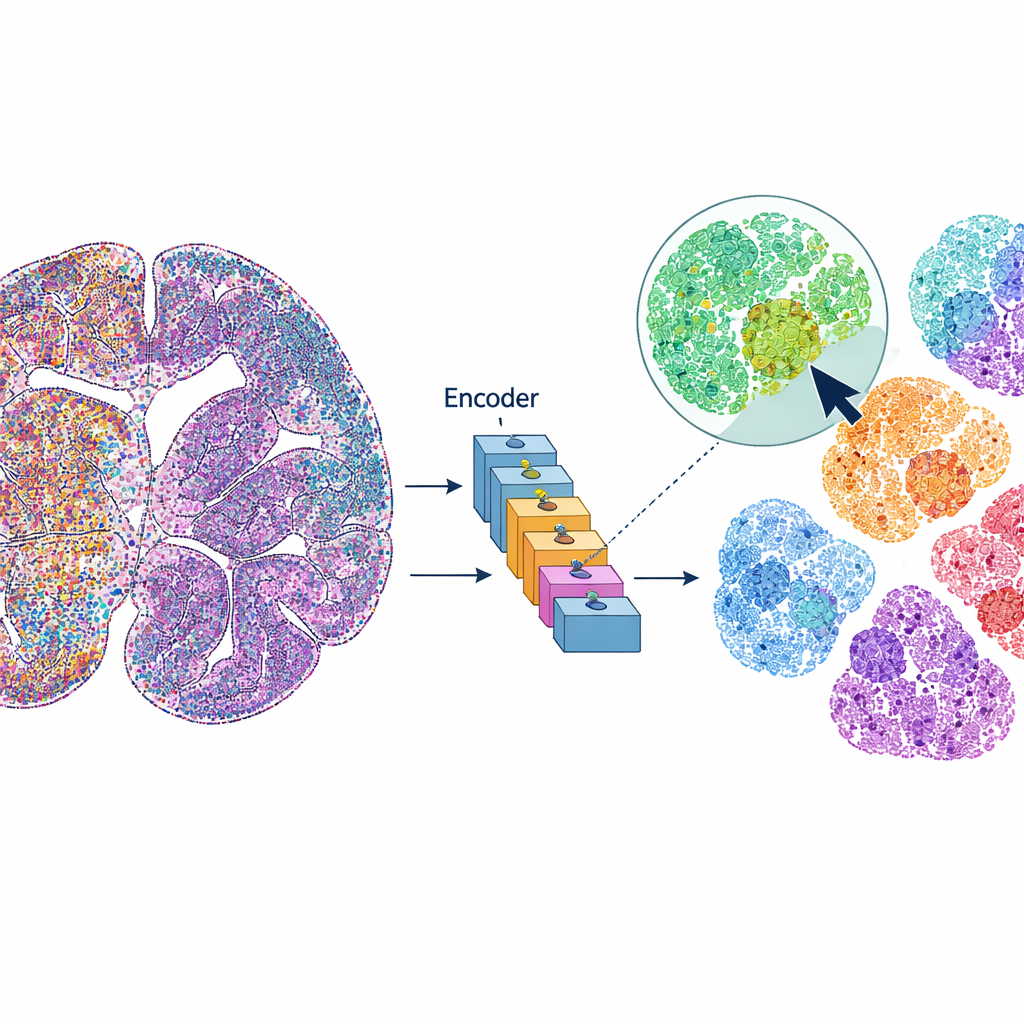
Dem Computer Gewebeverständnis beibringen
Damit das funktioniert, durchläuft mViSE zunächst eine Lernphase, die vollständig im Hintergrund abläuft. Die Autoren teilen die vielen Proteinkanäle in biologisch sinnvolle Panels auf, etwa Marker, die Zelltypen, Gliazellen, Nervenfasern oder Blutgefäße hervorheben. Für jedes Panel betrachtet ein leistungsfähiger Vision Transformer – ein modernes Deep‑Learning‑Modell – viele kleine Patches im Gehirn und lernt, jeden Patch als Punkt in einem hochdimensionalen „Merkmalsraum“ zu repräsentieren. Patches, die ähnlich aussehen und wirken, sollten in diesem Raum nahe beieinander liegen. Ein informationstheoretisches Community‑Detection‑Verfahren gruppiert dann benachbarte Punkte in Communities, die wiederkehrende Muster der Gewebearchitektur widerspiegeln. Wichtig ist, dass dieses Lernen selbstüberwacht erfolgt: Es benötigt keine menschliche Annotation, erzeugt aber dennoch farbkodierte Karten, die visuell bestätigen, dass bekannte Schichten und Regionen erfasst werden.
Reinzoomen auf Zellen und Nachbarschaften
Nachdem das System trainiert ist, kann mViSE auf verschiedene Abfragetypen reagieren. Bei sehr kleinen Patches mit einzelnen Zellen ruft es die ähnlichsten Zellen im ganzen Gehirn ab und zeigt, wo sie liegen. Die Autoren zeigen, dass das System zuverlässig die großen Gehirnzelltypen findet – etwa Neuronen, Astrozyten, Oligodendrozyten, Mikroglia und vaskuläre Zellen – sowie spezifischere neuronale Subtypen und sogar Zellpaare neben Blutgefäßen. Bei größeren Patches, die mehrere Zellen und lokale Verschaltungen umfassen, liefert mViSE die gesamte Community ähnlicher Nachbarschaften und zeichnet dabei oft bekannte Gehirnregionen oder Bahnen nach. Durch die Kombination von Informationen aus mehreren Marker‑Panels gleichzeitig kann es auch subtile Unterschiede zwischen kortikalen Schichten und kleinen Unterregionen herausarbeiten, die sonst schwer zu unterscheiden wären.
Bessere Leistung als generische KI‑Modelle
Die Forschenden verglichen mViSE mit mehreren hochmodernen „Foundation“‑Modellen, die ursprünglich auf großen Sammlungen von Natur‑ oder Pathologiebildern trainiert wurden. Da diese Modelle einfache Dreifarb‑Bilder erwarten, mussten die vielen Proteinkanäle auf Rot, Grün und Blau zusammengedrängt werden, was Informationsverlust verursachte. Selbst nach dieser Anpassung lieferten diese generischen Modelle unschärfere Grenzen zwischen Schichten und übersahen feinkörnige Unterregionen. Im Gegensatz dazu wurde mViSE, das dafür konzipiert ist, viele Kanäle direkt zu verarbeiten und jeden Kanal separat zu kodieren, bevor sie kombiniert werden, bei der Zuordnung bekannter Hirnatlas‑Regionen genauer. Es erzeugte schärfere Karten kortikaler Schichten und kohärentere Communities ähnlicher Patches, was darauf hindeutet, dass seine Repräsentationen die biologische Organisation besser abbilden. 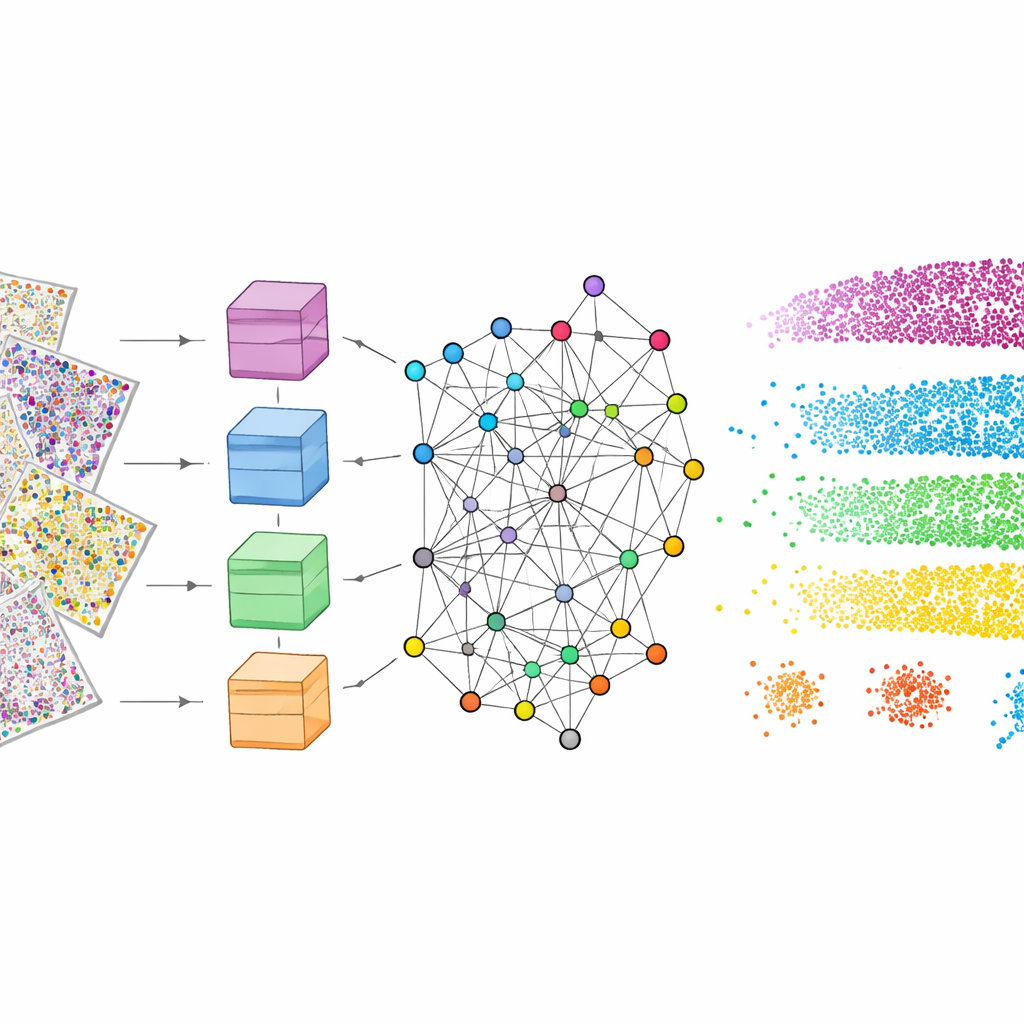
Eine neue Art, die lebendige Karte zu erkunden
Im Kern verwandelt mViSE riesige, vielfarbig kodierte Gehirnbilder in eine interaktive Karte, die Forschende visuell durchsuchen können. Anstatt jede Analyse mühselig zu skripten, können Wissenschaftler auf Zellen oder Mikro‑Umgebungen klicken, die ihnen ins Auge fallen, und sofort sehen, wo ähnliche Strukturen auftreten und wie ihre Proteinprofile verglichen sind. Die Methode benötigt während des Trainings keine manuelle Annotation und skaliert zu sehr großen Datensätzen, wodurch sie eine praktische Ergänzung im Werkzeugkasten der räumlichen Proteomik darstellt. Wenn die Bildgebungstechnologien noch mehr molekulare Kanäle hinzufügen und ähnliche Ansätze auf erkrankte Gehirne und andere Organe ausgeweitet werden, könnten Tools wie mViSE helfen, die rohe Bildkomplexität in intuitive, navigierbare Darstellungen der Gewebearchitektur zu verwandeln – und uns so dem Ziel näherbringen, das komplexe molekulare Atlas des Gehirns wie eine durchsuchbare Karte zu lesen.
Zitation: Huang, L., Mills, R., Mandula, S. et al. mViSE: A visual search engine for analyzing multiplex IHC brain tissue images (spatial proteomics). Sci Rep 16, 10245 (2026). https://doi.org/10.1038/s41598-026-40620-5
Schlüsselwörter: räumliche Proteomik, Gehirnbildgebung, visuelle Suchmaschine, multiplexe Mikroskopie, computationale Pathologie