Clear Sky Science · zh
突破“五元环规则”以合成桥联双环杂芳烃的生物等排体
为什么三维分子重要
许多现代药物由平面环状分子构成,像钥匙与锁一样契合蛋白靶点。化学家发现,将这些平面片段替换为小型三维骨架有时可以提高药物的溶解性、延长体内半衰期并减少不良代谢途径。本文探讨了一种构建此类三维构件的新方法,可能为药物设计者在调节药物性能时提供新的选择。
从平面环到微型骨架
药物分子中常含有含氮环,这类结构在获批药物中很常见,但也可能面临快速代谢等问题。近年来,被称为桥联双环的紧凑笼状结构已成为取代简单苯环的“替身”,它们在保持关键原子间距相似的同时提供更具三维性的形状。然而,用于模拟含氮环的近缘结构更难合成,尤其是那些在受张力的四元环中包含氮原子的版本。这类罕见骨架称为6-氮杂双环[3.1.1]庚烷,理论上具有诱人的性质,但缺乏通用的合成路线。
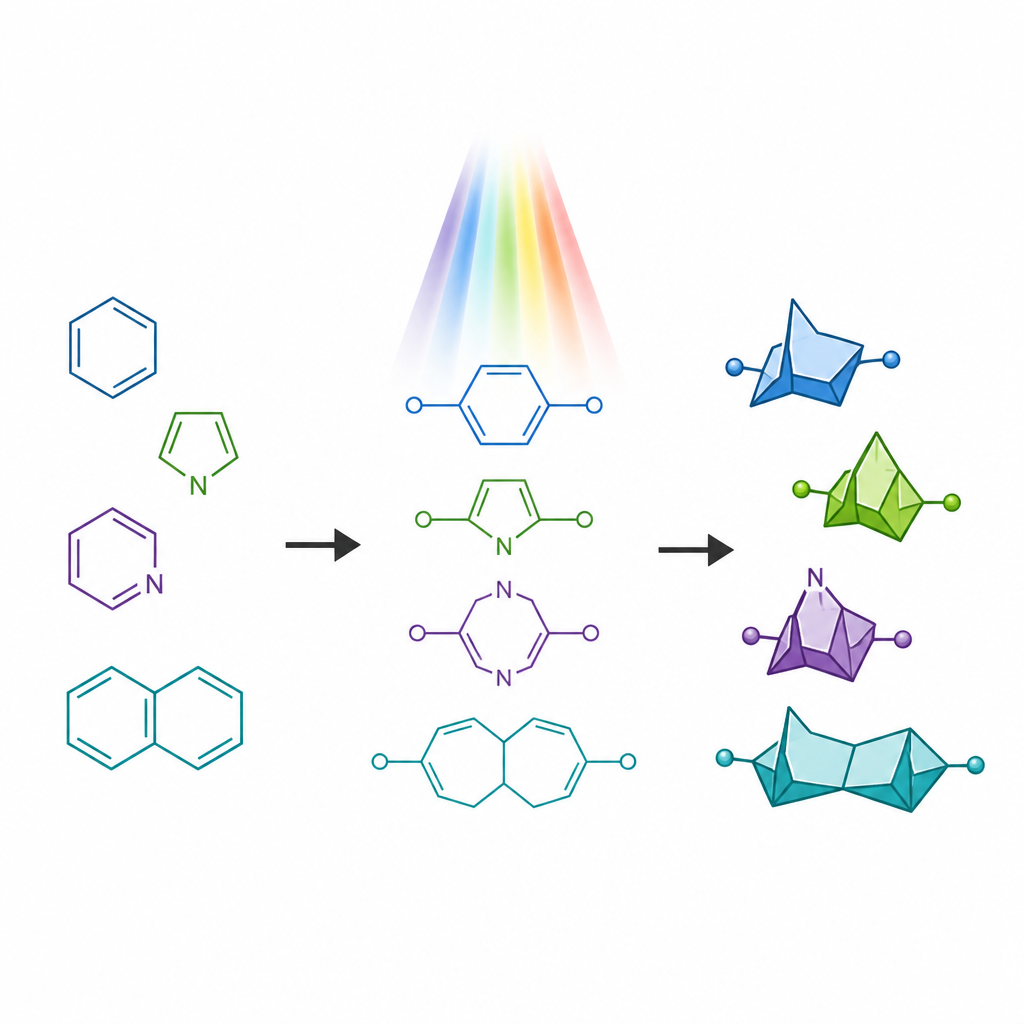
打破古老的环化规则
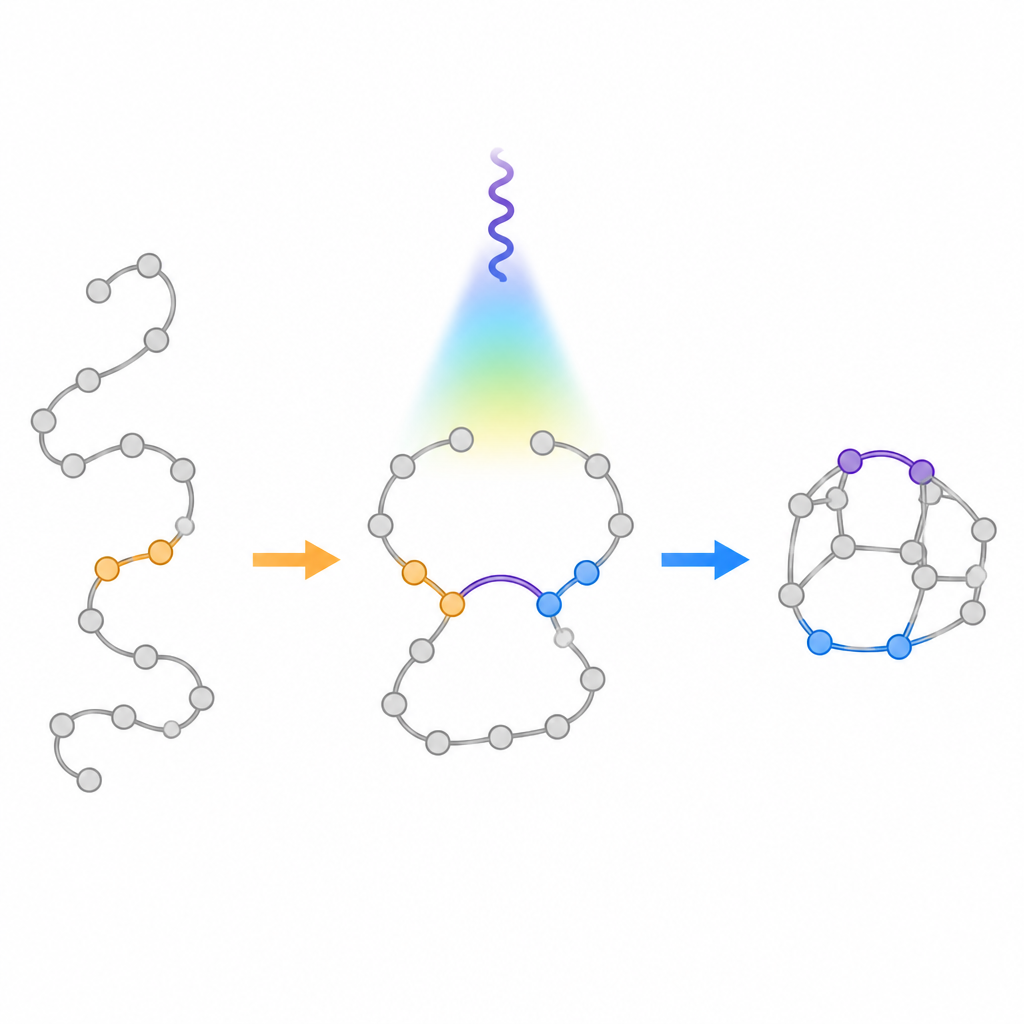
传统的光驱动方法将柔性链转化为环时,往往遵循一条被称为“五元环规则”的经验法则,偏向形成五元环而非六元环。当化学家用光照射含有两个双键的链状分子时,它们通常折叠形成较小的融合环,而不是所需的更大桥联笼。作者们有意推翻这一偏向,设计了一类称为氮代1,6-二烯的特殊起始物,这些分子在同一链上同时含有碳-碳双键和碳-氮双键。通过在链的特定位置引入能稳定自由基的基团,他们试图减缓通常的五元环路径,从而引导分子走向六元桥联笼。
用温和的光引导结构转变
团队开发了一种可见光工艺,使用光催化剂将能量转移到氮代1,6-二烯而不改变其电荷。分子被激发后短暂形成一对自由基中间体,两个活性位点可通过不同方式闭合。计算结果表明,在关键位置引入苯环可稳定其中一个自由基并抬高不希望发生的五元闭合的能垒。实验验证了这一设计:在蓝光和含铱致敏剂的条件下,这些链可靠地折叠成目标桥联双环,仅产生少量融合副产物。该反应对多种取代环系均有效,包括来自真实药物的片段,并且可以放大到克级产量。
从新笼状骨架构建工具箱
获得新的6-氮桥联骨架后,作者展示了这些结构可以进一步多方向改造。一个带有乙烯基的多功能产物通过氢化、臭氧分解和氧化等常规步骤被转化为醇、酸、胺及其他有用的官能团。与此同时,笼内的氮氧键可被还原露出次级胺,随后可制备脲类、磺酰胺、氨基甲酸酯和酰胺等衍生物。这类丰富的后续化学反应意味着刚性骨架可以承载多种侧链,这是药物发现中研究构效关系的关键。
在类药物环境中测试新形状
为探讨这些笼状结构在生物环境中的表现,研究者构建了已知酶抑制剂的类似物,用新的3,6-二氮杂双环[3.1.1]庚烷核心替换了柔性的哌嗪环。在人肝微粒体中的测定显示,改造后的分子分子量略高但疏水性降低,这一变化常与溶解性改善相关,同时保留了与原化合物相近的代谢稳定性。这些早期结果表明,新骨架可以替代常见的含氮环而不损害关键的类药物性质。
对未来药物的意义
简言之,该研究展示了如何诱导受激分子打破对小环的既有偏好,转而形成紧凑的三维笼状结构,这些结构在很大程度上模拟常见的含氮环。由于这些新形状易于引入多样化取代基且代谢上表现稳健,它们为医药化学家在调整溶解性、稳定性与分子形状时提供了新的拼搭部件。尽管还需更多生物学测试,这一“反五元环规则”策略打开了新的化学空间,可能有助于未来药物更有效且在体内更持久地发挥作用。
引用: Zhang, ZX., Shu, K., Tilby, M.J. et al. Breaking the ‘rule-of-five’ to access bridged bicyclic heteroaromatic bioisosteres. Nat. Synth 5, 790–797 (2026). https://doi.org/10.1038/s44160-026-00990-0
关键词: 光化学, 生物等排体, 药物设计, 杂环化合物, 可见光催化