Clear Sky Science · it
Infrangere la «regola dei cinque» per accedere a bioisosteri eteroaromatici biciclici bridged
Perché le pillole tridimensionali contano
Molti farmaci moderni sono costruiti a partire da molecole ad anello piatte che si inseriscono nei target proteici come chiavi nelle serrature. I chimici hanno scoperto che sostituire questi frammenti piatti con piccoli assortimenti tridimensionali può talvolta rendere i farmaci più solubili, più duraturi nell'organismo e meno soggetti a degradazione indesiderata. Questo articolo esplora un nuovo modo di costruire tali blocchi 3D che potrebbe offrire ai progettisti di farmaci opzioni fresche per modulare il comportamento di una medicina.
Da anelli piatti a minuscoli telai
Le molecole farmaceutiche spesso contengono anelli azotati, comuni nei medicinali approvati ma soggetti a problemi come metabolismo rapido. Negli ultimi anni, strutture compatte a gabbia chiamate bridged bicycles sono emerse come «sostituti» di semplici anelli benzenici, offrendo una forma più tridimensionale mantenendo distanze simili tra atomi chiave. Tuttavia, parenti stretti che imitano anelli contenenti azoto sono stati molto più difficili da ottenere, specialmente le versioni in cui un atomo di azoto si trova all'interno di un anello teso a quattro membri. Questi rari telai, noti come 6-azabicyclo[3.1.1]eptani, sono previsti avere proprietà interessanti ma sono mancati di rotte sintetiche generali.
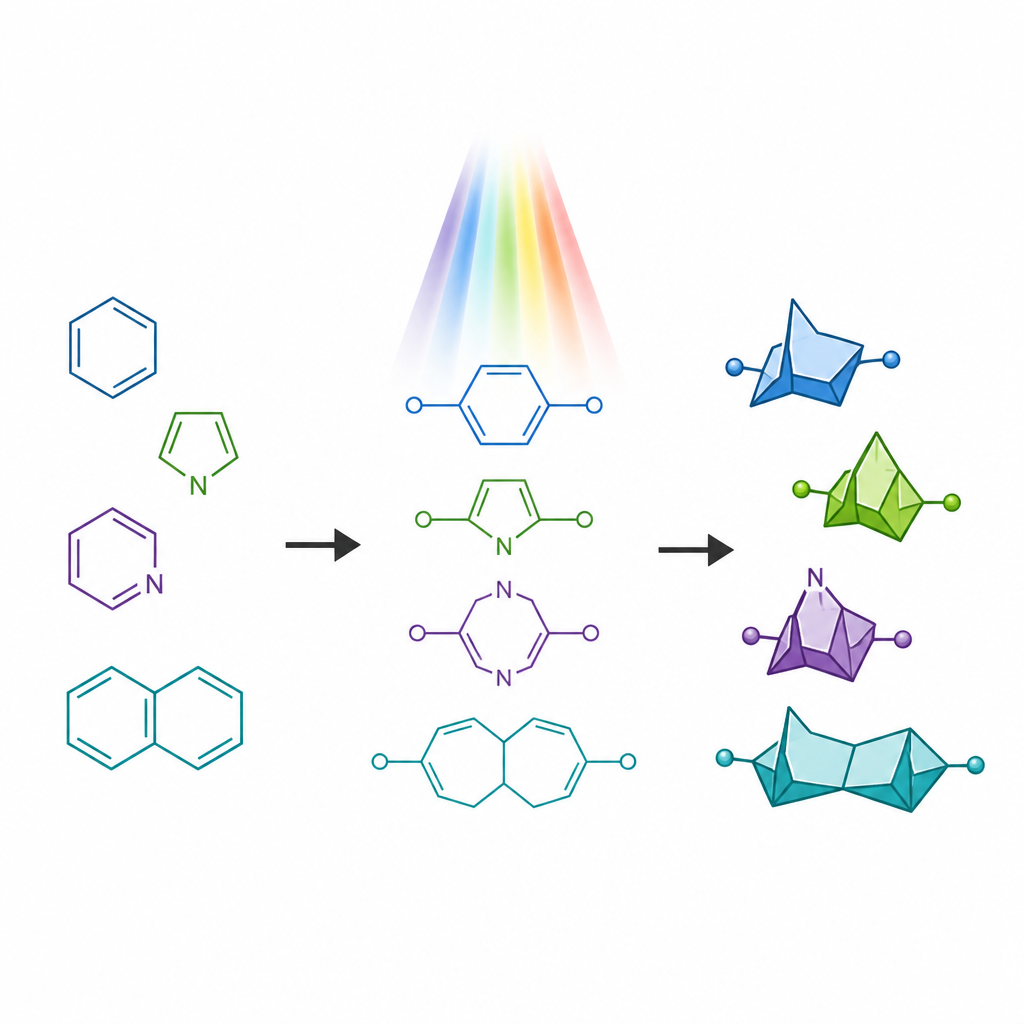
Infrangere una vecchia regola nella costruzione degli anelli
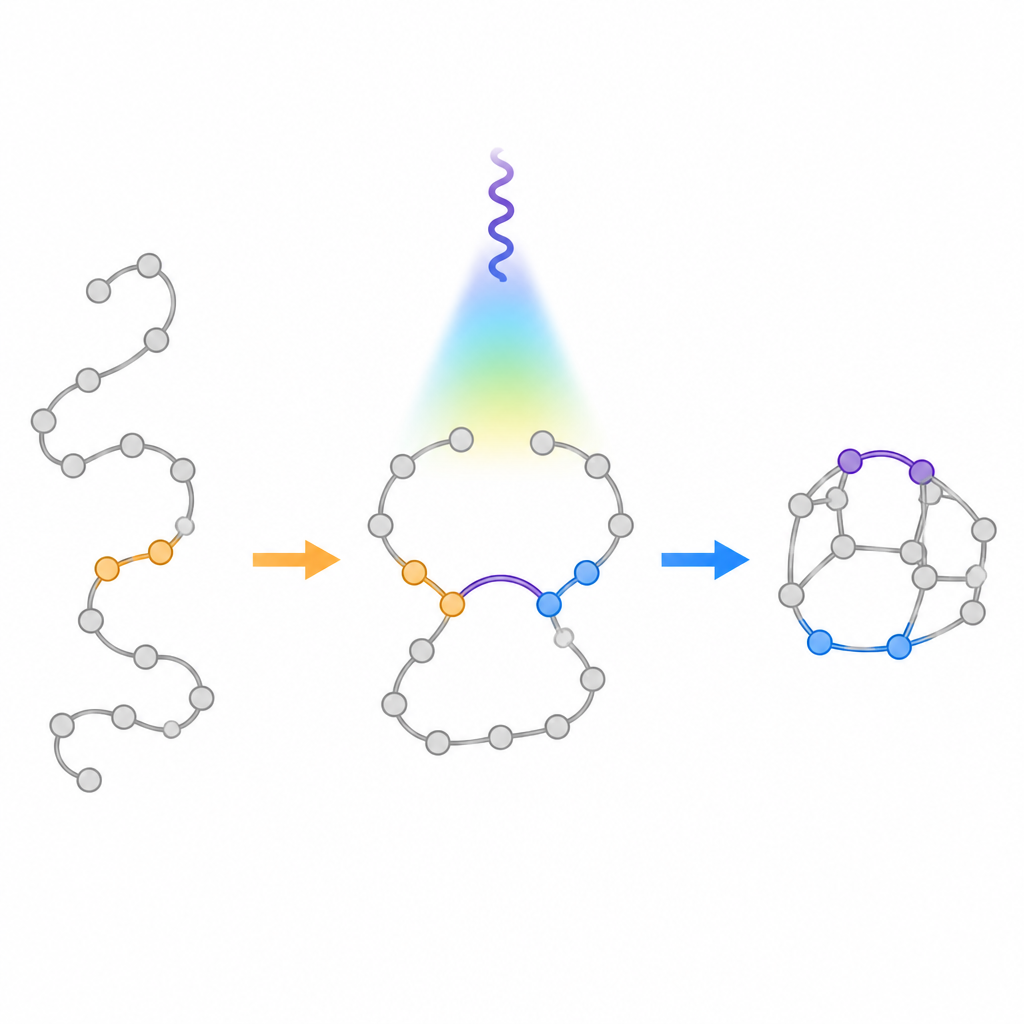
I metodi tradizionali indotti dalla luce per trasformare catene flessibili in anelli tendono a rispettare una vecchia linea guida chiamata «regola dei cinque», che favorisce la formazione di anelli a cinque membri rispetto a quelli a sei membri. Quando i chimici irradiano con luce certe molecole a catena con due doppi legami, di solito si ripiegano per dare anelli fusi più piccoli piuttosto che le più grandi gabbie bridged desiderate qui. Gli autori si sono posti l'obiettivo di ribaltare deliberatamente questo bias. Hanno progettato materiali di partenza speciali chiamati aza-1,6-dieni che contengono sia un doppio legame carbonio-carbonio sia un doppio legame carbonio-azoto collegati nella stessa catena. Posizionando un gruppo che stabilizza i radicali in una posizione specifica lungo la catena, hanno mirato a rallentare la via comune verso l'anello a cinque membri e invece indirizzare la molecola verso la gabbia bridged a sei membri.
Usare luce gentile per guidare la trasformazione
Il team ha sviluppato un processo con luce visibile che usa un fotocatalizzatore per trasferire energia agli aza-1,6-dieni senza cambiarne la carica. Una volta eccitate, queste molecole formano brevemente un intermedio biradicale in cui due siti reattivi possono chiudersi in modi diversi. Calcoli computazionali hanno suggerito che l'attacco di un anello fenile nella posizione chiave avrebbe stabilizzato uno di questi radicali e innalzato la barriera per la chiusura indesiderata a cinque membri. Gli esperimenti hanno confermato questo progetto: sotto luce blu in presenza di un sensibilizzatore a base di iridio, le catene si sono ripiegate in modo affidabile nei bridged bicycles mirati, con solo piccole quantità di sottoprodotti fusi. La reazione ha funzionato su molti anelli diversi attaccati, inclusi frammenti estratti da farmaci reali, e può essere scalata a quantità grammo.
Costruire una cassetta degli attrezzi dalle nuove gabbie
Una volta ottenuti i nuovi telai bridged a 6 atomi di azoto, gli autori hanno dimostrato che possono essere ulteriormente modificati in molte direzioni. Un prodotto versatile contenente un gruppo vinilico è stato trasformato in alcoli, acidi, amine e altri manipoli utili tramite passaggi standard come idrogenazione, ozonolisi e ossidazione. Parallelamente, il legame azoto-ossigeno all'interno della gabbia poteva essere ridotto per rivelare un'amina secondaria, poi funzionalizzata con uree, sulfonamidi, carbammati e ammidi. Questa ricca chimica di follow-up significa che il nucleo rigido può supportare una grande varietà di catene laterali, un requisito chiave per esplorare le relazioni struttura-attività nella scoperta di farmaci.
Testare le nuove forme in un contesto simile a un farmaco
Per sondare come queste gabbie possano comportarsi in un contesto biologico, i ricercatori hanno costruito un analogo di un noto inibitore enzimatico, sostituendo un anello piperazina flessibile con un nuovo nucleo 3,6-diazabicyclo[3.1.1]eptano. Misurazioni in microsomi di fegato umano hanno mostrato che la molecola modificata aveva un peso molecolare leggermente più alto ma una lipofilia inferiore, un cambiamento spesso correlato a una migliore solubilità, mantenendo al contempo una stabilità metabolica simile al composto originale. Questi risultati preliminari suggeriscono che i nuovi telai possono sostituire i comuni anelli contenenti azoto senza compromettere le proprietà chiave simili a quelle dei farmaci.
Cosa significa per i medicinali futuri
In termini semplici, lo studio mostra come indurre molecole eccitate dalla luce a rompere una vecchia preferenza per anelli più piccoli e invece formare compatte gabbie tridimensionali che imitano da vicino gli anelli contenenti azoto familiari. Poiché queste nuove forme possono essere facilmente funzionalizzate e sembrano metabolicamente robuste, offrono ai chimici medicinali nuovi pezzi da inserire nei progetti di farmaci per regolare solubilità, stabilità e forma. Pur richiedendo ulteriori test biologici, questa strategia «anti regola dei cinque» apre nuovi spazi chimici che potrebbero aiutare i futuri medicinali a funzionare meglio e durare più a lungo nell'organismo.
Citazione: Zhang, ZX., Shu, K., Tilby, M.J. et al. Breaking the ‘rule-of-five’ to access bridged bicyclic heteroaromatic bioisosteres. Nat. Synth 5, 790–797 (2026). https://doi.org/10.1038/s44160-026-00990-0
Parole chiave: fotochimica, bioisostere, progettazione di farmaci, eterocicli, catalisi con luce visibile