Clear Sky Science · ru
Нарушая «правило пяти» ради доступа к мостиковым бициклическим гетероароматическим биоизостерам
Почему трёхмерные лекарства важны
Многие современные препараты построены из плоских циклических молекул, которые входят в белковые мишени как ключ в замок. Химики выявили, что замена этих плоских фрагментов на небольшие трёхмерные каркасы иногда делает лекарства более растворимыми, дольше сохраняющимися в организме и менее склонными к нежелательному распаду. В этой статье рассматривается новый способ создания таких 3D‑блоков, который может дать дизайнерам лекарств новые опции при тонкой настройке свойств препарата.
От плоских колец к компактным каркасам
Молекулы лекарств часто содержат азотсодержащие кольца, которые распространены среди одобренных препаратов, но могут страдать от таких проблем, как быстрое метаболическое преобразование. В последние годы компактные каркасные структуры, называемые мостиковыми бициклями, появились как «заместители» простых бензольных колец, предлагая более трёхмерную форму при сохранении расстояний между ключевыми атомами. Однако близкие аналоги, имитирующие азотсодержащие кольца, оказались гораздо труднее синтезируемыми, особенно варианты, где атом азота находится в сжатом четырёхчленном кольце. Эти редкие каркасы, известные как 6‑азабицикло[3.1.1]гептаны, предсказываются как обладающие привлекательными свойствами, но им долго не хватало общих синтетических маршрутов.
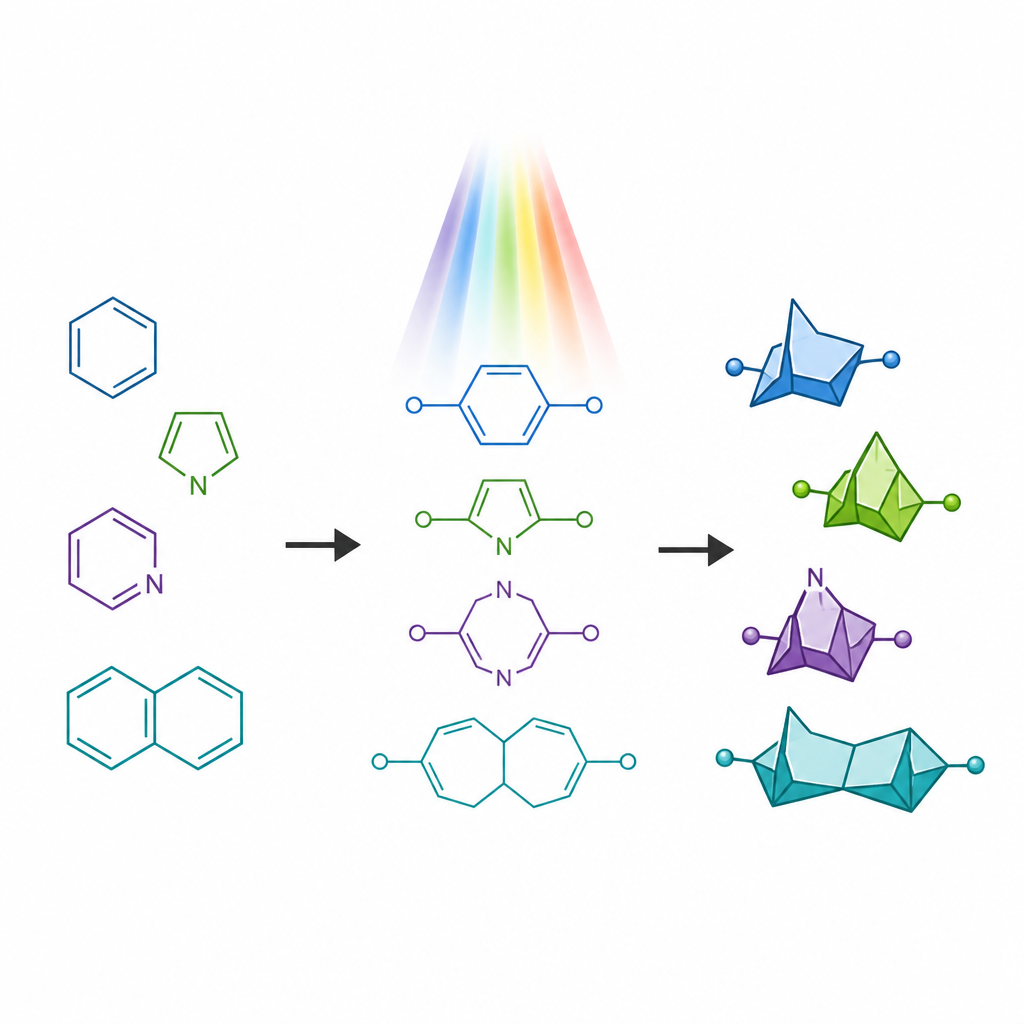
Нарушая старое правило построения колец
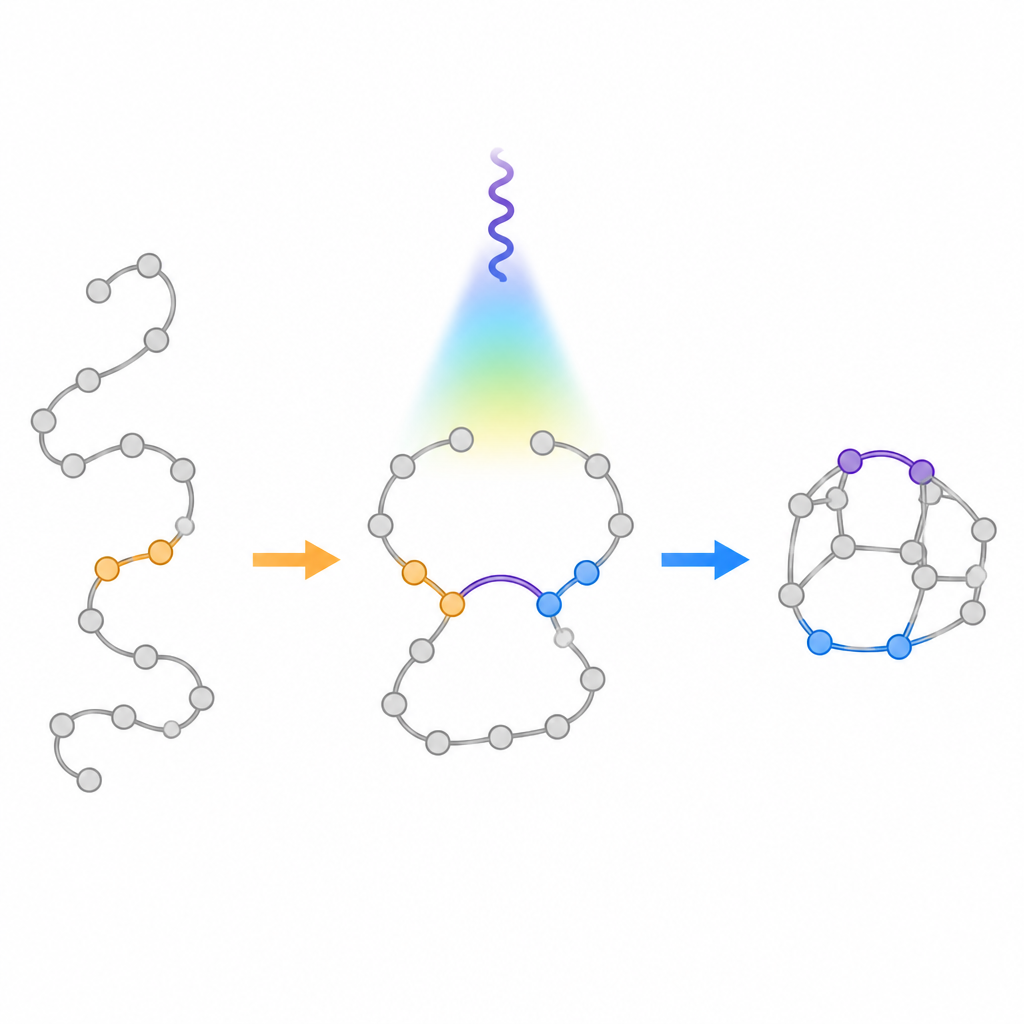
Традиционные методы, запускаемые светом, превращающие гибкие цепи в кольца, как правило, подчиняются старому правилу «правила пяти», которое отдаёт предпочтение образованию пятичленных колец перед шестичленными. Когда химики облучают определённые линейные молекулы с двумя двойными связями, они обычно складываются, давая меньшие конденсированные кольца вместо больших желаемых мостиковых каркасов. Авторы поставили цель сознательно опровергнуть эту предвзятость. Они спроектировали специальные исходные материалы — аза‑1,6‑диены, содержащие как углеродно‑углеродную, так и углеродно‑азотную двойную связь в одной цепи. Поместив в определённой позиции группу, стабилизирующую радикалы, они стремились замедлить привычный путь образования пятичленного кольца и направить молекулу к образованию шестичленного мостикового каркаса.
Использование мягкого света для направления превращения
Группа разработала процесс с видимым светом, который использует фотокатализатор для передачи энергии аза‑1,6‑диенам без изменения их заряда. При возбуждении эти молекулы кратковременно формируют бирадикальный интермедиат, в котором два реакционноспособных центра могут замыкаться разными путями. Вычисления подсказали, что присоединение фенильного кольца в ключевой позиции стабилизирует один из радикалов и повысит барьер для нежелательной пятичленной замыкания. Эксперименты подтвердили эту стратегию: под синим светом в присутствии иридиевого сенсибилизатора цепи надёжно складывались в целевые мостиковые бициклы, с лишь незначительными количествами конденсированных побочных продуктов. Реакция работала с широким набором присоединённых фрагментов, включая фрагменты из реальных лекарств, и её удалось масштабировать до граммовых количеств.
Создание набора инструментов из новых каркасов
Получив новые 6‑азотсодержащие мостиковые каркасы, авторы показали, что их можно далее разнообразно модифицировать. Один универсальный продукт с винильной группой был превращён в спирты, кислоты, амины и другие полезные функциональные группы стандартными приёмами — гидрированием, озонолизом и окислением. Параллельно азотно‑кислородная связь внутри каркаса могла быть восстановлена, открывая вторичный амин, который затем модифицировали уреями, сульфонамидами, карбаматами и амидами. Это богатое дальнейшее химическое разнообразие означает, что жёсткое ядро может нести широкий набор боковых цепей — ключевое требование для изучения взаимосвязи структуры и активности в поиске лекарств.
Проверка новых форм в условиях, близких к лекарственным
Чтобы оценить, как эти каркасы могут вести себя в биологическом контексте, исследователи создали аналог известного ингибитора фермента, заменив гибкое кольцо пиперазина на новый 3,6‑диазабицикло[3.1.1]гептановый каркас. Измерения в человеческих печёночных микросомах показали, что модифицированная молекула имела несколько большую молекулярную массу, но меньшую липофильность — изменение, часто связанное с улучшенной растворимостью, при сохранении сходной метаболической стабильности по сравнению с исходным соединением. Эти ранние результаты указывают, что новые каркасы могут замещать распространённые азотные кольца, не ухудшая ключевые лекарственные свойства.
Чего ожидать для будущих препаратов
Проще говоря, исследование показывает, как заставить возбуждённые светом молекулы преодолеть старое предпочтение к образованию меньших колец и вместо этого формировать компактные трёхмерные каркасы, близко имитирующие знакомые азотсодержащие кольца. Поскольку эти новые формы легко функционализируются и кажутся метаболически устойчивыми, они предлагают медицинам‑химикам новые фрагменты для встраивания в проекты лекарств при настройке растворимости, стабильности и формы. Хотя требуется больше биологических испытаний, эта стратегия «против правила пяти» открывает новое химическое пространство, которое может помочь будущим препаратам работать лучше и дольше сохраняться в организме.
Цитирование: Zhang, ZX., Shu, K., Tilby, M.J. et al. Breaking the ‘rule-of-five’ to access bridged bicyclic heteroaromatic bioisosteres. Nat. Synth 5, 790–797 (2026). https://doi.org/10.1038/s44160-026-00990-0
Ключевые слова: фотохимия, биоизостер, дизайн лекарств, гетероциклы, катализ видимым светом