Clear Sky Science · pl
Łamanie „reguły pięciu” w dostępie do bridżowanych dwupierścieniowych heteroaromatycznych bioizosterów
Dlaczego trójwymiarowe tabletki mają znaczenie
Wiele współczesnych leków zbudowanych jest z płaskich, pierścieniowych cząsteczek, które pasują do białkowych celów jak klucze do zamków. Chemicy przekonali się, że wymiana tych płaskich fragmentów na niewielkie, trójwymiarowe ramy może czasem poprawić rozpuszczalność, wydłużyć czas działania w organizmie i zmniejszyć podatność na niepożądany rozpad. Ten artykuł opisuje nowy sposób budowy takich 3D-cegiełek, który może dać projektantom leków nowe opcje przy dostrajaniu zachowania substancji leczniczych.
Z płaskich pierścieni do małych ram
Cząsteczki leków często zawierają pierścienie z azotem, powszechne w zatwierdzonych lekach, ale narażone na problemy, takie jak szybki metabolizm. W ostatnich latach pojawiły się zwarte, klatkowe struktury zwane bridżowanymi dwupierścieniami, które pełnią rolę „zamienników” dla prostych pierścieni benzenowych, oferując bardziej trójwymiarowy kształt przy zachowaniu podobnego rozmieszczenia kluczowych atomów. Jednak bliscy kuzyni naśladujący pierścienie zawierające azot są znacznie trudniejsi do otrzymania, szczególnie wersje, w których atom azotu znajduje się w napiętym, czteroatomowym pierścieniu. Te rzadkie ramy, znane jako 6-azabicyclo[3.1.1]heptany, prognozowane są jako posiadające atrakcyjne właściwości, lecz brakowało dla nich ogólnych dróg syntezy.
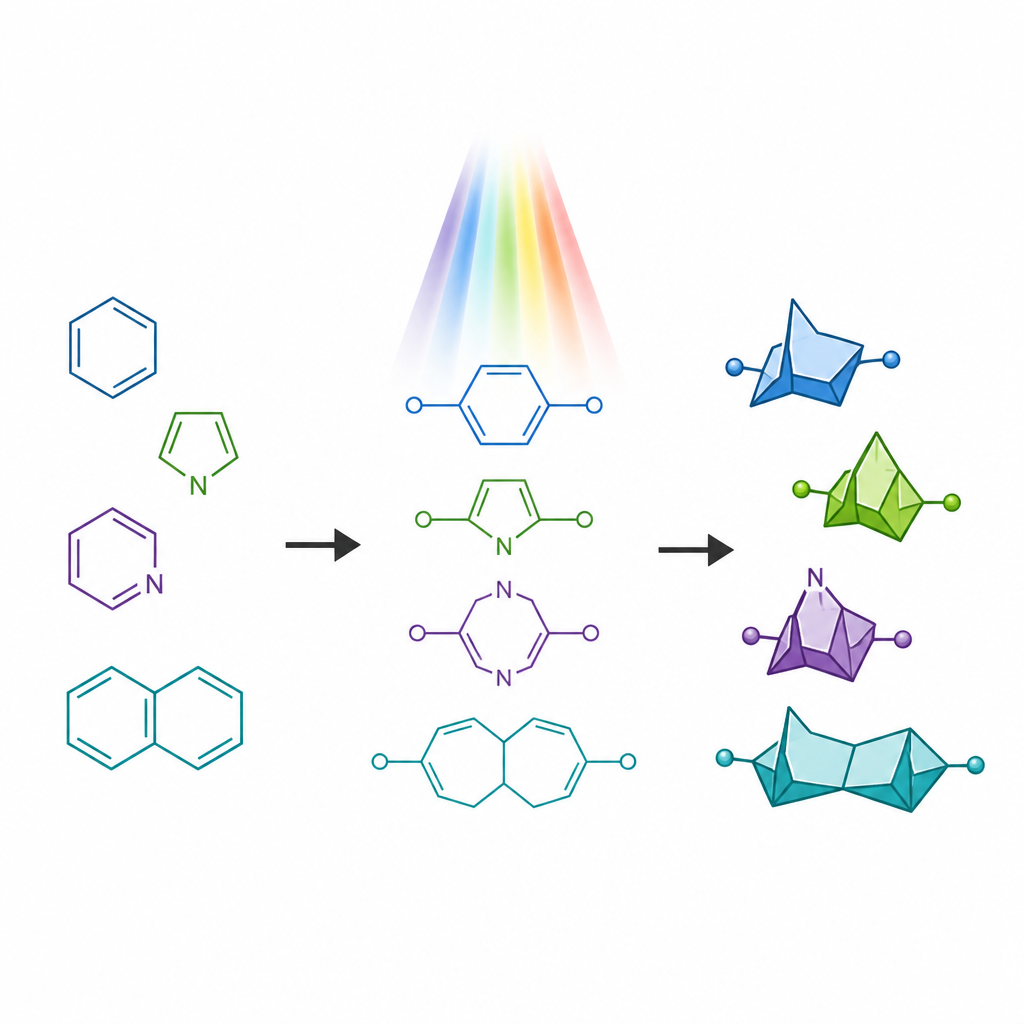
Łamanie starej reguły budowy pierścieni
Tradycyjne, światłem napędzane metody zamiany elastycznych łańcuchów w pierścienie zwykle przestrzegają dawnej wskazówki zwanej „regułą pięciu”, która sprzyja powstawaniu pięcioczłonowych pierścieni kosztem sześcioczłonowych. Gdy chemicy oświetlają pewne łańcuchowe molekuły zawierające dwa podwójne wiązania, zwykle składają się one do mniejszych, zespolonych pierścieni zamiast pożądanych większych bridżowanych klatek. Autorzy postanowili celowo odwrócić to uprzedzenie. Zaprojektowali specjalne substraty zwane aza-1,6-dienami, które zawierają zarówno podwójne wiązanie węglowo-węglowe, jak i węglowo-azotowe połączone w tym samym łańcuchu. Umieszczając grupę stabilizującą rodniki w określonej pozycji na łańcuchu, dążyli do spowolnienia zwykłej ścieżki prowadzącej do pięcioczłonowego zamknięcia i skierowania molekuły ku powstaniu sześcioczłonowej bridżowanej klatki.
Użycie łagodnego światła do pokierowania przemianą
Zespół opracował proces wykorzystujący światło widzialne i fotokatalizator do przekazania energii aza-1,6-dienom bez zmiany ich ładunku. Po wzbudzeniu te molekuły krótkotrwale tworzą biradikowy pośrednik, w którym dwa reaktywne centra mogą zamykać się różnymi drogami. Obliczenia komputerowe zasugerowały, że przyłączenie pierścienia fenylowego w kluczowej pozycji ustabilizuje jeden z tych rodników i podniesie barierę dla niepożądanego pięcioczłonowego zamknięcia. Eksperymenty potwierdziły ten projekt: pod niebieskim światłem w obecności irydowego sensityzera łańcuchy niezawodnie składały się do wybranych bridżowanych dwupierścieni, z jedynie niewielką ilością produktów zespolonych. Reakcja działała dla wielu różnych dołączonych pierścieni, w tym fragmentów pochodzących z rzeczywistych leków, i dała się skalować do gramowych ilości.
Budowanie zestawu narzędzi z nowych klatek
Gdy nowe, 6-azotowe bridżowane ramy były dostępne, autorzy pokazali, że można je dalej modyfikować na wiele sposobów. Jeden wszechstronny produkt z grupą winylową przekształcono w alkohole, kwasy, aminy i inne użyteczne funkcjonalności przez standardowe kroki, takie jak hydrogenacja, ozonoliza i utlenianie. Równolegle wiązanie azot-tlen wewnątrz klatki można było zredukować, odsłaniając aminę drugorzędową, którą następnie modyfikowano przez wprowadzenie ureatów, sulfonamidów, karbamin i amidów. Ta bogata chemia następcza oznacza, że sztywny rdzeń może nosić różnorodne łańcuchy boczne — kluczowy wymóg przy badaniu zależności struktura-aktywność w odkrywaniu leków.
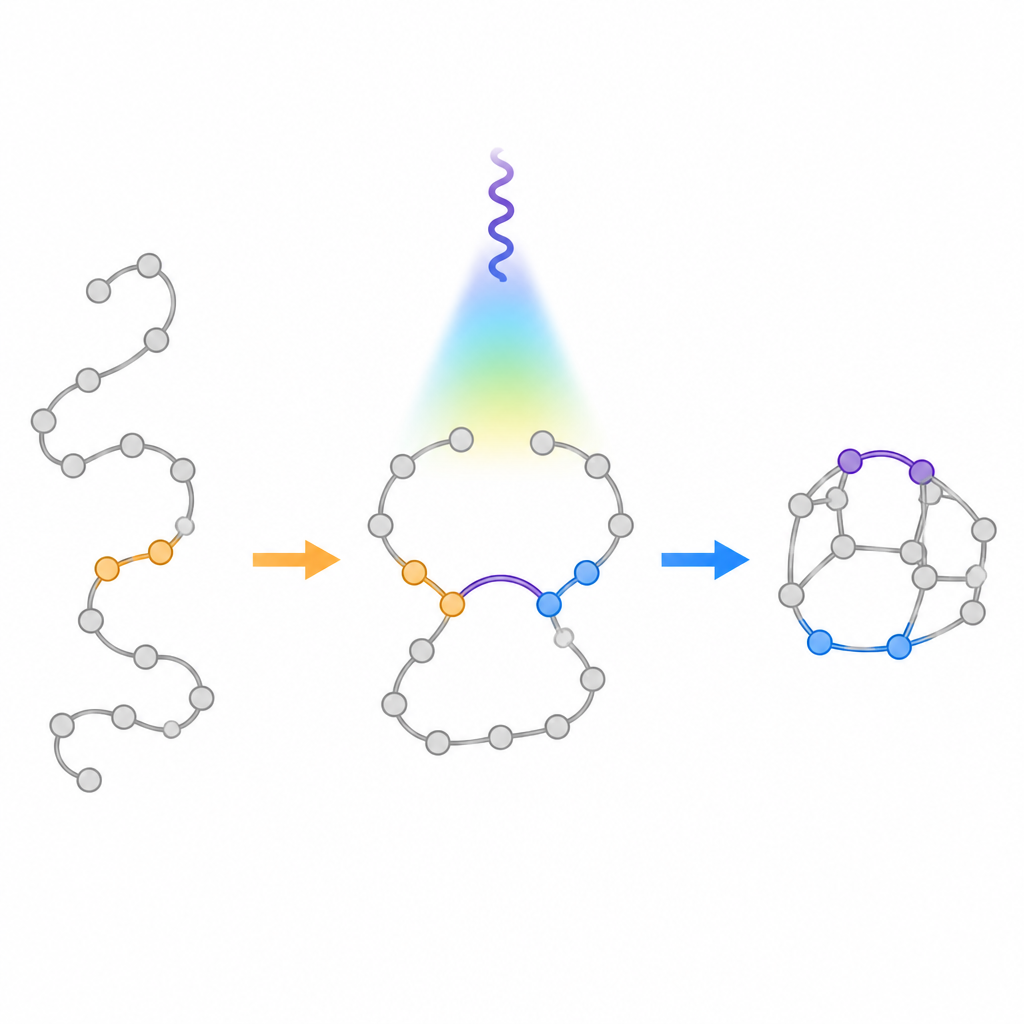
Testowanie nowych kształtów w kontekście typu leku
Aby sprawdzić, jak te klatki mogą się zachowywać w kontekście biologicznym, badacze zbudowali analog znanego inhibitora enzymu, zamieniając elastyczny pierścień piperazyny na nowy rdzeń 3,6-diazabicyclo[3.1.1]heptanu. Pomiary w ludzkich mikrosomach wątroby wykazały, że zmodyfikowana cząsteczka miała nieco większą masę molową, lecz niższą lipofilowość — zmianę często związaną z lepszą rozpuszczalnością — przy zachowaniu podobnej stabilności metabolicznej co związek oryginalny. Te wstępne wyniki sugerują, że nowe ramy mogą zastępować powszechne pierścienie azotowe bez uszczerbku dla kluczowych właściwości przypominających leki.
Co to oznacza dla przyszłych leków
Mówiąc prosto, badanie pokazuje, jak skłonić wzbudzone światłem molekuły do złamania starego przywiązania do mniejszych pierścieni i zamiast tego tworzenia zwartych, trójwymiarowych klatek, które ściśle naśladują znane pierścienie zawierające azot. Ponieważ nowe kształty można łatwo modyfikować i wydają się odporne metabolicznie, oferują chemikom medycznym nowe fragmenty do włączania w projekty leków przy dostrajaniu rozpuszczalności, stabilności i kształtu. Choć potrzebne są dalsze testy biologiczne, ta anty-reguła-pięciu strategia otwiera nową przestrzeń chemiczną, która może pomóc przyszłym lekom działać lepiej i dłużej pozostawać aktywnymi w organizmie.
Cytowanie: Zhang, ZX., Shu, K., Tilby, M.J. et al. Breaking the ‘rule-of-five’ to access bridged bicyclic heteroaromatic bioisosteres. Nat. Synth 5, 790–797 (2026). https://doi.org/10.1038/s44160-026-00990-0
Słowa kluczowe: fotochemia, bioizoster, projektowanie leków, heterocykle, kataliza światłem widzialnym