Clear Sky Science · ar
كسر «قاعدة الخمسة» للوصول إلى بدائل حيوية جسرية ثنائية الحلقات ذات حلقات عطرية تحتوي على ذرات غير الكربون
لماذا تهم الحبوب ثلاثية الأبعاد
تُبنى العديد من الأدوية الحديثة من جزيئات حلزية مسطحة تشبّه المفاتيح التي تدخل الأقفال البروتينية. تعلّم الكيميائيون أن استبدال هذه القطع المسطحة بأُطُر ثلاثية الأبعاد صغيرة يمكن أن يحسّن في بعض الأحيان ذائبية الأدوية، ويطيل مدة بقائها في الجسم، ويقلل احتمالات تفككها بطرق غير مرغوبة. تستعرض هذه المقالة طريقة جديدة لبناء مثل هذه الوحدات الثلاثية الأبعاد التي قد تمنح مصممي الأدوية خيارات جديدة عند تعديل سلوك الدواء.
من الحلقات المسطحة إلى الأُطُر الصغيرة
غالبًا ما تحتوي جزيئات الأدوية على حلقات حاملة للنيتروجين، وهي شائعة في الأدوية المعتمدة ولكنها قد تعاني من مشاكل مثل الأيض السريع. في السنوات الأخيرة ظهرت هياكل مضغوطة على شكل أقفاص تُدعى ثنائيات حلقية جسرية كـ«بدائل» للحلقات البنزينية البسيطة، مقدمة شكلاً ثلاثي الأبعاد مع الحفاظ على تباعد الذرات الرئيسي مماثلًا. ومع ذلك، فإن الأقارب التي تحاكي الحلقات الحاملة للنيتروجين كانت أصعب كثيرًا في التحضير، لا سيما النسخ التي تحتوي على ذرة نيتروجين داخل حلقة متوترة من أربعة أعضاء. تُعرف هذه الأُطُر النادرة باسم 6-أزابيسيكلو[3.1.1]هيبتانات، ويتوقع أن تمتلك خصائص جذابة لكنها افتقرت إلى طرق تخليق عامة.
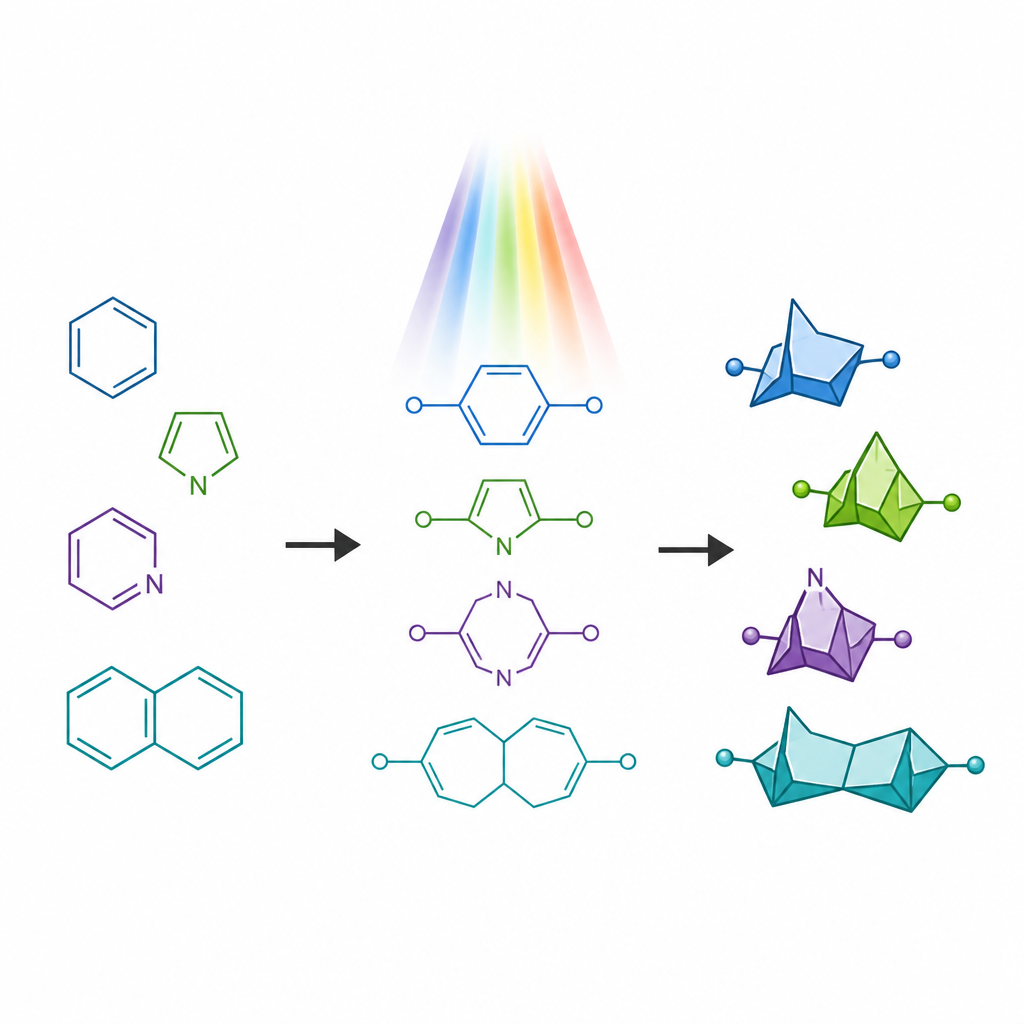
كسر قاعدة قديمة في بناء الحلقات
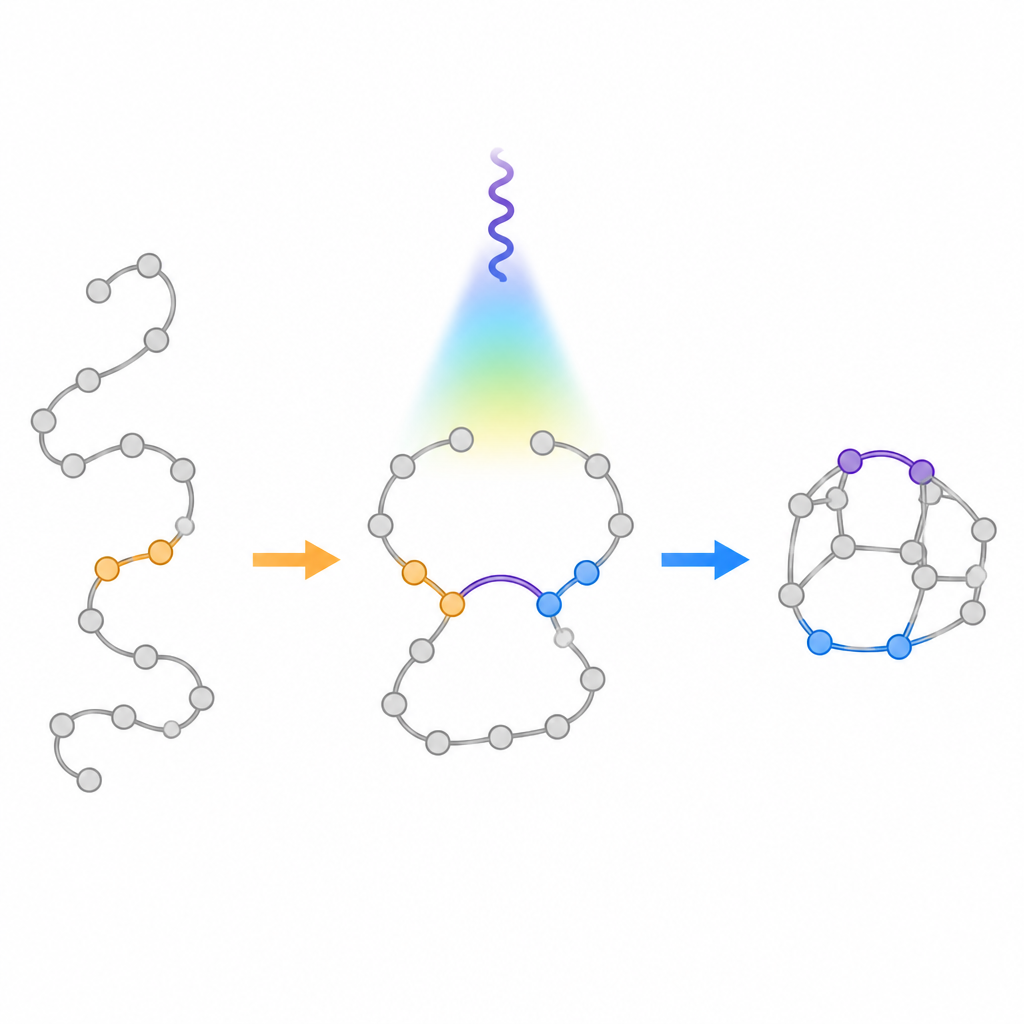
تميل الطرق التقليدية المدفوعة بالضوء لتحويل سلاسل مرنة إلى حلقات إلى الامتثال لتوجيه قديم يُسمى «قاعدة الخمسة»، التي تفضّل تكوّن حلقات من خمسة أعضاء على تلك المكونة من ستة أعضاء. عندما يعرض الكيميائيون سلاسل جزيئية ذات رابطتي مزدوجتين للضوء، فإنها عادةً ما تنطوي لتشكل حلقات مدمجة أصغر بدلاً من الأقفاص الجسرية الأكبر المطلوبة هنا. انطلق المؤلفون بهدف دحض هذا الانحياز عمدًا. صمموا مواد بادئة خاصة تُدعى أزا-1,6-ديينات تحتوي كل منها على رابطة مزدوجة كربون-كربون ورابطة مزدوجة كربون-نيتروجين مرتبطة في نفس السلسلة. بوضع مجموعة تُثبّت الجذور الحرة في موقع محدد على السلسلة، سعوا إلى إبطاء المسار المعتاد لتشكيل الحلقة الخماسية وبدلاً من ذلك توجيه الجزيء نحو تكوين القفص الجسرى ذي الستة أعضاء.
استخدام ضوء لطيف لتوجيه التغيير
طور الفريق عملية تعمل بالضوء المرئي تستخدم حفّازًا ضوئيًا لنقل الطاقة إلى أزا-1,6-الديينات دون تغيير شحنتها. بعد إثارتها، تُشكل هذه الجزيئات مؤقتًا وسيطًا ثنائي الجذور حيث يمكن لموقعين تفاعليين أن يغلقا بعدة طرق. أشارت حسابات حاسوبية إلى أن ربط حلقة فينيلية في الموقع الأساسي سيُثبّت أحد هذه الجذور ويرفع حاجز إغلاق الحلقة الخماسية غير المرغوب فيه. أكدت التجارب هذا التصميم: تحت ضوء أزرق وبوجود حساس قائم على الإيريديوم، انطوت السلاسل بشكل موثوق لتُكوّن الثنائيات الجسرية المستهدفة، مع كميات ضئيلة فقط من المنتجات المدمجة الجانبية. نجحت التفاعل عبر العديد من الحلقات المرفقة المختلفة، بما في ذلك شظايا مأخوذة من أدوية حقيقية، ويمكن توسيعه إلى كميات غرامية.
بناء صندوق أدوات من الأقفاص الجديدة
بعد الحصول على هياكل الجسور المكونة من ستة نيتروجين الجديدة، أظهر المؤلفون أنها قابلة للتعديل بعدة اتجاهات. حُوّل منتج متعدد الاستخدامات يحمل مجموعة فينيلية إلى كحولات وأحماض وأمينات ومواضع أخرى مفيدة عبر خطوات قياسية مثل الهدرجة، والتحلل بالأوزون، والأكسدة. بالتوازي، كان من الممكن تقليل الرابطة نيتروجين-أكسجين داخل القفص لكشف أمين ثانوي، ثم تزويده بمجموعات اليوريا والسلفوناميد والكربامات والأميدات. تعني هذه الكيمياء اللاحقة الغنية أن النواة الصلبة يمكن أن تدعم تنوعًا واسعًا من السلاسل الجانبية، وهو شرط أساسي لاستكشاف علاقات البنية والنشاط في اكتشاف الأدوية.
اختبار الأشكال الجديدة في سياق شبيه بالدواء
لاستقصاء كيف قد تؤدي هذه الأقفاص في سياق بيولوجي، بنى الباحثون نظيرًا لمثبط إنزيم معروف، مستبدلين حلقة بيبرازين مرنة بنواة جديدة 3,6-ديوزابيسيكلو[3.1.1]هيبتان. أظهرت القياسات في ميكروزومات كبد بشرية أن الجزيء المعدل كان ذا كتلة جزيئية أعلى قليلًا لكنه أقل استقطابًا شحميًا، وهو تغيير غالبًا ما يرتبط بذائبية أفضل، مع احتفاظه باستقرار أيضي مشابه للمركب الأصلي. تشير هذه النتائج الأولية إلى أن الأُطُر الجديدة يمكن أن تحل محل الحلقات النيتروجينية الشائعة دون الإضرار بالخصائص الدوائية الأساسية.
ماذا يعني هذا لأدوية المستقبل
بعبارات بسيطة، تُظهر الدراسة كيفية إقناع الجزيئات المثارة بالضوء لكسر تفضيل قديم للحلقات الأصغر وتشكيل أقفاص ثلاثية الأبعاد مضغوطة تحاكي عن قرب الحلقات الحاملة للنيتروجين المألوفة. وبما أن هذه الأشكال الجديدة يمكن تزيينها بسهولة وتبدو قوية أيضيًا، فإنها تقدم للكيميائيين الدوائيين قطعًا جديدة يمكن إدراجها في تصميم الأدوية عند تعديل الذائبية والثبات والشكل. ومع ضرورة إجراء مزيد من الاختبارات البيولوجية، تفتح استراتيجية معاكسة لقاعدة الخمسة مساحة كيميائية جديدة قد تساعد الأدوية المستقبلية على العمل بشكل أفضل والدوام لفترة أطول في الجسم.
الاستشهاد: Zhang, ZX., Shu, K., Tilby, M.J. et al. Breaking the ‘rule-of-five’ to access bridged bicyclic heteroaromatic bioisosteres. Nat. Synth 5, 790–797 (2026). https://doi.org/10.1038/s44160-026-00990-0
الكلمات المفتاحية: الكيمياء الضوئية, بديل حيوي, تصميم الأدوية, حلقيات غير متجانسة, تتحفيز بالضوء المرئي