Clear Sky Science · de
Die „Rule-of-Five“ brechen, um zugängliche, überbrückte bicyclische heteroaromatische Bioisostere zu erhalten
Warum dreidimensionale Wirkstoffe wichtig sind
Viele moderne Medikamente basieren auf flachen, ringförmigen Molekülen, die in Proteinziele wie Schlüssel in Schlösser passen. Chemiker haben herausgefunden, dass der Austausch dieser flachen Bausteine durch kleine dreidimensionale Gerüste die Löslichkeit verbessern, die Verweildauer im Körper verlängern und den unerwünschten Abbau vermindern kann. Dieser Artikel untersucht eine neue Methode zum Aufbau solcher 3D-Bausteine, die Arzneimittelentwicklern zusätzliche Optionen beim Feinabstimmen des Verhaltens eines Wirkstoffs bieten könnte.
Von flachen Ringen zu winzigen Gerüsten
Wirkstoffmoleküle enthalten häufig stickstoffhaltige Ringe, die in zugelassenen Medikamenten weit verbreitet sind, aber Probleme wie raschen Stoffwechsel aufweisen können. In den letzten Jahren sind kompakte, käfigartige Strukturen, sogenannte überbrückte Bicycles, als Ersatz für einfache Benzolringe aufgekommen: Sie bieten eine stärker dreidimensionale Form und erhalten gleichzeitig die Anordnung wichtiger Atome. Enge Verwandte, die stickstoffhaltige Ringe nachahmen, waren jedoch weitaus schwerer herzustellen, insbesondere Varianten, bei denen ein Stickstoffatom in einem gespannte viergliedrigen Ring sitzt. Diese seltenen Gerüste, bekannt als 6-azabicyclo[3.1.1]heptane, werden aufgrund ihrer vorteilhaften Eigenschaften prognostiziert, verfügten aber bislang nicht über allgemeine Syntheserouten.
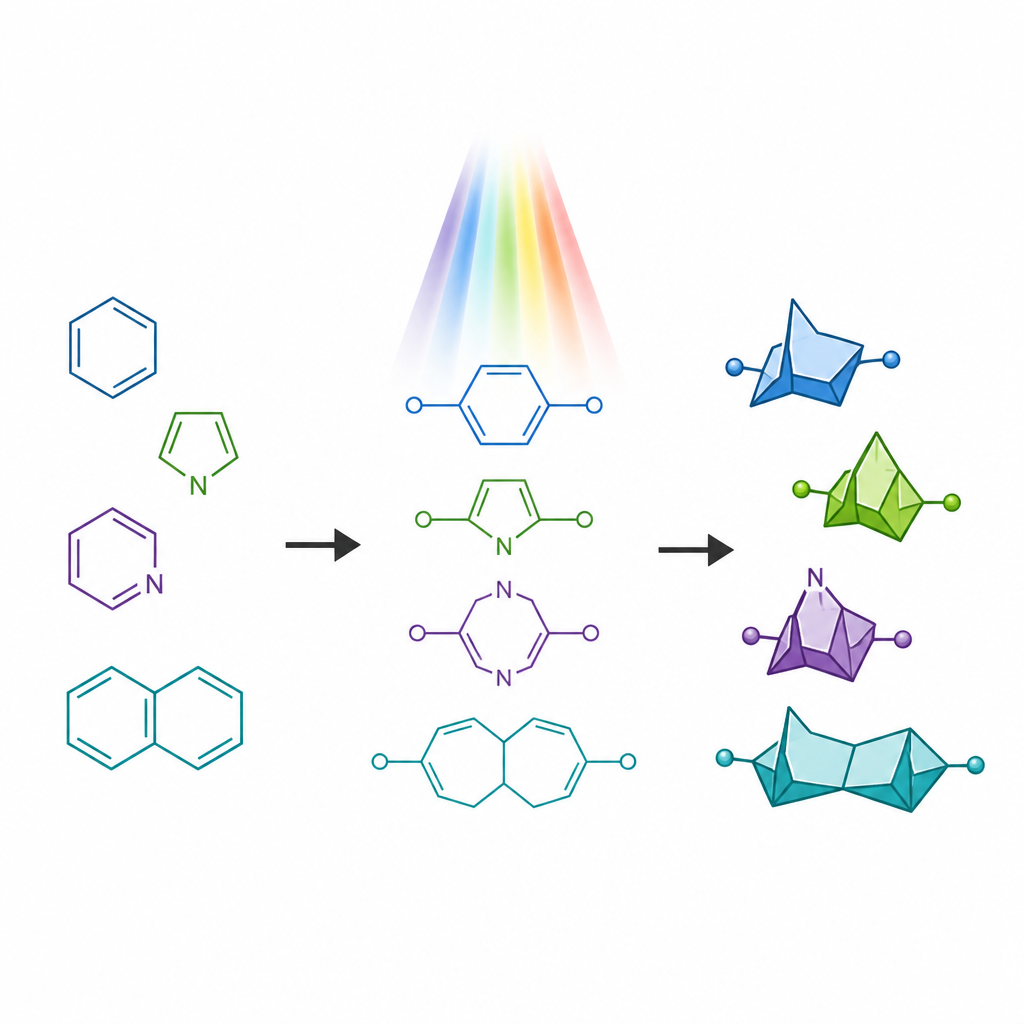
Eine alte Regel des Ringbaus brechen
Traditionelle, lichtgetriebene Methoden, um flexible Ketten in Ringe zu überführen, folgen oft einer alten Richtlinie, der sogenannten „Rule of Five“, die die Bildung von fünfgliedrigen Ringen gegenüber sechsgliedrigen begünstigt. Wenn Chemiker Licht auf bestimmte kettenartige Moleküle mit zwei Doppelbindungen scheinen lassen, falten sich diese normalerweise zu kleineren, fusionierten Ringen zusammen, statt zu den hier gewünschten überbrückten Käfigen. Die Autoren machten es sich zum Ziel, diese Voreingenommenheit gezielt zu überwinden. Sie entwickelten spezielle Ausgangsmaterialien, sogenannte aza-1,6-diene, die sowohl eine C=C- als auch eine C=N-Doppelbindung in derselben Kette enthalten. Durch das Platzieren einer Gruppe, die Radikale stabilisiert, an einer bestimmten Position der Kette wollten sie den üblichen Weg zur fünfgliedrigen Ringbildung verlangsamen und das Molekül stattdessen zur Bildung des sechsgliedrigen überbrückten Käfigs lenken.
Sanftes Licht zur Steuerung der Umwandlung
Das Team entwickelte einen Prozess mit sichtbarem Licht, der einen Photokatalysator verwendet, um Energie auf die aza-1,6-diene zu übertragen, ohne deren Ladungszustand zu verändern. Einmal angeregt, bilden diese Moleküle kurzzeitig ein Biradikal-Zwischenprodukt, in dem zwei reaktive Stellen auf unterschiedliche Weise schließen können. Rechnerische Untersuchungen deuteten darauf hin, dass die Anbringung eines Phenylrings an der Schlüsselposition eines dieser Radikale stabilisieren und die Barriere für die unerwünschte fünfgliedrige Schließung erhöhen würde. Experimente bestätigten dieses Design: Unter blauem Licht und in Gegenwart eines iridiumbasierten Sensitizers falteten sich die Ketten zuverlässig zu den angestrebten überbrückten Bicycles, mit nur geringen Anteilen an fusionierten Nebenprodukten. Die Reaktion funktionierte für viele verschiedene angehängte Ringe, einschließlich Fragmenten aus realen Wirkstoffen, und ließ sich auf Grammmaßstab skalieren.
Ein Werkzeugkasten aus den neuen Käfigen
Sobald die neuen 6‑Stickstoff-überbrückten Gerüste vorlagen, zeigten die Autoren, dass diese sich in viele Richtungen weiter modifizieren lassen. Ein vielseitiges Produkt mit einer Vinylgruppe wurde durch Standardschritte wie Hydrierung, Ozonolyse und Oxidation in Alkohole, Säuren, Amine und andere nützliche funktionelle Gruppen überführt. Parallel dazu konnte die N–O-Bindung im Käfig reduziert werden, um ein sekundäres Amin freizulegen, das dann mit Harnstoffen, Sulfonamiden, Carbamaten und Amiden weiter versehen wurde. Diese vielfältige Nachfolgechemie ermöglicht es, dem starren Kern eine große Bandbreite an Seitenketten anzuhängen — eine wesentliche Voraussetzung, um Struktur‑Aktivität‑Beziehungen in der Wirkstoffforschung zu erkunden.
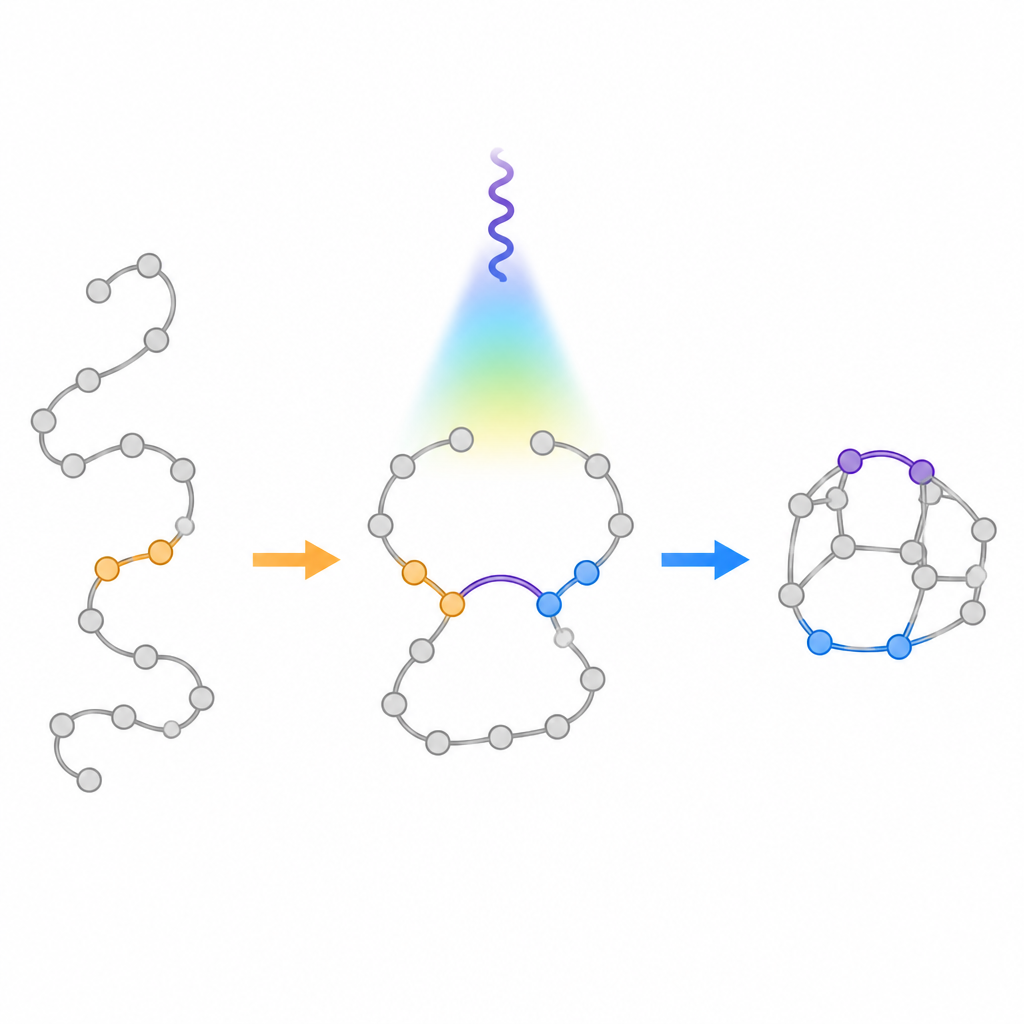
Testen der neuen Formen in einem wirkstoffähnlichen Kontext
Um zu prüfen, wie sich diese Käfige biologisch verhalten könnten, bauten die Forscher ein Analogon eines bekannten Enzyminhibitors, indem sie einen flexiblen Piperazinring gegen einen neuen 3,6-diazabicyclo[3.1.1]heptan-Kern austauschten. Messungen in humanen Lebermikrosomen zeigten, dass das modifizierte Molekül ein etwas höheres Molekulargewicht, aber geringere Lipophilie aufwies — eine Änderung, die häufig mit besserer Löslichkeit einhergeht — und gleichzeitig eine ähnliche metabolische Stabilität wie die ursprüngliche Verbindung beibehielt. Diese ersten Ergebnisse deuten darauf hin, dass die neuen Gerüste gängige Stickstoffringe ersetzen können, ohne zentrale wirkstoffähnliche Eigenschaften zu beeinträchtigen.
Was das für künftige Medikamente bedeutet
Vereinfacht gesagt demonstriert die Studie, wie man lichtangeregte Moleküle dazu bringt, eine alte Präferenz für kleinere Ringe zu durchbrechen und stattdessen kompakte, dreidimensionale Käfige zu bilden, die vertraute stickstoffhaltige Ringe eng nachahmen. Da sich diese neuen Formen leicht weiterfunktionalisieren lassen und offenbar metabolisch robust sind, bieten sie der medizinischen Chemie neue Bausteine, um Löslichkeit, Stabilität und Form von Wirkstoffen zu optimieren. Zwar sind weitere biologische Prüfungen nötig, doch eröffnet diese Anti‑Rule‑of‑Five‑Strategie neuen chemischen Raum, der künftigen Medikamenten helfen könnte, besser zu wirken und länger im Körper zu verbleiben.
Zitation: Zhang, ZX., Shu, K., Tilby, M.J. et al. Breaking the ‘rule-of-five’ to access bridged bicyclic heteroaromatic bioisosteres. Nat. Synth 5, 790–797 (2026). https://doi.org/10.1038/s44160-026-00990-0
Schlüsselwörter: Photochemie, Bioisostere, Wirkstoffdesign, Heterocyclen, Katalyse mit sichtbarem Licht