Clear Sky Science · pt
Quebrando a “regra dos cinco” para acessar bioisósteros heteroaromáticos bicicíclicos com pontes
Por que comprimidos tridimensionais importam
Muitos medicamentos modernos são construídos a partir de moléculas planas em forma de anel que se encaixam em alvos proteicos como chaves em fechaduras. Os químicos perceberam que substituir essas peças planas por pequenas estruturas tridimensionais pode, por vezes, tornar os fármacos mais solúveis, mais duradouros no organismo e menos propensos a degradarem-se de maneiras indesejadas. Este artigo explora uma nova forma de construir esses blocos 3D que pode oferecer aos projetistas de medicamentos opções frescas ao ajustar o comportamento de um remédio.
De anéis planos a estruturas minúsculas
Moléculas medicamentosas frequentemente contêm anéis com nitrogênio, comuns em fármacos aprovados, mas que podem sofrer com problemas como metabolismo rápido. Nos últimos anos, estruturas compactas em forma de gaiola, chamadas biciclos com ponte, surgiram como “substitutos” de anéis benzênicos simples, oferecendo uma forma mais tridimensional enquanto mantêm o espaçamento de átomos chave semelhante. Contudo, parentes próximos que imitam anéis contendo nitrogênio têm sido muito mais difíceis de sintetizar, especialmente versões em que um átomo de nitrogênio está dentro de um anel tensionado de quatro membros. Essas estruturas raras, conhecidas como 6-azabicyclo[3.1.1]heptanos, são previstas como tendo propriedades atraentes, mas careciam de rotas sintéticas gerais.
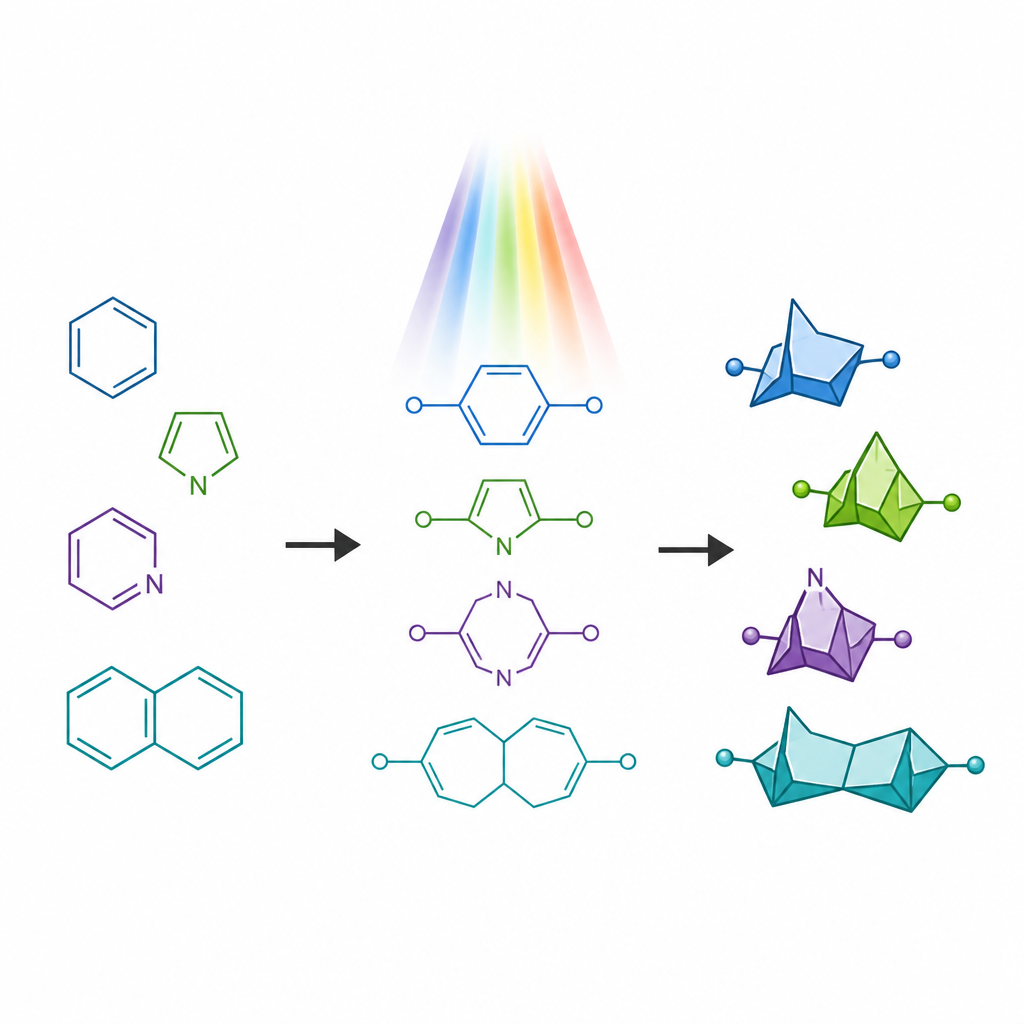
Quebrando uma velha regra da construção de anéis
Métodos tradicionais acionados por luz para transformar cadeias flexíveis em anéis tendem a obedecer a uma antiga diretriz chamada “regra dos cinco”, que favorece a formação de anéis de cinco membros em detrimento dos de seis. Quando os químicos iluminam certas moléculas em cadeia com duas duplas ligações, elas geralmente se dobram para dar anéis fundidos menores em vez das grandes gaiolas com ponte desejadas aqui. Os autores propuseram deliberadamente reverter esse viés. Eles projetaram materiais iniciais especiais chamados aza-1,6-dienos que contêm tanto uma dupla ligação carbono–carbono quanto uma dupla ligação carbono–nitrogênio conectadas na mesma cadeia. Ao posicionar um grupo que estabiliza radicais em uma posição específica da cadeia, buscaram desacelerar a via usual para anéis de cinco membros e, em vez disso, direcionar a molécula para formar a gaiola com ponte de seis membros.
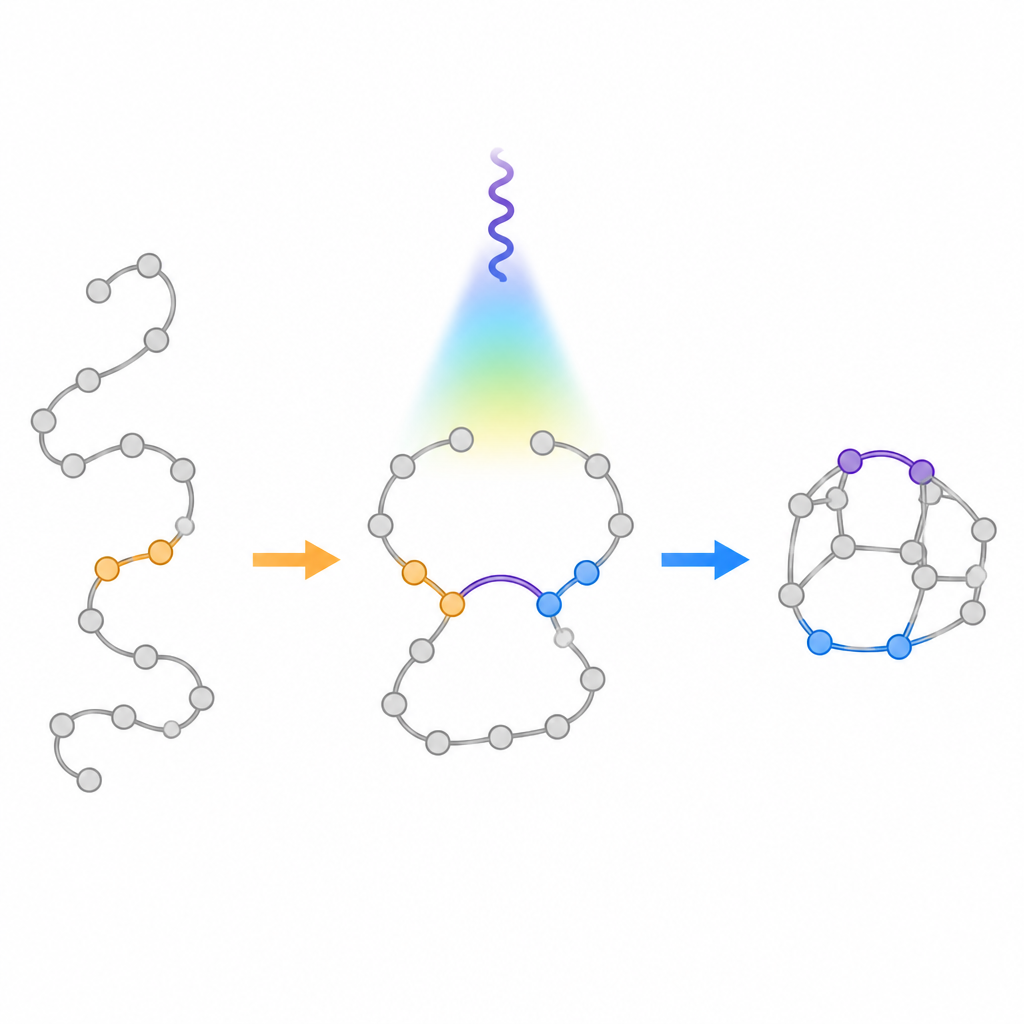
Usando luz suave para guiar a transformação
A equipe desenvolveu um processo com luz visível que usa um fotocatalisador para transferir energia aos aza-1,6-dienos sem alterar sua carga. Uma vez excitadas, essas moléculas formam brevemente um intermediário biradical no qual dois sítios reativos podem fechar de modos diferentes. Cálculos computacionais sugeriram que a instalação de um anel fenil na posição chave estabilizaria um desses radicais e elevaria a barreira para o fechamento indesejado de cinco membros. Experimentos confirmaram esse projeto: sob luz azul na presença de um sensibilizador à base de irídio, as cadeias se dobraram de maneira confiável para os biciclos com ponte almejados, com apenas pequenas quantidades dos subprodutos fundidos. A reação funcionou para muitos anéis ligados diferentes, incluindo fragmentos retirados de fármacos reais, e pôde ser escalada até escalas de gramas.
Construindo uma caixa de ferramentas a partir das novas gaiolas
Uma vez em mãos as novas estruturas bridged de 6 nitrogênios, os autores demonstraram que elas podem ser modificadas em muitas direções. Um produto versátil contendo um grupo vinílico foi transformado em álcoois, ácidos, aminas e outras funções úteis por etapas padrão como hidrogenação, ozonólise e oxidação. Em paralelo, a ligação nitrogênio–oxigênio dentro da gaiola pôde ser reduzida para revelar uma amina secundária, que foi então funcionalizada com ureas, sulfonamidas, carbamatos e amidas. Essa rica química subsequente significa que o núcleo rígido pode suportar uma ampla variedade de cadeias laterais, um requisito chave para explorar relações estrutura–atividade em descoberta de fármacos.
Testando as novas formas em um contexto semelhante a fármacos
Para sondar como essas gaiolas podem se comportar em um contexto biológico, os pesquisadores construíram um análogo de um inibidor enzimático conhecido, trocando um anel de piperazina flexível por um novo núcleo 3,6-diazabicyclo[3.1.1]heptano. Medições em microsomos hepáticos humanos mostraram que a molécula modificada tinha massa molecular ligeiramente maior, mas lipofilicidade menor — uma mudança frequentemente associada a melhor solubilidade — enquanto mantinha estabilidade metabólica semelhante ao composto original. Esses resultados iniciais sugerem que as novas estruturas podem substituir anéis nitrogenados comuns sem prejudicar propriedades farmacológicas chave.
O que isso significa para futuros medicamentos
Em termos simples, o estudo mostra como induzir moléculas excitadas pela luz a romper uma antiga preferência por anéis menores e, em vez disso, formar gaiolas compactas e tridimensionais que imitam de perto anéis contendo nitrogênio familiares. Como essas novas formas podem ser prontamente decoradas e mostram robustez metabólica, elas oferecem aos químicos medicinais peças novas para inserir em projetos de fármacos ao ajustar solubilidade, estabilidade e conformação. Embora sejam necessários mais testes biológicos, essa estratégia anti–regra dos cinco abre um novo espaço químico que pode ajudar futuros medicamentos a funcionarem melhor e a durarem mais no organismo.
Citação: Zhang, ZX., Shu, K., Tilby, M.J. et al. Breaking the ‘rule-of-five’ to access bridged bicyclic heteroaromatic bioisosteres. Nat. Synth 5, 790–797 (2026). https://doi.org/10.1038/s44160-026-00990-0
Palavras-chave: fotquímica, bioisóstero, design de fármacos, heterociclos, catálise por luz visível