Clear Sky Science · sv
Att bryta "regel-om-fem" för att nå bryggade bicykliska heteroaromatiska bioisosterer
Varför tredimensionella piller spelar roll
Många moderna läkemedel byggs av platta, ringformade molekyler som passar in i proteintargets ungefär som nycklar i lås. Kemister har lärt sig att byta ut dessa platta delar mot små tredimensionella ramverk kan göra att läkemedel blir mer vattenlösliga, får längre halveringstid i kroppen och blir mindre benägna att brytas ner på oönskade sätt. Den här artikeln behandlar en ny metod för att bygga sådana 3D-byggstenar som kan ge läkemedelsutvecklare nya alternativ när de finjusterar hur ett läkemedel beter sig.
Från platta ringar till små ramverk
Läkemedelsmolekyler innehåller ofta kvävebärande ringar, vilka är vanliga i godkända läkemedel men kan ha problem som snabb metabolism. Under de senaste åren har kompakta, bur-liknande strukturer kallade bryggade bicykler framträtt som "ersättare" för enkla bensenringar, eftersom de erbjuder en mer tredimensionell form samtidigt som de behåller avstånden mellan viktiga atomer. Däremot har nära släktingar som imiterar kväveinnehållande ringar varit mycket svårare att framställa, särskilt varianter där ett kväve sitter i en påfrestad fyrledsring. Dessa sällsynta ramverk, kända som 6-azabicyclo[3.1.1]heptaner, förväntas ha attraktiva egenskaper men har saknat generella syntestrategier.
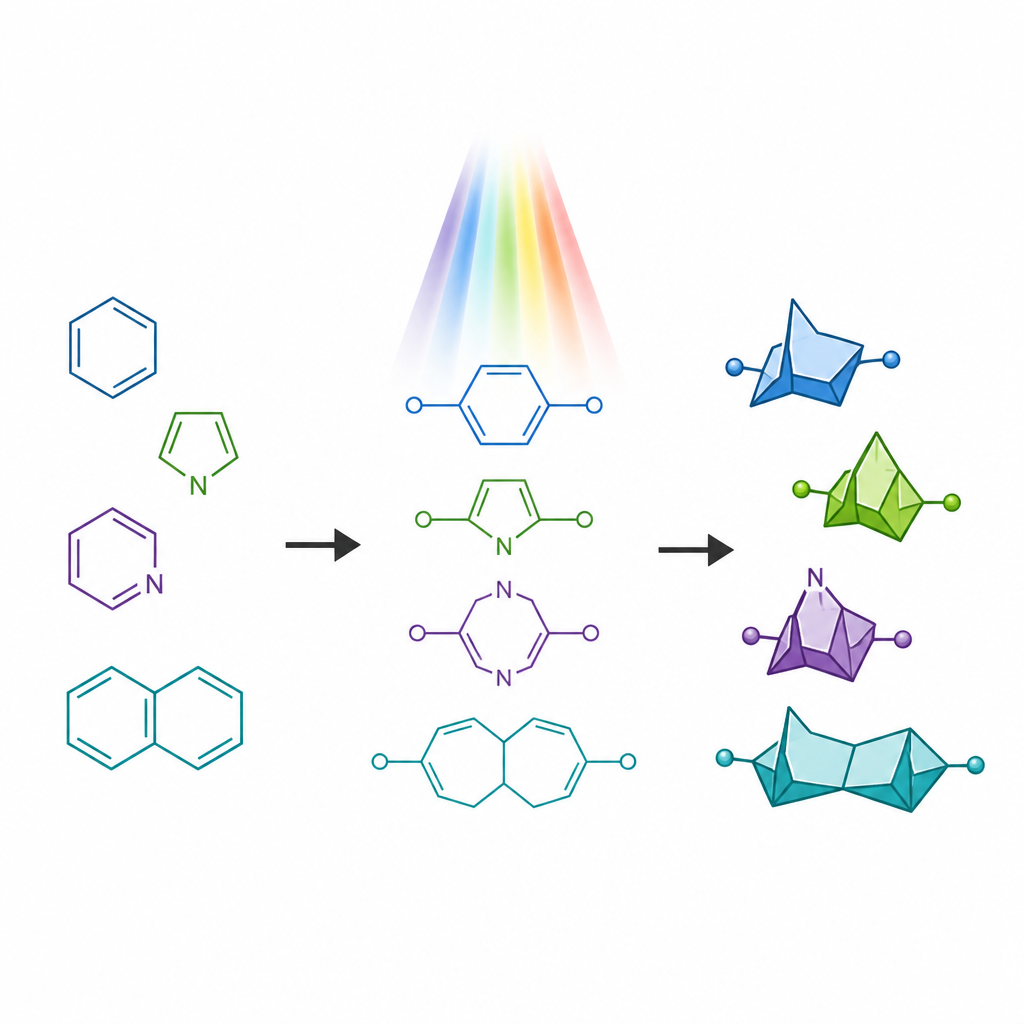
Att bryta en gammal regel för ringbildning
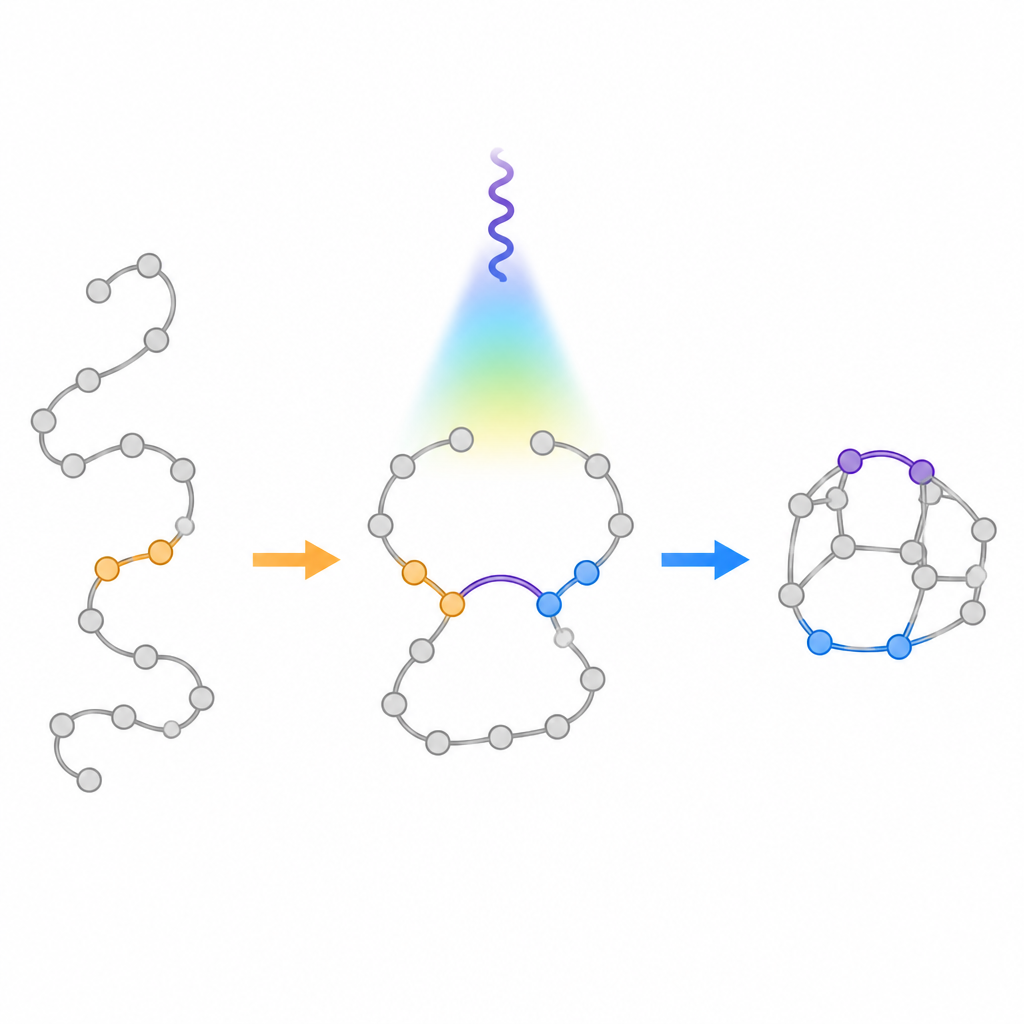
Traditionella ljusstyrda metoder för att förvandla flexibla kedjor till ringar tenderar att följa en gammal vägledning kallad "regel-om-fem", som gynnar bildandet av femledsringar framför sexledsringar. När kemister bestrålar vissa kedjelika molekyler med två dubbelbindningar, veckar de sig vanligtvis ihop till mindre fuserade ringar i stället för de större bryggade burarna som önskas här. Författarna satte som mål att avsiktligt överskrida denna partiskhet. De designade speciella startmaterial kallade aza-1,6-diener som innehåller både en kol-kol-dubbelbindning och en kol-kväve-dubbelbindning länkade i samma kedja. Genom att placera en grupp som stabiliserar radikaler i en specifik position i kedjan försökte de sakta ner den vanliga femledsringsvägen och i stället styra molekylen mot den sexledrade bryggade buren.
Använda milt ljus för att leda omvandlingen
Gruppen utvecklade en process med synligt ljus som använder en fotokatalysator för att överföra energi till aza-1,6-dienerna utan att ändra deras laddning. När dessa molekyler exciteras bildas kortvarigt ett biradikalt mellanläge där två reaktiva centra kan sluta sig på olika sätt. Beräkningar visade att en fenylring i nyckelpositionen skulle stabilisera en av dessa radikaler och höja barriären för den oönskade femledsringens slutning. Experiment bekräftade denna design: under blås ljus i närvaro av en iridium-baserad sensitisator veckades kedjorna konsekvent till de avsedda bryggade bicyklerna, med endast små mängder fuserade biprodukter. Reaktionen fungerade för många olika påhängda ringar, inklusive fragment hämtade från verkliga läkemedel, och kunde skalas upp till gramkvantiteter.
Bygga ett verktygslåda från de nya burarna
När de nya 6-kväve-bryggade ramverken var tillgängliga visade författarna att de kan modifieras vidare på många sätt. En mångsidig produkt med en vinylgrupp omvandlades till alkoholer, syror, aminer och andra användbara funktionella grupper genom standardsteg som reduktion, ozonolys och oxidation. Parallellt kunde kväve-oxygen-bindningen inom buren reduceras för att blotta en sekundär amin, som sedan kunde modifieras med ureakomponenter, sulfonamider, karbamater och amider. Denna rika efterföljande kemi innebär att den styva kärnan kan bära en mängd olika sidokedjor, ett krav för att utforska struktur-aktivitetssamband i läkemedelsupptäckt.
Testa de nya formerna i en läkemedelslik miljö
För att undersöka hur dessa burar kan prestera i ett biologiskt sammanhang byggde forskarna en analog till en känd enzymhämmare genom att byta ut en flexibel piperazinsring mot en ny 3,6-diazabicyclo[3.1.1]heptane-kärna. Mätningar i humana levermikrosomer visade att den modifierade molekylen hade något högre molekylvikt men lägre lipofilicitet, en förändring som ofta kopplas till bättre löslighet, samtidigt som den behöll liknande metabolisk stabilitet som ursprungskomponenten. Dessa tidiga resultat tyder på att de nya ramverken kan ersätta vanliga kväveringar utan att skada viktiga läkemedelsliknande egenskaper.
Vad detta betyder för framtida läkemedel
Enkelt uttryckt visar studien hur man kan få ljusexciterade molekyler att bryta en gammal preferens för mindre ringar och istället bilda kompakta tredimensionella burar som nära efterliknar välkända kväveinnehållande ringar. Eftersom dessa nya former lätt kan dekoreras och verkar vara metabolt robusta, erbjuder de medicinska kemister nya komponenter att sätta in i läkemedelsdesigner när man justerar löslighet, stabilitet och form. Medan mer biologisk testning krävs, öppnar denna anti-"regel-om-fem"-strategi upp nytt kemiskt utrymme som kan hjälpa framtida läkemedel att fungera bättre och vara längre verkande i kroppen.
Citering: Zhang, ZX., Shu, K., Tilby, M.J. et al. Breaking the ‘rule-of-five’ to access bridged bicyclic heteroaromatic bioisosteres. Nat. Synth 5, 790–797 (2026). https://doi.org/10.1038/s44160-026-00990-0
Nyckelord: fotokemi, bioisoster, läkemedelsdesign, heterocykliska föreningar, katalys med synligt ljus