Clear Sky Science · fr
Briser la « règle des cinq » pour accéder à des hétéroarènes bridgées bicycliques bioisostères
Pourquoi des pilules tridimensionnelles comptent
De nombreux médicaments modernes sont constitués de molécules en forme d’anneaux plats qui s’insèrent dans des cibles protéiques comme des clés dans des serrures. Les chimistes ont montré que remplacer ces éléments plats par de petits cadres tridimensionnels peut parfois rendre les médicaments plus solubles, plus durables dans l’organisme et moins susceptibles de se dégrader de façon indésirable. Cet article explore une nouvelle façon de construire ces blocs 3D qui pourrait offrir aux concepteurs de médicaments des options inédites pour ajuster le comportement d’un médicament.
Des anneaux plats aux petits cadres
Les molécules médicamenteuses contiennent souvent des cycles portant de l’azote, fréquents dans les médicaments approuvés mais susceptibles de présenter des problèmes tels qu’un métabolisme rapide. Ces dernières années, des structures compactes en forme de cage appelées bicycliques bridgées ont émergé comme des « substituts » des simples noyaux benzéniques, offrant une forme plus tridimensionnelle tout en conservant l’espacement des atomes clés. Cependant, leurs analogues qui imitent des cycles contenant de l’azote ont été beaucoup plus difficiles à synthétiser, notamment les versions où un atome d’azote se trouve dans un cycle contraint à quatre atomes. Ces cadres rares, connus sous le nom de 6-azabicyclo[3.1.1]heptanes, sont supposés posséder des propriétés prometteuses mais manquaient de voies synthétiques générales.
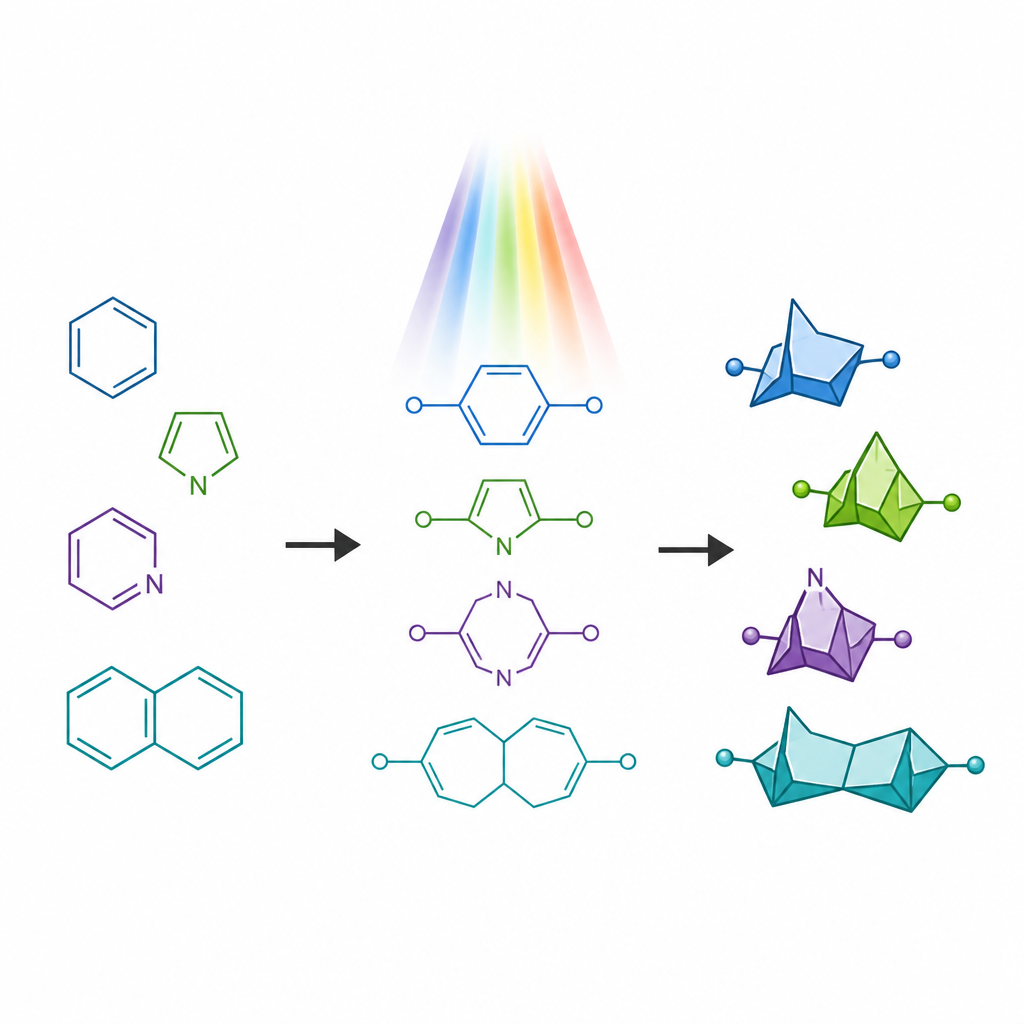
Briser une vieille règle de construction d’anneaux
Les méthodes traditionnelles photochimiques pour transformer des chaînes flexibles en cycles tendent à respecter une vieille ligne directrice appelée « règle des cinq », qui favorise la formation d’anneaux à cinq atomes plutôt que d’anneaux à six atomes. Quand on éclaire certaines molécules en chaîne contenant deux doubles liaisons, elles se replient généralement en donnant des cycles condensés plus petits plutôt que les cages bridgées plus grandes recherchées ici. Les auteurs ont cherché à renverser délibérément ce biais. Ils ont conçu des matériaux de départ particuliers appelés aza-1,6-diènes qui contiennent à la fois une double liaison carbone–carbone et une double liaison carbone–azote reliées le long de la même chaîne. En plaçant un groupe qui stabilise les radicaux à une position spécifique de la chaîne, ils visaient à ralentir la voie menant au cycle à cinq membres et à orienter la molécule vers la cage bridgée à six membres.
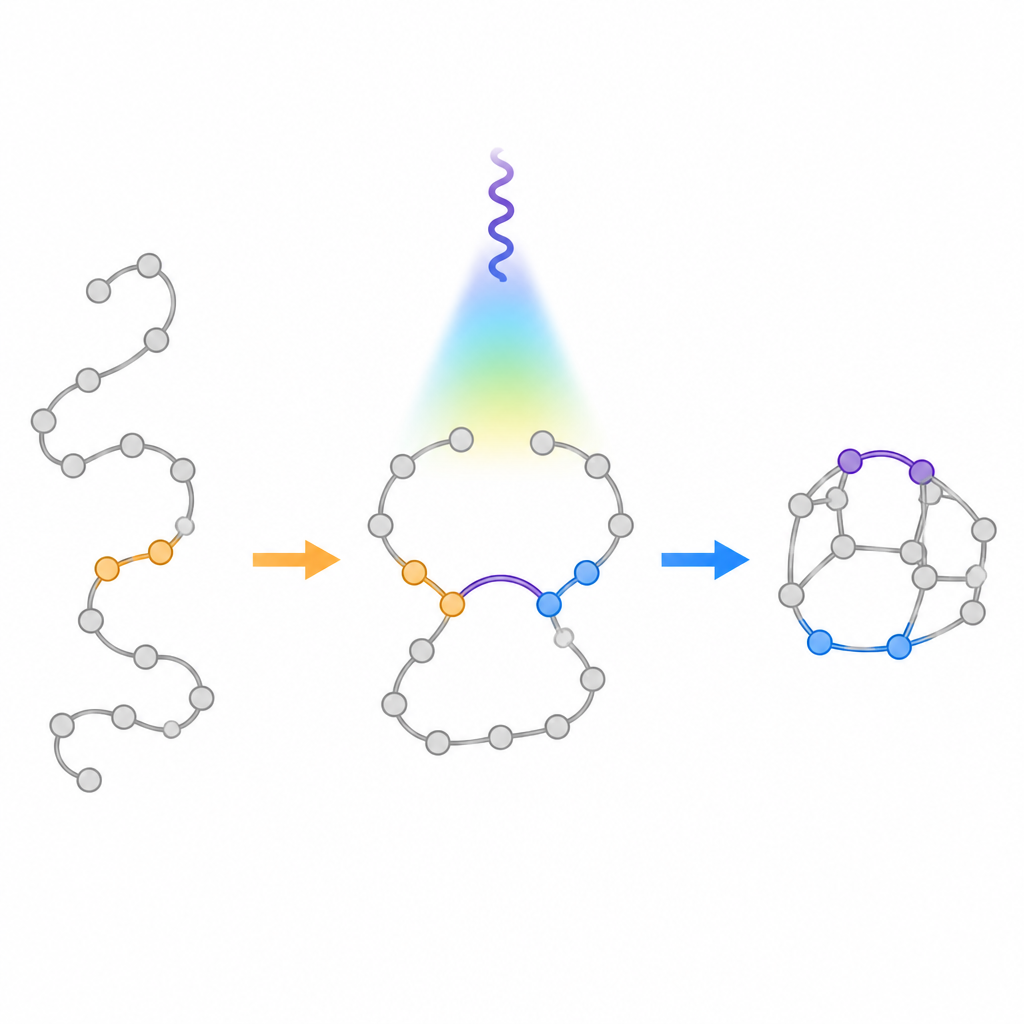
Utiliser une lumière douce pour guider la transformation
L’équipe a développé un procédé à la lumière visible qui utilise un photocatalyseur pour transférer de l’énergie aux aza-1,6-diènes sans modifier leur charge. Une fois excitées, ces molécules forment brièvement un intermédiaire biradical dans lequel deux sites réactifs peuvent se refermer de manières différentes. Des calculs informatiques ont suggéré que l’ajout d’un groupe phényl à la position clé stabiliserait l’un de ces radicaux et élèverait la barrière pour la fermeture indésirable en cycle à cinq membres. Les expériences ont confirmé cette conception : sous lumière bleue en présence d’un sensibilisateur à base d’iridium, les chaînes se sont repliées de manière fiable pour donner les bicycliques bridgés ciblés, avec seulement de faibles quantités de sous-produits condensés. La réaction a fonctionné avec de nombreux cycles substitués, y compris des fragments issus de médicaments réels, et pouvait être montée à l’échelle en quantités grammes.
Construire une boîte à outils à partir des nouvelles cages
Une fois les nouveaux cadres bridgés à 6 atomes d’azote obtenus, les auteurs ont montré qu’ils peuvent être modifiés dans de nombreuses directions. Un produit polyvalent portant un groupe vinyle a été transformé en alcools, acides, amines et autres fonctions utiles par des étapes classiques telles que l’hydrogénation, l’ozonolyse et l’oxydation. Parallèlement, la liaison azote–oxygène à l’intérieur de la cage pouvait être réduite pour révéler une amine secondaire, qui a ensuite été fonctionnalisée par des urées, sulfonamides, carbamates et amides. Cette chimie de suivi riche signifie que le noyau rigide peut supporter une grande variété de chaînes latérales, exigence clé pour explorer les relations structure–activité en découverte de médicaments.
Tester les nouvelles formes dans un contexte semblable à un médicament
Pour évaluer la performance potentielle de ces cages en contexte biologique, les chercheurs ont construit un analogue d’un inhibiteur enzymatique connu, en remplaçant un cycle piperazine flexible par un nouveau noyau 3,6-diazabicyclo[3.1.1]heptane. Des mesures dans des microsomes hépatiques humains ont montré que la molécule modifiée présentait un poids moléculaire légèrement plus élevé mais une lipophilicité réduite, un changement souvent associé à une meilleure solubilité, tout en conservant une stabilité métabolique similaire au composé d’origine. Ces premiers résultats suggèrent que les nouveaux cadres peuvent remplacer des cycles azotés courants sans nuire aux propriétés clés des médicaments.
Ce que cela signifie pour les médicaments futurs
En termes simples, l’étude montre comment contraindre des molécules excitées par la lumière à enfreindre une vieille préférence pour les petits cycles afin de former des cages compactes tridimensionnelles qui imitent étroitement des cycles contenant de l’azote familiers. Parce que ces nouvelles formes peuvent être facilement fonctionnalisées et semblent robustes sur le plan métabolique, elles offrent aux chimistes médicinaux de nouvelles pièces à intégrer dans des conceptions de médicaments pour ajuster la solubilité, la stabilité et la forme. Bien que des tests biologiques supplémentaires soient nécessaires, cette stratégie « anti‑règle des cinq » ouvre un nouvel espace chimique qui pourrait aider les médicaments futurs à mieux fonctionner et à durer plus longtemps dans l’organisme.
Citation: Zhang, ZX., Shu, K., Tilby, M.J. et al. Breaking the ‘rule-of-five’ to access bridged bicyclic heteroaromatic bioisosteres. Nat. Synth 5, 790–797 (2026). https://doi.org/10.1038/s44160-026-00990-0
Mots-clés: photochimie, bioisostère, conception de médicaments, hétérocycles, catalyse à la lumière visible