Clear Sky Science · es
Rompiendo la “regla de los cinco” para acceder a bioisósteros heteroaromáticos bicicíclicos puenteados
Por qué importan las pastillas tridimensionales
Muchos medicamentos modernos se basan en moléculas en forma de anillo planas que encajan en las dianas proteicas como llaves en cerraduras. Los químicos han comprobado que sustituir estos fragmentos planos por marcos tridimensionales pequeños a veces puede hacer que los fármacos sean más solubles, perduren más tiempo en el organismo y se degraden menos de formas no deseadas. Este artículo explora una nueva manera de construir tales bloques 3D que podría ofrecer a los diseñadores de fármacos opciones frescas a la hora de ajustar el comportamiento de un medicamento.
De anillos planos a marcos minúsculos
Las moléculas farmacéuticas con frecuencia contienen anillos que llevan nitrógeno, frecuentes en fármacos aprobados pero susceptibles a problemas como el metabolismo rápido. En los últimos años han surgido estructuras compactas en forma de jaula llamadas bicicletas puenteadas como “sustitutos” del benceno simple, ofreciendo una forma más tridimensional mientras mantienen un espaciamiento similar de átomos clave. Sin embargo, parientes cercanos que imiten anillos que contienen nitrógeno han sido mucho más difíciles de preparar, especialmente las versiones donde un átomo de nitrógeno forma parte de un anillo tensionado de cuatro miembros. Estos marcos poco comunes, conocidos como 6-azabicyclo[3.1.1]heptanos, se predicen con propiedades atractivas pero han carecido de rutas sintéticas generales.
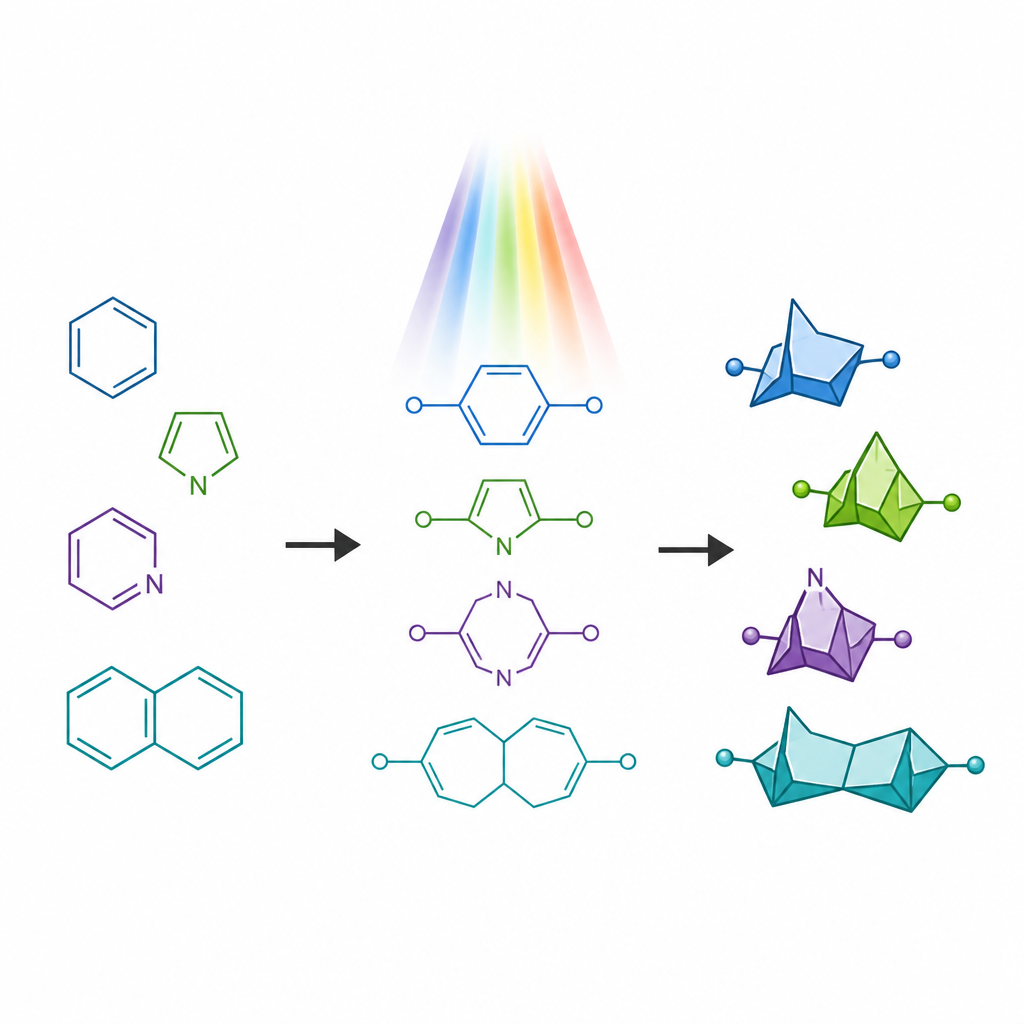
Rompiendo una antigua regla de construcción de anillos
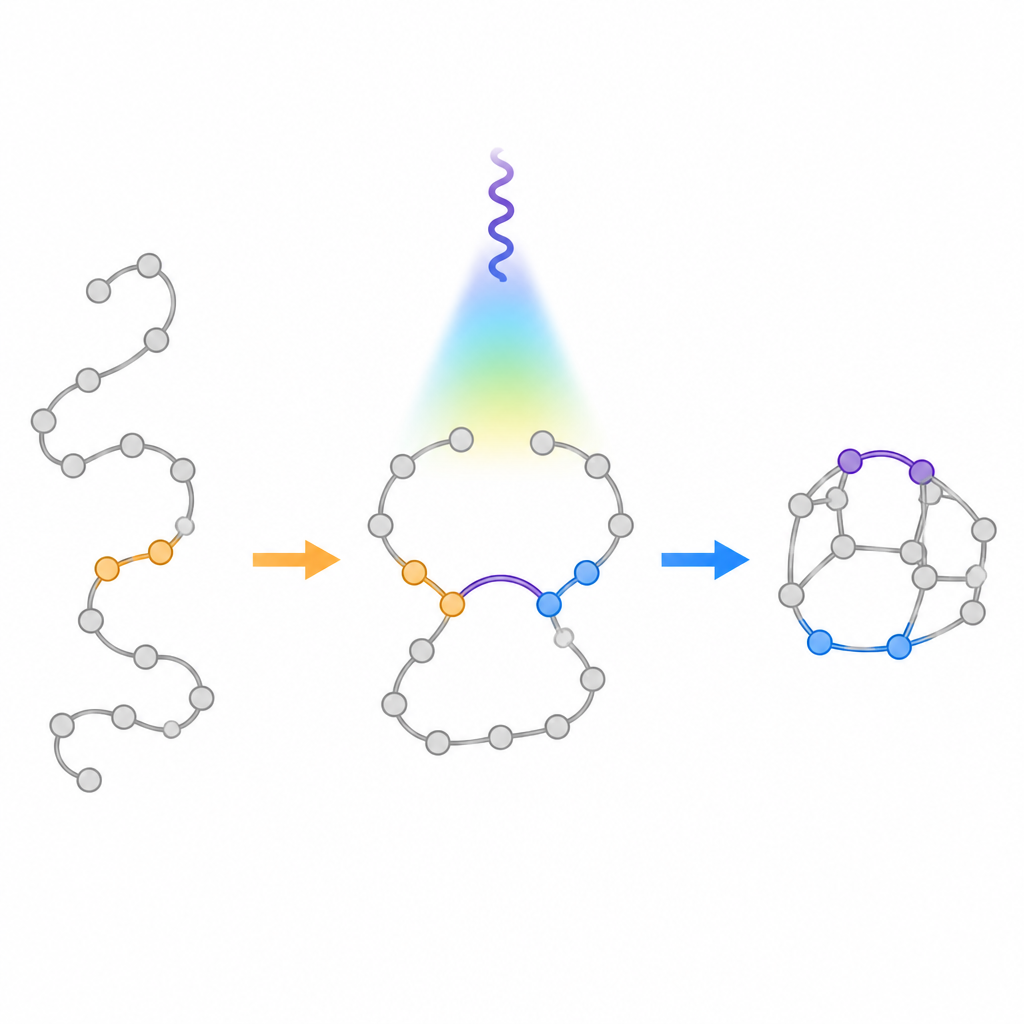
Los métodos tradicionales impulsados por luz para convertir cadenas flexibles en anillos tienden a seguir una pauta antigua llamada “regla de los cinco”, que favorece la formación de anillos de cinco miembros frente a los de seis. Cuando los químicos iluminan ciertas moléculas con dos dobles enlaces, suelen plegarse para dar anillos fusionados más pequeños en lugar de las grandes jaulas puenteadas deseadas aquí. Los autores se propusieron deliberadamente revertir este sesgo. Diseñaron materiales de partida especiales denominados aza-1,6dienos que contienen tanto un doble enlace carbono–carbono como un doble enlace carbono–nitrógeno enlazados en la misma cadena. Al colocar un grupo que estabiliza radicales en una posición específica de la cadena, buscaron ralentizar la vía habitual hacia el anillo de cinco miembros y, en su lugar, dirigir la molécula hacia la jaula puenteada de seis miembros.
Usando luz suave para guiar la transformación
El equipo desarrolló un proceso con luz visible que emplea un fotocatalizador para transferir energía a los aza-1,6dienos sin cambiar su carga. Una vez excitadas, estas moléculas forman brevemente un intermedio birradical en el que dos sitios reactivos pueden cerrarse de diferentes maneras. Cálculos computacionales sugerían que fijar un anillo fenilo en la posición clave estabilizaría uno de estos radicales y aumentaría la barrera para el cierre indeseado en cinco miembros. Los experimentos confirmaron este diseño: bajo luz azul en presencia de un sensibilizador a base de iridio, las cadenas se plegaron de forma fiable hacia las bicicletas puenteadas deseadas, con solo pequeñas cantidades de los subproductos fusionados. La reacción funcionó con muchos anillos distintos unidos, incluidos fragmentos tomados de fármacos reales, y pudo escalarse a cantidades de gramos.
Construyendo una caja de herramientas a partir de las nuevas jaulas
Una vez obtenidos los nuevos marcos puenteados con 6 átomos de nitrógeno, los autores demostraron que pueden modificarse en múltiples direcciones. Un producto versátil que lleva un grupo vinilo se transformó en alcoholes, ácidos, aminas y otras funcionalidades útiles mediante pasos estándar como hidrogenación, ozonólisis y oxidación. Paralelamente, el enlace nitrógeno–oxígeno dentro de la jaula pudo reducirse para revelar una amina secundaria, que fue luego derivatizada con ureas, sulfonamidas, carbamatos y amidas. Esta rica química posterior significa que el núcleo rígido puede soportar una gran variedad de cadenas laterales, un requisito clave para explorar las relaciones estructura–actividad en el descubrimiento de fármacos.
Probando las nuevas formas en un contexto parecido a un fármaco
Para sondear cómo podrían comportarse estas jaulas en un contexto biológico, los investigadores construyeron un análogo de un conocido inhibidor enzimático, sustituyendo un anillo de piperazina flexible por un nuevo núcleo 3,6-diazabicyclo[3.1.1]heptano. Mediciones en microsomas hepáticas humanas mostraron que la molécula modificada tenía un peso molecular ligeramente mayor pero menor lipofilicidad, un cambio a menudo relacionado con mejor solubilidad, manteniendo una estabilidad metabólica similar al compuesto original. Estos resultados preliminares sugieren que los nuevos marcos pueden sustituir a anillos nitrogenados comunes sin perjudicar propiedades clave similares a las de los fármacos.
Qué significa esto para futuros medicamentos
En términos sencillos, el estudio muestra cómo inducir a moléculas excitadas por luz a romper una preferencia antigua por anillos más pequeños y, en su lugar, formar jaulas compactas tridimensionales que imitan de cerca anillos nitrogenados familiares. Dado que estas nuevas formas pueden decorarse con facilidad y parecen robustas frente al metabolismo, ofrecen a los químicos medicinales piezas nuevas para incorporar en diseños farmacológicos al ajustar solubilidad, estabilidad y forma. Aunque se requieren más pruebas biológicas, esta estrategia anti-“regla de los cinco” abre un nuevo espacio químico que podría ayudar a que futuros fármacos funcionen mejor y perduren más tiempo en el organismo.
Cita: Zhang, ZX., Shu, K., Tilby, M.J. et al. Breaking the ‘rule-of-five’ to access bridged bicyclic heteroaromatic bioisosteres. Nat. Synth 5, 790–797 (2026). https://doi.org/10.1038/s44160-026-00990-0
Palabras clave: fotochemistry, bioisósteros, diseño de fármacos, heterociclos, catálisis con luz visible