Clear Sky Science · zh
Fe/αKG 依赖脱羧酶 TraH 中揭示的盖环介导质子转移
为何一个微小可动环至关重要
在微生物体内,专门的蛋白悄然合成并改造复杂分子,其中包括潜在的抗生素。本研究聚焦于一种来自常见食物腐败真菌的蛋白 TraH。研究者揭示,TraH 中一个小而柔性的“盖”像可移动的闸门,控制酶如何切除底物的一部分,在某些情况下甚至决定整个反应走向何种化学改变。理解这个可动部件不仅加深了我们对自然催化剂工作机制的认知,也可能帮助科学家设计用于制药及其他重要化合物合成的新酶。
真菌在分子合成中的助力者
TraH 属于一大家族酶,它们利用铁和一种名为 α‑酮戊二酸的辅因子执行强力的氧化反应。这类酶是微生物化学的核心成员,参与合成诸如色素、毒素和类药物等“次级代谢产物”。在真菌 Penicillium crustosum 中,TraH 有助于产生 terrestric acid,这是一种具有潜在抗菌和抗病毒活性的化合物。TraH 的主要功能是从名为 crustosic acid 的前体分子上切除一个二氧化碳基团,同时在分子中引入一个双键。有趣的是,TraH 也能作用于同一化合物的甲基酯近亲,在那种情况下它仅引入双键而不去除二氧化碳。
一个闭合的盖重塑活性位点
通过 X 射线晶体学,作者捕捉到了 TraH 在不同状态下的高分辨率快照:空状态、仅结合金属态,以及结合金属并结合 crustosic acid 或其甲基酯的状态。所有构象都共享一个双层 β‑螺旋形的刚性核心,该核心固定催化反应发生的铁原子。缠绕在这核心周围的是蛋白两端的额外片段,其中一个位于前端的环表现得像一个盖子。在未结合状态下,这个盖子松散并在晶体结构中部分不可见,表明它是游移的。当真正的羧酸底物结合时,盖子下摆、变得有序,并与附近的螺旋一道封闭活性位点,使底物深陷在一个封闭口袋内。而对于甲基酯底物,大部分盖仍然无序并向后拉开,显示其精确闭合依赖于所结合分子的性质。
基于水的质子中继通道
对与 crustosic acid 结合的闭合盖构象的更细致观察揭示出一个复杂的氢键网络,将盖子与酶核心中保守的赖氨酸(K191)及底物的羧基相连。关键的盖区残基有助于在 K191 与底物反应端之间定位一到两个水分子。为检验该网络的重要性,团队对盖和邻近核心的单个氨基酸进行了替换。破坏该网络的突变,尤其是在 Q99、D112、K114、K191 和 Y214 位点的改变,显著降低或消除了脱羧反应,而对邻近非网络残基的改变影响甚微。相反,这些破坏性突变大多几乎不影响酶对甲基酯底物进行去饱和(引入双键)的能力,表明该水介导网络对二氧化碳丢失这一特定过程至关重要。
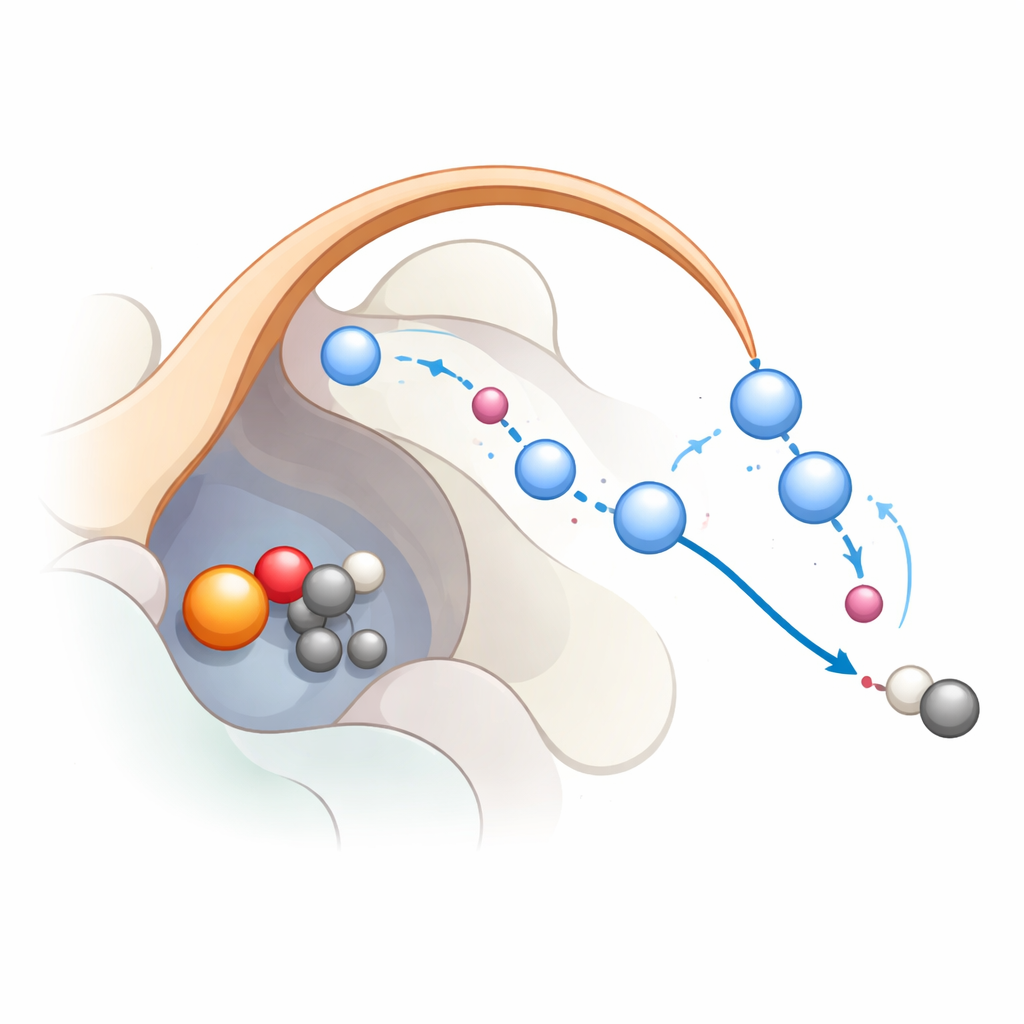
逐步追踪反应过程
为了观察该网络在反应过程中如何实际工作,研究者将经典分子动力学与更高级的量子力学模拟结合。他们从铁已形成高反应性铁‑氧中间体的状态开始,这是该酶家族的常见中间体。计算支持一个三步途径:首先,铁‑氧从底物抽取一个氢原子,生成自由基;第二,电子返移到铁上,帮助底物脱去二氧化碳;第三,铁结合的羟基被重新质子化,使铁回到其休眠态。模拟显示,K191 与盖环稳定的一连串水分子构成了一个质子中继,在最后步骤中高效搬运质子。当该中继被破坏时,反应在能量上变得不利,这与突变学数据吻合。
引导酶进化的可适应环
超越 TraH 本身,作者比较了共享相同铁结合核心却执行不同化学任务的相关酶。许多此类酶也携带类似盖的环,但它们的长度、序列和运动程度差异很大。有些酶中,环会牢牢闭合于底物之上并形成关键氢键;而在另一些中,环保持开放,似乎并不参与化学反应。通过构建进化树和分析序列模式,团队发现 TraH 氢键网络中涉及的某些盖区残基高度保守,而其他位置的变异则与不同底物偏好相对应。这表明进化通过调节这些环的刚性和化学性质来识别新分子并将反应偏向特定产物。
对未来化学的意义
对非专业读者而言,核心信息是:酶表面一个小而柔性的环能够控制质子和水分子在内部的流向,而这种控制可以决定一个分子是仅丢失一个氢还是也丢失二氧化碳。在 TraH 中,盖的作用不仅是封闭活性位点,还由氨基酸和困 trapped 的水分子组装成一个微小的质子转移装置。这种由环介导的策略不同于许多相关酶,它们通常在离去基团旁放置一个固定的碱性残基。通过揭示这一替代设计,这项工作拓宽了我们对自然如何构建多功能催化剂的理解,并为工程可重新布线其可动部件以催生新反应和新生物活性分子的酶提供了蓝图。
引用: Zheng, X., Ge, R., Guo, Z. et al. Lid loop-mediated proton transfer revealed in the Fe/αKG-dependent decarboxylase TraH. Commun Chem 9, 159 (2026). https://doi.org/10.1038/s42004-026-01986-9
关键词: 酶的机制, 非血红素铁酶, 质子转移, 真菌次级代谢, 酶的进化