Clear Sky Science · ar
كشف نقل البروتون بواسطة غطاء حلقي في ديكاربوكسيلاز TraH المعتمد على الحديد/αKG
لماذا يهم غطاء صغير متحرك
داخل الميكروبات، تبني بروتينات متخصصة بهدوء وتعيد تشكيل جزيئات معقدة، بما في ذلك جزيئات قد تصبح مضادات حيوية. تركز هذه الدراسة على بروتين واحد من هذا النوع، يدعى TraH، من فطر شائع يفسد الطعام. يكشف الباحثون أن "غطاء" صغير مرن في TraH يعمل كبوابة قابلة للتحرك تتحكم في كيفية إزالة جزء من الجزيء، وفي بعض الحالات تساعد في تحديد نوع التغيير الكيميائي الذي يحدث. لا يثري فهم هذا الجزء المتحرك صورتنا عن كيفية عمل المحفزات الطبيعية فحسب، بل يمكن أن يساعد العلماء أيضاً في تصميم إنزيمات جديدة لصنع أدوية ومركبات قيّمة أخرى.
مساعد فطري في تصنيع الجزيئات
ينتمي TraH إلى عائلة كبيرة من الإنزيمات التي تستخدم الحديد وجزيئاً مساعداً يُدعى α‑كيتوجلوتارات لإجراء تفاعلات أكسدة قوية. تلعب هذه الإنزيمات دوراً مركزياً في كيمياء الميكروبات، حيث تساعد في بناء "المنتجات الثانوية" مثل الأصباغ والسموم والجزيئات الشبيهة بالأدوية. في الفطر Penicillium crustosum، يساعد TraH في إنتاج حمض terrestric، وهو مركب له خصائص مضادة للبكتيريا والفيروسات واعدة. الوظيفة الأساسية لـ TraH هي قطع مجموعة ثاني أكسيد الكربون من سلف يُدعى حمض crustosic، مع إدخال رابطة مزدوجة في الجزيء في الوقت نفسه. ومن المثير للاهتمام أن TraH يمكنه أيضاً العمل على نسخة ميثيل‑إستر قريبة الصلة من نفس المركب، لكن في هذه الحالة يقتصر تأثيره على إدخال الرابطة المزدوجة دون إزالة ثاني أكسيد الكربون.
غطاء يغلق يعيد تشكيل الموقع النشط
باستخدام البلورة بالأشعة السينية، التقط المؤلفون لقطات عالية الدقة لـ TraH في حالات مختلفة: خالية، مرتبطة بالمعدن فقط، ومرتبطة بالمعدن ومعها إما حمض crustosic أو استره الميثيلي. تشترك كل الأشكال في لب ثابت ذا شكل شِرارة بيتا ذات طبقتين، يحتفظ بذرة الحديد حيث تحدث الكيمياء. تلف حول هذا اللب مقاطع إضافية عند نهايات البروتين، ومنها حلقة قرب المقدمة تتصرف كغطاء. في الحالة غير المرتبطة، يكون هذا الغطاء مترنحاً وجزئياً غير مرئي في بنية البلورة، ما يدل على أنه يتجول. عند ارتباط الركيزة الحقيقية الكربوكسيلاتية، يهوي الغطاء لأسفل، ويصبح منظماً جيداً، ومع الهياكل اللولبية القريبة يختم الموقع النشط بحيث يجلس الجزيء عميقاً داخل جيب مغلق. أما بالنسبة لركيزة الاستر الميثيلي، فتبقى أجزاء كبيرة من الغطاء غير منظمة ومتنحّية للخلف، ما يُظهر أن إغلاقه الدقيق يعتمد على طبيعة الجزيء المرتبط.
مرحلة نقل تعتمد على الماء لتحريك البروتونات
أظهر الفحص الدقيق لبنية الغطاء المغلق مع حمض crustosic شبكة معقدة من الروابط الهيدروجينية تربط الغطاء بلِيسين محفوظ (K191) في لب الإنزيم وبالمجموعة الكربوكسيلية للركيزة. تساعد بقايا رئيسية في الغطاء على وضع جزيء أو اثنين من الماء بين K191 والنهاية المتفاعلة للركيزة. لاختبار أهمية هذه الشبكة، غيّر الفريق أحماض أمينية فردية في الغطاء واللب القريب. أدت الطفرات التي عطلت الشبكة، خصوصاً عند المواقع Q99 وD112 وK114 وK191 وY214، إلى تقليل أو إلغاء تفاعل إزالة الكربوكسيل بشدة، بينما كان لتغييرات في بقايا مجاورة غير جزء من الشبكة أثر ضئيل. بالمقابل، لم تؤثر معظم هذه الطفرات المعطلة تأثيراً كبيراً على قدرة الإنزيم على إجراء إزالة التشبع (desaturation) على ركيزة الاستر الميثيلي، مما يشير إلى أن الشبكة المتوسطة بالماء ضرورية خصوصاً لفقدان ثاني أكسيد الكربون.
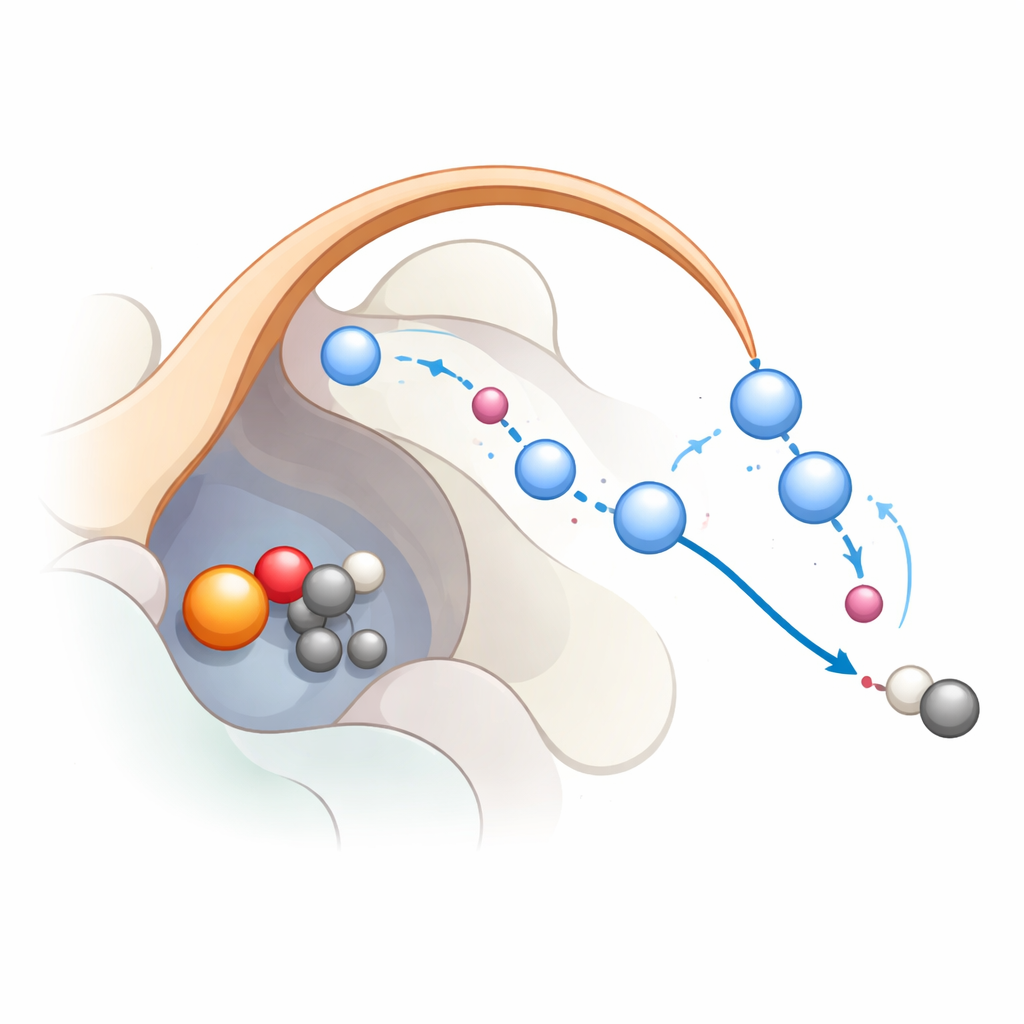
متابعة خطوة التفاعل خطوة بخطوة
لرؤية كيفية عمل هذه الشبكة أثناء التفاعل فعلاً، جمع الباحثون بين ديناميكيات جزيئية كلاسيكية ومحاكاة كمية متقدمة. انطلقوا من حالة حيث شكل الحديد بالفعل نوعاً شديد التفاعل من الحديد‑أوكْسو، وهو وسيط شائع في عائلة هذا الإنزيم. تدعم الحسابات مساراً مؤلفاً من ثلاث خطوات: أولاً، يسحب الحديد‑أوكْسو ذرة هيدروجين من الركيزة مكوناً جذراً؛ ثانياً، ينتقل إلكترون إلى الحديد، مما يساعد الركيزة على فقدان ثاني أكسيد الكربون؛ ثالثاً، يُعاد بروتنة مجموعة الهيدروكسيل المرتبطة بالحديد فيعود الحديد إلى حالته الراحة. تُظهر المحاكيات أن K191 وسلسلة جزيئات الماء المستقرة بفضل حلقة الغطاء تشكلان تتابع نقل بروتونات ينقّل البروتونات بكفاءة خلال الخطوات الأخيرة. عندما ينكسر هذا التتابع، يصبح التفاعل غير مواتٍ من الناحية الطاقية، مما يتوافق بدقة مع بيانات الطفرات.
حلقة قابلة للتكيف توجه تطور الإنزيمات
بعيداً عن TraH نفسه، قارن المؤلفون إنزيمات ذات صلة تشترك في نفس لب ربط الحديد لكنها تقوم بمهام كيميائية مختلفة. تحمل العديد من هذه الإنزيمات أيضاً حلقات شبيهة بالغطاء، لكن أطوالها وتسلسلاتها ودرجات حركتها تختلف على نحو واسع. في بعضها، يغلق الغطاء بقوة فوق الركائز ويشكل روابط هيدروجينية رئيسية؛ وفي أخرى يبقى مفتوحاً ولا يبدو أنه يشارك في الكيمياء. من خلال بناء أشجار تطورية وتحليل أنماط التسلسل، وجد الفريق أن بعض بقايا الغطاء المشاركة في شبكة الروابط الهيدروجينية في TraH محفوظة بشدة، بينما تتنوع مواقع أخرى بطريقة تتتبع تفضيلات الركائز المختلفة. يقترح هذا أن التطور يضبط كل من صلابة الكيمياء لهذه الحلقات للتعرف على جزيئات جديدة ولتوجيه التفاعلات نحو نتائج معينة.
ما الذي يعنيه هذا للكيمياء المستقبلية
لغير المتخصصين، الرسالة الأساسية هي أن حلقة صغيرة مرنة على سطح الإنزيم يمكن أن تتحكم في مسار حركة البروتونات وجزيئات الماء داخله، وأن هذا التحكم يمكن أن يحدد ما إذا فقد الجزيء هيدروجيناً فقط أم فقد أيضاً ثاني أكسيد الكربون. في TraH، لا يقتصر دور الغطاء على إغلاق الموقع النشط بل على تجميع آلة صغيرة لنقل البروتونات من أحماض أمينية ومياه محبوسة. تختلف هذه الاستراتيجية القائمة على الغطاء عن نهج العديد من الإنزيمات ذات الصلة، التي تستخدم بقايا أساسية ثابتة موضوعة بجوار المجموعة المغادرة مباشرة. من خلال الكشف عن هذا التصميم البديل، توسع الدراسة فهمنا لكيفية بناء الطبيعة لمحفزات متعددة الاستخدامات وتقدم مخططاً هندسياً لتعديل إنزيمات يمكن إعادة توصيل أجزائها المتحركة لصنع تفاعلات جديدة وجزيئات بيوفعّالة جديدة.
الاستشهاد: Zheng, X., Ge, R., Guo, Z. et al. Lid loop-mediated proton transfer revealed in the Fe/αKG-dependent decarboxylase TraH. Commun Chem 9, 159 (2026). https://doi.org/10.1038/s42004-026-01986-9
الكلمات المفتاحية: آليات الإنزيم, إنزيمات الحديد غير الهيمية, نقل البروتون, الأيض الثانوي الفطري, تطور الإنزيمات